Introduction
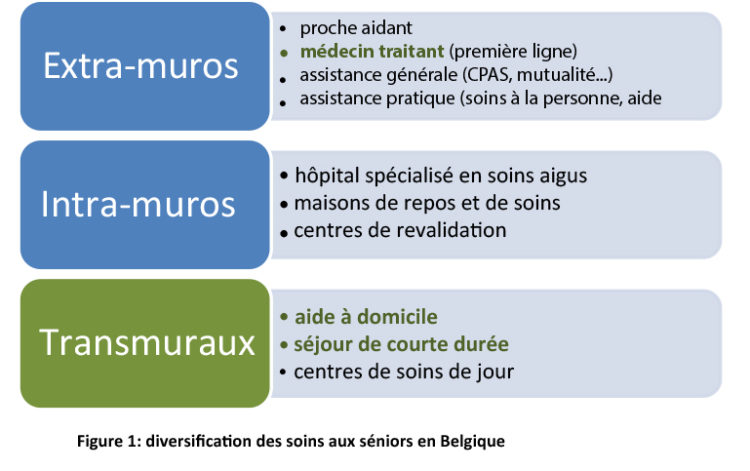
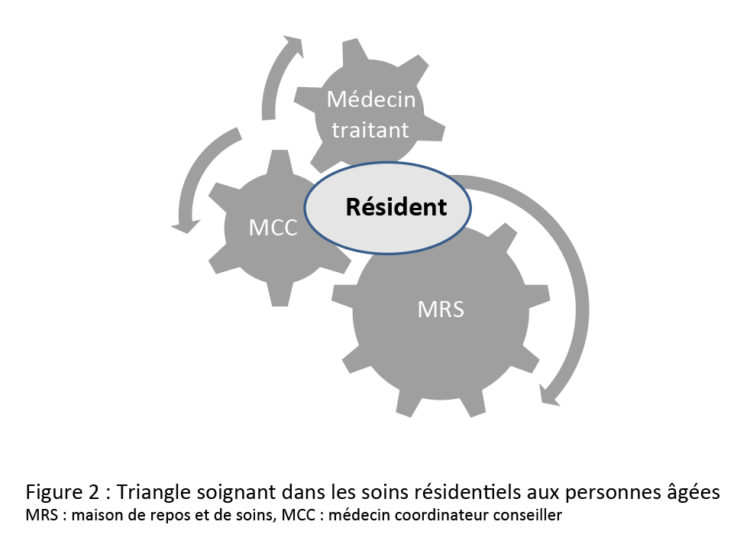
La population belge vieillit. D’ici 2030, les plus de 65 ans représenteront près de 25% de la population totale. Ce vieillissement de la population entraîne l’augmentation du nombre de personnes souffrant d’affections chroniques et de problèmes de dépendance, et donc également du besoin de soins et d’assistance. Dans notre pays, ces soins sont très diversifiés et peuvent être intramuraux, transmuraux ou extramuraux (Fig. 1). C’est dans les soins intramuraux que l’assistance médicale et paramédicale sont les plus importants. Dans les maisons de repos et de soins (MRS), le besoin structurel en matière de prévention et de maîtrise des infections liées aux soins est presque aussi important que dans les hôpitaux spécialisés dans les soins aigus. La mise en place et l’entretien de ces structures pour plus de 1.500 établissements spécialisés dans les maladies chroniques (contre une centaine d’hôpitaux spécialisés en soins aigus) en Belgique est un défi de taille (Fig. 2).
En avril 2009, tous les hôpitaux, MRS et MRPA (appelées MRS ci-après) de Belgique ont été invités à participer à un projet-pilote du Service Public Fédéral (SPF) Santé publique, sécurité de la chaîne alimentaire et environnement. Pour chaque communauté/région (Flandre, Wallonie, Bruxelles et Communauté germanophone), un groupe de projet a été choisi, composé d’au moins 3 et de maximum 8 MRS, ainsi que d’un hôpital spécialisé en soins pour la coordination. Les groupes de projet sélectionnés ont été appelés consortiums. Au niveau fédéral, le projet a été porté par le coordinateur de la Cellule Soins chroniques, soins aux personnes âgées et soins palliatifs du SPF santé publique, sécurité de la chaîne alimentaire et environnement.
L’étude a été menée en deux temps : une étude de faisabilité a d’abord été mise en route pendant 18 mois (de janvier 2010 à juin 2011) pour mettre en place les structures, expertises et ressources nécessaires à la maîtrise des infections ; ensuite (en 2014), 2 consortiums supplémentaires ont été ajoutés afin de créer une base plus large pour mettre à l’épreuve et valider les recommandations issues de la première partie de l’étude. Cette partie de l’étude comprenait également une obligation de résultat et requérait donc un rapport final commun destiné au Fédéral. Pendant l’étude, les compétences relatives aux soins aux personnes âgées ont été définitivement transférées aux Régions. Les compétences relatives aux maisons de repos et de soins ont été transférées aux Régions et Communautés le 1er juillet 2014.
Pour la Flandre, nous avons eu l’opportunité de participer tout au long du trajet avec une équipe composée de 8 MRS (nombre de lits passant de 861 à 937) et d’un hôpital spécialisé en soins aigus (805 lits). Dans cet article, nous décrivons notre expérience en tant que consortium. Dans le descriptif, nous mettons l’accent sur le chemin que nous avons parcouru ensemble. Nous donnons un aperçu des barrières et des opportunités que nous avons rencontrées tout au long de ce projet-pilote.
Ressources matérielles et méthodes
Un groupe de base et un groupe de projet ont été mis en place au sein de chaque consortium. Le groupe de base rassemble les leaders des différents secteurs représentés dans le groupe. Outre les 2 médecins coordinateurs conseillers (MCC) et 2 infirmiers issus des maisons de repos et de soins participantes, on y retrouve également 3 représentants de l’hôpital coordinateur, à savoir le chef de service des soins gériatriques (G) et membre du groupe de travail de liaison gériatrique. fonctionnelle, le médecin et l’infirmier responsables de la prévention des infections. Ils font office de groupe de réflexion, préparent les réunions du consortium et élaborent les décisions qui bénéficient d’un soutien. Au sein du groupe, ce sont eux les responsables de l’organisation du symposium final et du rapport final. Le groupe de projet rassemble tous les représentants possibles des MRS participantes. Outre les infirmiers et MCC, on peut également y retrouver des médecins du travail et des responsables de la qualité. Ils évaluent et révisent le travail préparatoire du groupe de base et sont également responsables en bout de course de la mise en œuvre des missions dans leur établissement respectif.
En outre, la 1ere partie de l’étude impose d’évaluer la faisabilité de la mise en place d’un nombre de structures en matière de prévention des infections. Les structures présentées, l’équipe et le comité en charge de la politique générale en matière d’infections liées aux soins (PGIS) sont représentatives de l’organisation de prévention des infections, avec une équipe et un comité de prévention des infections au sein de l’hôpital spécialisé en soins aigus. Il était également obligatoire de participer aux études de prévalence ponctuelle « Healthcare Associated Infections and Antimicrobial use in European Long-Term Care Facilities » (HALT 1) et « Multi-drug Resistant Organism (MDRO) » (SARM et BSLE). La première partie de l’étude a été bouclée avec un symposium local du consortium en juin 2011 et un symposium fédéral en octobre 2011.
La 2e partie de l’étude s’est penchée sur la consolidation des structures mises en place dans la 1re partie, mais aussi sur 8 thèmes spécifiques. Notre consortium s’est chargé de l’enregistrement et de la surveillance des infections avec création d’un registre des infections et d’une collaboration (échange d’informations et soutien) transmurale via la liaison gériatrique fonctionnelle et une liaison externe.
Résultats
Structures
Du matériel relatif à l’hygiène des mains et des équipements de protection individuelle ont été achetés et de petites adaptations ont été apportées aux infrastructures pour les optimiser. Ce type de dépenses peut vite monter en flèche pris individuellement par chaque établissement . En outre, on a appris à utiliser le règlement de travail pour augmenter le respect des accords et des procédures. La présence et l’apport du médecin du travail, des médecins généralistes et des infirmiers (en chef) dans le comité PGIS ont représenté une plus-value. Ces derniers peuvent également faire office de référents en matière de prévention des infections dans leur service. L’équipe et le comité PGIS peuvent faire appel à l’expertise de l’équipe d’hygiène hospitalière de l’hôpital spécialisé en soins aigus.
Les membres du consortium gardent un sentiment positif de leur collaboration. L’installation du groupe de base au sein du consortium constitue une plus-value évidente.
Processus
Tous les membres du consortium font état d’une augmentation claire de la prise de conscience en matière de prévention des infections liées aux soins. La participation au projet a donné lieu à une dynamique dans tous les secteurs de l’organisation de la MRS. L’hôpital spécialisé en soins aigus a appris à mieux connaître la problématique et les canaux de communication au sein de la MRS. L’installation de l’équipe PGIS apporte plus de clarté sur le lieu de travail. En effet, on sait mieux à qui s’adresser pour tout ce qui a trait à la prévention des infections liées aux soins. Les équipes peuvent se charger d’une formation interne à la mesure de la MRS et à la mesure du groupe-cible. L’installation d’un comité performant en matière de politique de lutte contre les infections liées aux soins n’a pas connu le même succès dans toutes les MRS. L’investissement en temps ne doit pas être sous-estimé : au-delà des réunions, une collaboration active à plusieurs projets est requise. Cela s’est avéré très compliqué pour les MRS dépourvues de structure qualité élaborée. Sans soutien financier supplémentaire, il est presque impossible de faire survivre les structures au-delà de l’étude. Il est ressorti clairement de ces études qu’une feuille de route uniforme s’imposait pour la prévention des infections liées aux soins. Depuis, la feuille de route en matière de politique de lutte contre les infections dans les maisons de repos et de soins flamandes, la « Draaiboek infectiebeleid in Vlaamse Woonzorgcentra – interactief », a été créée.
Une concertation entre les MRS et les hôpitaux s’impose. Cette communication transmurale peut être favorisée grâce à l’échange de données sur les infections liées aux soins et le statut de colonisation du patient/résident. La liaison gériatrique fonctionnelle et la liaison externe sont d’autres instruments déjà présents qui peuvent y contribuer. Il faut en outre permettre aux MRS d’avoir accès par voie électronique, sur une plateforme de communication standardisée, aux données relatives à l’admission et à la sortie, y compris aux directives relatives au suivi des infections liées aux soins.
Résultats
La participation à deux enquêtes (2011 et 2014) portant sur la prévention des infections liées aux soins chez les collaborateurs et médecins a révélé des points sensibles en interne quant à la vision et l’attitude adoptée en matière de précautions habituelles. Collaborer à des études de prévalence comme l’HALT et la MDRO permettent à la MRS d’avoir une meilleure vue sur ses propres chiffres. Cela permet d’introduire progressivement une culture de l’évaluation. Le registre des infections qui reprend tous les mois les résidents porteurs d’une infection représente un instrument accessible et pratique. Son utilisation est maintenue non seulement dans les MRS de notre consortium, mais aussi dans les autres consortiums du projet.
Nous nous référons ici au complément d’information du MCC ci-après (sous Ad 3).
Expériences d’un MCC
Plusieurs maisons de repos et de soins de Flandre-Orientale ont collaboré à ce projet fédéral entre 2010 et 2014 au sein d’un consortium avec l’AZ Sint-Lucas en vue de démarrer, améliorer et uniformiser la politique générale de lutte contre les infections liées aux soins. Grâce à des comités réunissant les MRS et les équipes internes, grâce à des formations complémentaires et une approche axée sur des missions sur le lieu de travail, les connaissances, aptitudes et attitudes relatives à la prévention, à la politique générale et à l’enregistrement des infections liées aux soins et aux germes multirésistants ont bénéficié d’une plus-value professionnelle.
En ma qualité de MCC, je peux affirmer que ce projet a donné de la substance et de la force à ma mission spécifique par rapport aux maladies infectieuses telles que décrites dans l’AR du 9/03/20142. Une collaboration passionnante s’est également mise en place avec d’autres maisons de repos et de soins et avec l’hôpital.
La littérature relative à la politique générale en cas d’infections à germes résistants a été approfondie et les conseils d’Evidence-Based Medicine (EBM – médecine fondée sur des données probantes) bénéficiant du plus haut degré de force de preuve ont été distribués : d’abord l’importance primordiale des mesures générales de précaution (hygiène des mains et équipements de protection individuelle), ensuite l’absolue nécessité d’une politique d’utilisation restrictive des antibiotiques (chaque « ligne » en médecine humaine, médecine vétérinaire, bio-industrie). Enfin, l’enregistrement en matière d’infections liées aux soins a été adapté.
Ad 1. les mesures de précautions générales
A chaque échelon de collaborateurs, un changement significatif s’est produit dans les MRS en matière de connaissance et d’attitude dans la prévention des infections. Pas uniquement grâce à la théorie apprise lors des mises à niveau, mais aussi grâce à des contrôles systématiques, poursuivis depuis, notamment sur les bijoux, l’utilisation et la consommation de lotion hydroalcoolique de gants jetables dans les services. Une interdiction de porter des bijoux est apparue dans le règlement de travail de toutes les maisons de repos et de soins. Les nouveaux collaborateurs et étudiants se voient communiquer les messages-clés des mesures de précautions générales, par ailleurs affichés dans chaque service. Les formations internes qui ont été entamées durant le projet ont connu une suite, au rythme d’une fois par an. Les médecins traitants qui viennent en visite sont priés de montrer l’exemple en matière d’hygiène des mains.
Ad 2. la politique d’utilisation restrictive d’antibiotiques
Il est demandé aux médecins traitants, lors des formations de mise à jour, des contacts individuels et par le biais de notes dans les dossiers, de prendre leurs responsabilités en matière d’antibiotiques. Ils sont priés de mettre leur liberté thérapeutique dans la balance face aux besoins sanitaires des communautés fermées.
Grâce au consortium, les MCC font passer le message à leurs collègues en visite, et des formations de mise à niveau ont été réparties à grande échelle : par le biais des réunions du groupe qualité local (LOK), de Domus Medica, ‘Wintermeeting Geriatrie’, ‘het Farmacotherapeutisch bijblijven’ à l’UZ de Gand, d’un article dans le Journal de la Médecine… Les médecins généralistes reçoivent les messages-clés suivants :
– Antibiotiques : cfr. la Commission belge de coordination de la politique antibiotique (BAPCOC) : spectre réduit, dose élevée, courte durée, pas de cure répétitive.
– En cas d’infection des voies respiratoires basses, cibler le pneumocoque qui est encore toujours sensible à la pénicilline ; en cas de résistance intermédiaire, on peut toujours augmenter la dose par la suite. Ce n’est qu’en cas de résistance totale (rare) ou d’allergie avérée induite par des anticorps IgE (très rare) qu’on évitera l’amoxicilline.
– Limiter le recours aux quinolones. En cas d’infection des voies respiratoires (voir plus haut) et d’infection urinaire, commencer avec de la nitrofurantoïne.
– Éviter ou restreindre l’utilisation prophylactique d’antibiotiques – l’uroprophylaxie est très élevée dans les maisons de repos !
– Suivre un arbre décisionnel lorsqu’une infection urinaire est diagnostiquée, ne pas commencer de traitement antibiotique sur base d’indications limitées comme une urine trouble ou malodorante. Partir du critère Mc Geer et procéder au test par bandelette réactive aux leucocytes et aux nitrites, et si ce dernier est négatif, exclure une infection urinaire. Si le test est positif aux leucocytes ou aux nitrites – en plus de présenter un critère Mc Geer positif – suivre le traitement recommandé par la BABCOC et le Formulaire de soins aux personnes âgées
– SARM : ne pas effectuer de dépistage systématique mais décontaminer en cas de résultat positif d’une culture. Autres MDRO : dépistage non indispensable, mais les mesures de précautions générales doivent être appliquées rigoureusement.
Ad 3. l’enregistrement des infections (liées aux soins)
Le MCC est tenu par la loi d’enregistrer les maladies infectieuses. Cela se passe différemment dans chaque maison de repos et de soins. Grâce au projet, le consortium a proposé au SPF – et ensuite à l’agence flamande des soins de santé – d’uniformiser cette obligation légale. Avec une approche en trois volets :
1. Résultats de laboratoire des cultures bactériennes, avec les MDRO qu’on y a isolés
2. Liste des infections cliniques par spécialités : gastro-intestinales, ORL/respiratoires, dermatologiques, urinaires etc.
3. Données pharmaceutiques avec la consommation de tous les antibiotiques, par classe.
Conclusion
Expériences : Quelques MRS du consortium continuent à travailler avec les structures installées d’équipe et comité de politique en matière d’infections liées aux soins. Dans la MRS où un infirmier voit une partie de son temps de travail dégagée pour la politique en matière d’infections liées aux soins, on est capable de mener une politique plus performante et cohérente. Dans d’autres MRS du consortium, les collaborateurs disposant de compétences adéquates (bachelor, master) ne sont pas en nombre suffisant pour pouvoir organiser une politique de lutte contre les infections liées aux soins, ou des collaborateurs qui disposent du profil de fonction adéquat doivent occuper des postes inférieurs d’une pénurie d’infirmiers.
Toutes les MRS reconnaissent le besoin et l’intérêt d’une formation et d’une remise à niveau régulières. Le pas est franchi pour organiser des formations continues en interne. Les procédures doivent être régulièrement revues/actualisées. Les infections liées aux soins ont été enregistrées grâce à l’élaboration d’un registre des infections, pratique et faisable.
Seule une répartition claire de ces études dans le temps permet de participer à l’enregistrement ou aux études de prévalence. La liaison gériatrique fonctionnelle est une plus-value évidente dans la réalisation d’une communication transmurale.
Le MCC et les MRS ont reçu le soutien de l’hôpital spécialisé en soins aigus pour améliorer tant d’un point de vue structurel que substantiel la théorie et la pratique relatives aux infections liées aux soins. L’hôpital spécialisé en soins aigus peut-il continuer à offrir ce soutien ?
Défis : La prévention est la pierre angulaire dans la maîtrise des infections dans tous les établissements de soins de santé, et il n’en va pas autrement pour les MRS. Que ce soit sur le terrain, au niveau de la direction ou dans la plume de chaque médecin, il convient de garder à l’esprit que les MDRO constituent une menace pour la santé publique, à fortiori dans les communautés fermées des personnes âgées vulnérables que sont nos MRS. Les mesures de précautions générales doivent être répétées à l’envi et les médecins doivent prescrire les antibiotiques de manière responsable. La feuille de route « Draaiboek infectiebeleid in Vlaamse Woonzorgcentra » est un instrument précieux3. Il faudrait rapidement en obtenir une traduction en français et en allemand.
Les évaluations qualitatives doivent devenir la norme dans les MRS. C’est possible grâce à un outil d’auto-évaluation que décrit le rapport final du projet, page 68.
Intégrer la maîtrise des infections liées aux soins avec une qualité des soins dans les établissements spécialisés dans les soins chroniques est un must. Dans cette optique, il est regrettable que le Vlaams Indicatoren Project voor woonzorgcentra (projet flamand d’indicateurs destinés aux MRS) n’évalue que le niveau de vaccination contre la grippe des prestataires de soins dans les indicateurs qualité des soins et sécurité à ce jour4.
L’enregistrement local des infections liées aux soins est nécessaire (évaluer, c’est savoir) et faisable grâce à l’élaboration d’un registre des infections. La participation à des études de prévalence est souhaitable, mais n’est possible que si ces études sont clairement étalées dans le temps, par ex. 1x/an.
La coopération transmurale, l’échange de données et le soutien peuvent être optimisés par le groupe de pilotage liaison gériatrique fonctionnelle et la liaison gériatrique externe.
En ce qui concerne la prévention et la prise en charge des infections liées aux soins dans les (±100) hôpitaux spécialisés en soins aigus, nous menons des actions depuis 30 ans déjà, avec des hauts et des bas. Pouvons-nous raisonnablement espérer faire pareil pour plus de 1.500 établissements spécialisés en soins chroniques d’ici quelques années ? Nous avons en tout cas constaté, dans le cadre du projet, que c’était possible, et cela nous gonfle d’espoir.
Références
1. Coordination P. Matthys, SPF Sané publique. Gestion des infections liées aux soins en MRS et MRPS, 6 consortiums. Rapport rédigé par le SPF Santé publique, sécurité de la chaîne alimentaire et environnement, 15 décembre 2014.
http://www.health.belgium.be/fr/gestion-des-infections-liees-aux-soins-en-mrs-et-mrpa
2. dimanche 9 mars 2014. — Arrêté royal modifiant l’arrêté royal du 21 septembre 2004 fixant les normes pour l’agrément spécial comme maison de repos et de soins, comme centre de soins de jour ou comme centre pour lésions cérébrales acquises http://www.ejustice.just.fgov.be/cgi/article_body.pl?language=fr&caller=summary&pub_date=14-04-10&numac=2014024114
3. Draaiboek infectiebeleid in Vlaamse woonzorgcentra (WZC). Van Houtte, T., Claesen, B., Haenen, R., Schuermans, A., Beke, A., & De Lepeleire, J. (2012). Brussel/Leuven: ACHG – VAZG – ACCO
4. Vlaams Indicatoren Project Woonzorgcentra: handleiding
https://www.zorg-en-gezondheid.be/sites/default/files/atoms/files/Handleiding%20over%20kwaliteitsindicatoren%20voor%20woonzorgcentra.pdf
Avec nos remerciements au consortium : WZC Domino-WZC Tempelhof, 9000 Gent, dr. Koen Verhofstadt, WZC Hof ter Linden, 9940 Evergem, dr. Joseph De Pourcq, dr. Annick De Mol, WZC Avondvrede, 9000 Gent, dr. Luc Staelens, WZC Brembloem, 9940 Evergem, dr. Luc Uyttendaele, WZC Home Claire, 9000 Gent, dr. Jan Dobbelaere, dr. Renaat Crevits, WZC Sint Coleta, 9000 Gent, dr. André Timmerman, dr. Jan Van Elsen, WZC Sint-Jozef, 9000 Gent, dr. Thierry Goetghebuer, WZC Veilge Have, WZC Zorghave en WZC Woonhave, 9880 Aalter, dr. Raf De Crop, AZ Sint-Lucas & Volkskliniek, 9000 Gent