I. Prologue
C’est l’arrêté royal (AR) du 24 avril 1974 qui marque les débuts officiels de l’hygiène hospitalière en Belgique. En effet, l’AR obligeait tous les hôpitaux à mettre en place un comité d’hygiène hospitalière (CHH) et à tenir un registre dans lequel étaient consignées les mesures prises par le comité (arrêté royal du 24 avril 1974 complétant l’arrêté royal du 23 octobre 1964 portant la fixation des normes auxquelles les hôpitaux et leurs services doivent répondre).
Lors de la mise en service technique et médicale de l’hôpital académique d’Anvers (aujourd’hui hôpital universitaire d’Anvers [UZA]) en 1979, un « comité de lutte contre les infections » fut immédiatement créé.
Dès la première réunion du comité d’hygiène hospitalière en 1979, le chef du laboratoire de microbiologie de l’époque avait souligné l’importance du rôle que pouvait jouer la désignation d’un(e) « infirmier(ère) hygiéniste ». Toutefois, ce type de désignation n’était pas encore possible à l’époque.
Il fallut attendre encore 10 ans avant qu’un premier infirmier hygiéniste hospitalier soit nommé à l’UZA, en même temps qu’un médecin hygiéniste hospitalier. À l’origine de cette décision, figure l’AR du 7 novembre 1988, qui prévoyait le recours à ces fonctions dans les hôpitaux afin de promouvoir l’hygiène.
II. Premiers pas comme infirmier hygiéniste hospitalier
Fort de mon expertise en matière de VIH et de SIDA, entre autre, je fus nommé infirmier hygiéniste hospitalier (IHH) par le comité de direction de l’UZA le 1er janvier 1989. Mon expérience des questions liées au VIH remonte au début des années 1980 ; j’étais alors infirmier à l’Institut de Médecine Tropicale (IMT) depuis 1979. Le transfert des activités d’hospitalisation de la « Clinique Léopold II » de l’IMT à l’UZA (impliquant le transfert des patients et du personnel) en 1987 avait engendré une augmentation du nombre de patients « séropositifs » à l’UZA, et par la même occasion un grand malaise au sein du personnel de l’UZA. C’est ainsi que certains médecins avaient suggéré (heureusement en vain) que ces patients portent un bracelet de couleur afin d’être facilement identifiables lors d’un examen médico-technique. Ce n’est pas pour rien que ma première présentation à l’UZA allait traiter du SIDA(1,2,3,4,5).
Avec pour seules armes un stylo à bille, un sous-main et une pile de rapports du CHH, ma première tâche consista à mettre au point la procédure « Nettoyage, désinfection et stérilisation ». Un PC partagé, qu’il fallait encore démarrer à l’aide d’une disquette et qui ne disposait que d’un programme de traitement de texte, remplaçait partiellement la bonne vieille machine à écrire. Après quelques mois, je reçus le renfort d’une collègue, ce qui donna un coup d’accélérateur au développement des procédures. Plusieurs procédures virent le jour au début des années 1990, comme la prévention des accidents par piqûre d’aiguille, les procédures d’isolement, les mesures à prendre lors de la préparation et de l’administration de cytostatiques, les procédures de zonage, etc. Alors que ma collègue travaillait plutôt au niveau des procédures, j’étais intégré au laboratoire de microbiologie où je me concentrais sur l’enregistrement des infections nosocomiales sous la supervision du chef du laboratoire de microbiologie. Concrètement, cela signifiait que les hygiénistes hospitaliers étaient répartis sur trois sites différents de l’hôpital.
A la fin de l’année 1989, j’ai demandé au président du CHH d’envisager les aménagements nécessaires pour optimiser le fonctionnement de l’hygiène hospitalière, et notamment la mise à disposition d’un espace de travail commun pour les hygiénistes hospitaliers avec le mobilier nécessaire ainsi que des abonnements à la littérature professionnelle. Sur la liste de souhaits figurait également un ordinateur doté d’une capacité suffisante pour le traitement de texte et l’enregistrement des infections/colonisations, et qui devait également être connecté à l’ordinateur central afin de faciliter l’obtention des données de laboratoire. Ce n’est qu’en 1992 que l’enregistrement des infections/colonisations allait connaître un coup d’accélérateur grâce au chef du laboratoire de microbiologie qui avait souligné, entre autre le caractère indispensable d’installations informatiques automatisées pour assurer correctement la fonction d’hygiène hospitalière. De même, l’accès aux données non microbiologiques des patients (tels les résultats d’analyses hématologiques), qui jusqu’alors nécessitait toujours l’autorisation du médecin-chef, allait être progressivement facilitée par la suppression des règles bureaucratiques (pour utiliser les termes du chef du laboratoire de microbiologie en 1992).
Afin de répondre aux exigences légales, l’équipe d’hygiène hospitalière suivit la formation d’hygiène hospitalière à l’UIA (aujourd’hui UA) de 1989 à 1991. La formation était alors commune pour les infirmiers(ères), les médecins et les pharmaciens(ennes).
III. Les surveillances
Les premières années au laboratoire de microbiologie furent essentiellement consacrées aux activités d’enregistrement (aussi optimal que possible) des infections/colonisations nosocomiales. Par ailleurs, la surveillance et l’enregistrement d’un certain nombre de germes spécifiques furent également initiés à cette époque. Celle-ci portait sur des bactéries multi-résistantes (tel le SARM qui constituait alors l’exemple type de la bactérie hospitalière multi-résistante) ou sur des espèces bactériennes reconnues pour leur propension à occasionner des épidémies nosocomiales (et ce indépendamment des critères de multi-résistance en vigueur à l’époque). Les bactéries concernées étaient les suivantes : Pseudomonas aeruginosa, Serratia marcescens, SARM, Xanthomonas maltophilia (aujourd’hui Stenotrophomonas maltophilia) et les bactéries du genre Acinetobacter. La collaboration soutenue avec le service informatique (ICT) déterminera en grande partie le fonctionnement de l’hygiène hospitalière dans les années ultérieures (voir plus loin).
Au début, la détection de nouveaux cas d’infections/colonisations occasionnées par ces microorganismes devait s’effectuer manuellement et quotidiennement, germe par germe, via le programme informatique du laboratoire et sur un PC de laboratoire (dont il fallait attendre la disponibilité). Comme on ne disposait pas encore d’un PC avec un programme graphique, on recourait à du papier quadrillé pour présenter visuellement les données (figures 1, 2 et 3).
Figure 1
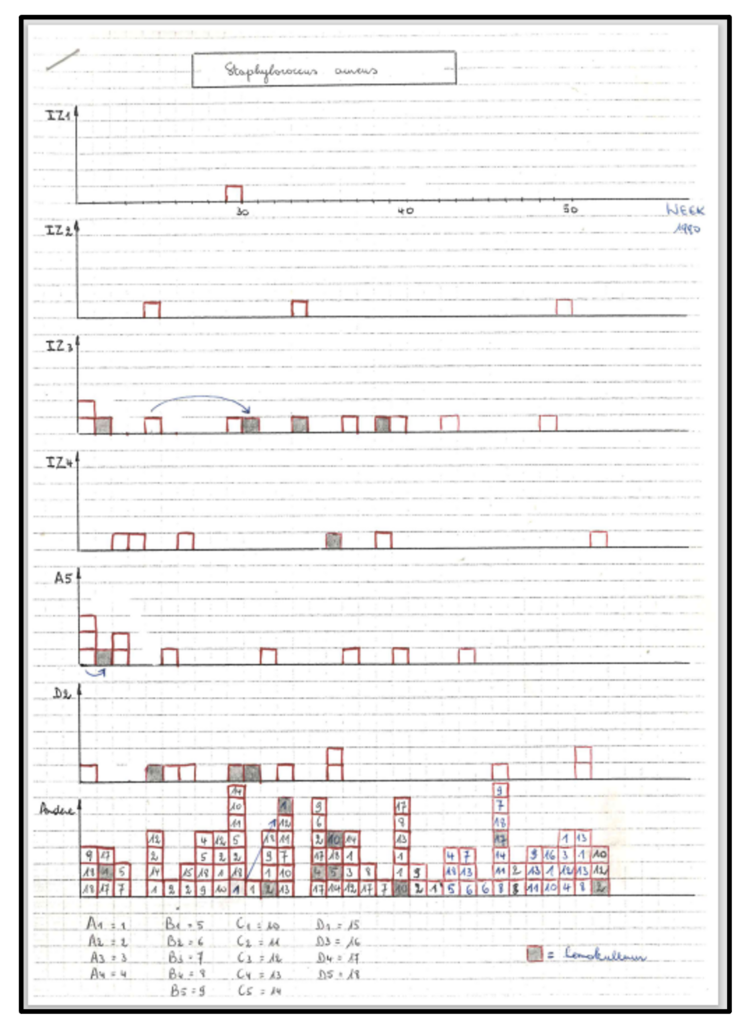
Figure 2
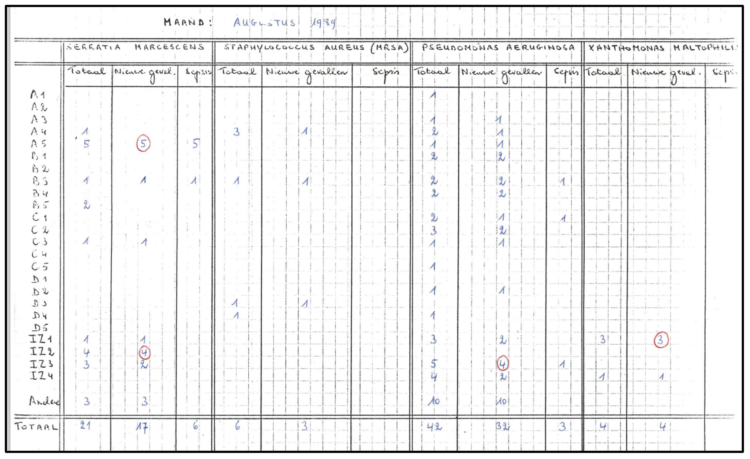
Figure 3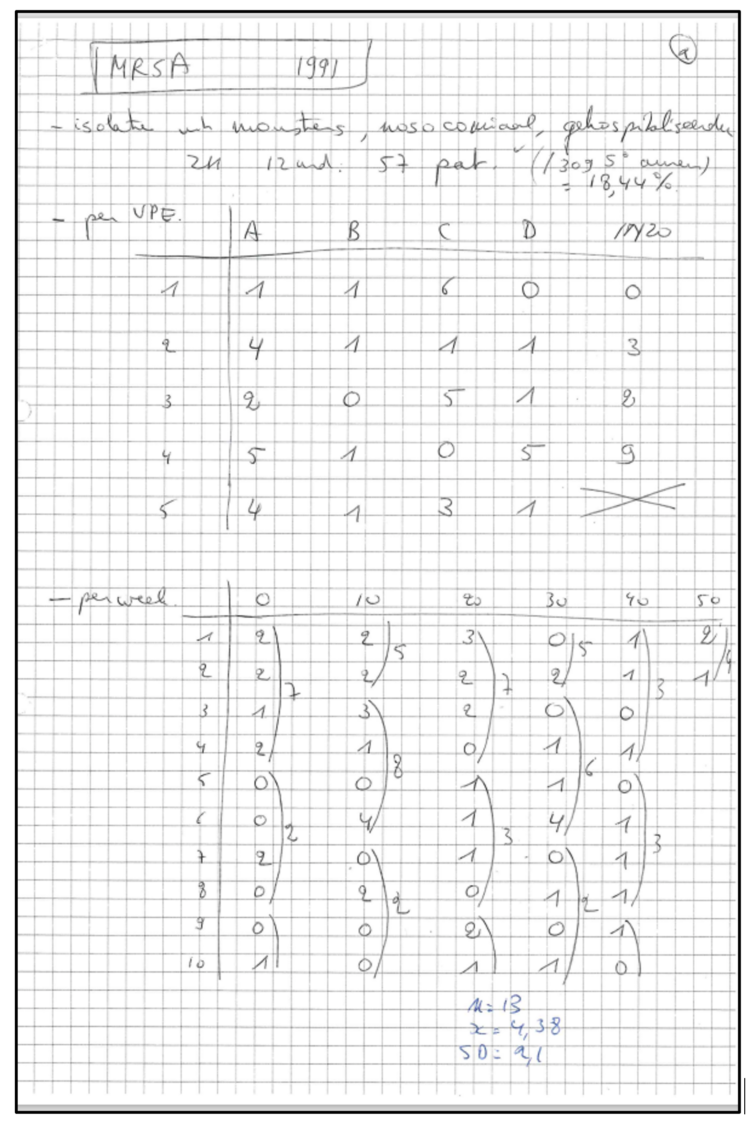
Nous utilisions également des fiches, rangées dans un bac à fiches métallique (de type Valrex®) fixé au mur (figure 4), avec une couleur de fiche spécifique pour chaque microorganisme. Même après l’arrivée d’un programme graphique, les données restèrent compliquées à présenter.
Figure 4

La collaboration avec le médecin hygiéniste hospitalier permit d’étendre le domaine d’enregistrements et de surveillance notamment au domaine des infections du site opératoire (ISO). Cette activité allait nous permettre de montrer dès 1991 que les taux d’incidence des ISO variaient de manière très significative selon qu’ils étaient établis au moment de la sortie d’hôpital ou plus tardivement grâce à la mise en place d’un follow-up après la sortie de l’hôpital (6,7). Mais l’application de nouvelles mesures préventives comme la dépilation préopératoire à la tondeuse, la douche préopératoire du patient et l’application de nouvelles techniques en chirurgie cardiaque eurent également un impact favorable sur l’incidence des ISO (voir plus loin).
Au fil des ans, la surveillance des infections allait s’affiner en se concentrant principalement sur les micro-organismes multi-résistants (MDRO) et en appliquant pour ceux-ci les critères de multi-résistance définis par Sciensano pour les surveillances nationales.
En collaboration avec le laboratoire de microbiologie, un protocole fut adopté pour signaler le plus précocement possible aux hygiénistes hospitaliers, sur papier, les MDRO importants et pouvoir ainsi instaurer très rapidement les mesures d’isolement et et/de décolonisation des patients. Il n’était pas rare que les techniciens de laboratoire glissent un papier de signalement sous la porte de notre bureau le soir, pour que nous puissions nous mettre immédiatement au travail le lendemain matin (figure 5).
Cette méthode allait par la suite être remplacée par l’envoi d’un e-mail aux hygiénistes hospitaliers et faire partie intégrante des nombreuses « étapes » d’analyse des échantillons de laboratoire.
Figure 5

Très vite, l’ICT put produire quotidiennement un listing imprimé, que nous devions aller chercher nous-mêmes au service ICT. Il en résultait chaque année des classeurs de 10 cm d’épaisseur destinés à conserver la chaîne de papier reprenant les résultats de laboratoire (figure 6).
Figure 6.

Les tâches des hygiénistes hospitaliers n’étant pas clairement définies au départ, les activités de surveillance relevaient strictement du domaine du service de prévention ou du laboratoire de microbiologie. Concrètement, il s’agissait d’enregistrer les contacts accidentels avec du sang (« accidents par piqûre d’aiguille »), d’établir des rapports dans le cadre des laboratoires vigies et de documenter la sensibilité réduite (« résistance aux antibiotiques ») des micro-organismes isolés à l’UZA.
Ce n’est qu’en 2022 que ces enregistrements furent confiés respectivement au service de prévention et aux biologistes cliniques du laboratoire de microbiologie. Ces enregistrements ont contribué à l’établissement d’une méthodologie standardisée pour la définition des critères de résistance aux antibiotiques des différentes bactéries. Instaurée dès 1994, cette méthodologie sera utilisée ensuite chaque année pour établir les taux de résistance aux antibiotiques (8). Le logiciel utilisé à cet effet était dBase III au début, puis dBase IV pour finalement passer à Access. Avant de pouvoir transmettre automatiquement les données microbiologiques avec les antibiogrammes, on recourait encore aux disquettes, qui étaient fournies mensuellement à l’équipe opérationnelle en hygiène hospitalière (EOHH) par le laboratoire de microbiologie.
L’enregistrement des contacts accidentels avec du sang, a permis également de montrer que l’introduction de matériel de sécurité (comme les aiguilles à ailettes et les chambres à cathéter implantables) avait pu réduire le nombre d’accidents par piqûre d’aiguille (9,10). En parallèle, des mesures furent également prises pour réduire le nombre d’accidents par piqûre avec les stylos à insuline et les glucomètres (11,12,13). Par ailleurs, nous avons pu grâce à cette activité de surveillance documenter sur plusieurs années le nombre de contacts sanguins accidentels avec des infections transmissibles par le sang (VIH, VHC et VHB), sans qu’aucune séroconversion ne soit observée au sein du personnel (14,15).
Le renforcement de l’équipe opérationnelle d’hygiène hospitalière (EOHH) en 2003 par un IHH maîtrisant le programme Access de MS Office déboucha rapidement sur un système d’enregistrement « maison ». Le programme permettait d’avoir un aperçu sur un seul écran, pour chaque patient, de son historique d’hospitalisation, des statuts d’isolement, des MDRO et des traitements de décolonisations réalisés pour le SARM. Ce système était toujours utilisé en 2022, car son intégration dans le dossier patient informatisé (DPI) n’est prévue qu’à un stade ultérieur.
Navigator et le décret qualité flamand
Le décret flamand sur la qualité de 1997 prévoyait certains thèmes obligatoires, parmi lesquels celui de la surveillance et de l’enregistrement des infections nosocomiales. Dans ce cadre nous avions décidé de retenir les ISO, la septicémie primaire nosocomiale (SEP) et la pneumopathie acquise sous ventilation mécanique (PAVM). Pour ces surveillances, il était recommandé d’utiliser les systèmes d’enregistrement existants de l’Institut scientifique de santé publique de l’époque. Fin de l’année 1998, l’EOHH fit part à l’administration de la santé de certaines préoccupations critiques quant à la faisabilité de l’enregistrement des ISO. La charge de travail intense inhérente à cette surveillance entraînant par manque de ressources la suppression progressive d’autres activités de surveillance existantes, comme l’enregistrement des MDRO. La circulaire suivante de l’administration des soins de santé, en 1999, indiqua alors que, contrairement aux autres thèmes obligatoires, il ne fallait pas encore mesurer d’indicateur pour le thème des infections du site opératoire en 1999. La mesure des indicateurs d’ISO commencera en janvier 2000. À cette fin, l’EOHH prit les contacts nécessaires avec différents services fin 1999 afin de collecter de la manière la plus efficace possible les données relatives aux ISO en orthopédie (bloc opératoire, service informatique, toutes les unités de soins avec patients orthopédiques et consultation).
En 2003, un nouveau décret flamand sur la qualité vit le jour. Il rassemblait les différents décrets relatifs à la qualité des secteurs des soins de santé et du bien-être ; il entra en vigueur en 2004. A partir de 2004, il ne fut dès lors plus nécessaire de procéder aux enregistrements prévus par le précédent décret qualité de 1997. Toutefois, chaque hôpital devait procéder à une évaluation de la politique menée entre 1997 et 2004 puis, en 2004, réfléchir à la politique de qualité à mener en 2005.
En 2004, l’UZA décida de poursuivre les surveillances des ISO et des infections en USI.
Comme des données étaient également recueillies par « Navigator » (figure 7) après 2004 pour le domaine « infections » (SARM, utilisation d’alcool pour les mains), ces indicateurs purent également être utilisés pour le décret qualité. Navigator était un système d’indicateurs du Centrum voor Ziekenhuis– en Verplegingswetenschap visant à assurer le suivi et l’amélioration continus de la qualité clinique et organisationnelle des soins.
Figure 7

Études de prévalence ponctuelle (EPP)
Une première étude de prévalence ponctuelle des infections des voies urinaires avait été menée en 1991. Elle fut réitérée en 2004 et mit en évidence l’augmentation de la prévalence comparativement à 1991. Ce fut l’occasion de rappeler aux infirmiers(ères) l’importance d’appliquer le système de drainage urinaire en circuit fermé (voir plus loin).
À l’initiative du chef du laboratoire de microbiologie, une étude de prévalence ponctuelle avait été réalisée en 1996, en collaboration avec l’EOHH, au cours de laquelle tous les patients avaient subi un dépistage des ERV un jour donné. Au total, 335 patients avaient été dépistés. Parmi les patients hospitalisés, 11,8 % s’étaient révélés positifs à l’ERV, contre 24,1 % chez les patients en dialyse. Même si la prévalence était plus élevée chez les patients dialysés, la différence avec les patients hospitalisés n’était pas significative. L’étude avait révélé également l’influence du type d’échantillonnage : l’ERV ayant été isolé dans 16,9 % des échantillons de selles, contre 5,7 % seulement à partir d’écouvillonnage rectal. Le pourcentage élevé de patients positifs à l’ERV pouvait éventuellement s’expliquer par la technique d’enrichissement utilisée dans le laboratoire (16).
En juin 2010, nous avons participé à une étude pilote d’une enquête européenne de prévalence ponctuelle sur les infections associées aux soins de santé et l’utilisation des antibiotiques dans les hôpitaux de soins aigus (Point Prevalence Survey on Health Care Associated infections and Antibiotic Use). Cette étude initiée par le Centre européen de prévention et de contrôle des maladies (ECDC) avait été organisée en Belgique par la Commission belge de coordination de la politique antibiotique (BAPCOC) avec le soutien scientifique de l’ISP. Cette étude pilote a révélé notamment que la proportion de patients atteints d’une infection nosocomiale à l’USI était plus élevée à l’UZA que dans d’autres hôpitaux belges et européens participants. Même constat pour la proportion de patients sous antibiothérapie en USI. La pneumonie était enregistrée comme principal diagnostic d’infection nosocomiale à l’UZA (essentiellement en USI). En 2011, nous avons également participé sur base volontaire au volet belge de cette EPP, qui était alors destinée à tous les hôpitaux de Belgique.
Surveillances des ICC et IUAC
Dans le cadre de l’accréditation « Magnet®-hospital » (voir plus loin), il fut décidé en 2013 de surveiller les infections urinaires associées aux cathéters (IUAC) et les infections sanguines associées aux cathéters centraux (ICC) en tant que « indicateurs de qualité des soins infirmiers ».
Dans le contexte de cette surveillance, il fallait disposer, pour chaque patient, des données relatives au type de cathéter et connaître la durée de sa mise en place. À partir de la mi-2013, l’ICT parvint à fournir mensuellement à l’EOHH un tableau Excel contenant ces données ; nous pûmes ainsi les relier aux données administratives et microbiologiques des patients dans la base de données du service d’hygiène hospitalière. Les définitions du CDC pour ces infections furent ensuite appliquées aux patients sélectionnés afin de déterminer leur incidence par 1000 jours-cathéters pour chaque service. Cela permit de transmettre aux unités de soins infirmiers les incidences mensuelles d’ICC et IUAC via le Business Intelligence Center (BI Center) (voir plus loin) avec représentation graphique et numérique des résultats. Enfin, les unités de soins infirmiers devaient prendre des mesures d’amélioration lorsque l’incidence dépassait la valeur cible.
L’année 2017 fut marquée par le développement d’un ensemble de processus de soins pour lutter contre les IUAC et l’introduction du principe « HOUDINI », un outil permettant de déterminer si la présence d’une sonde vésicale est toujours indiquée.
En 2019, des mesures furent prises à l’échelle de l’hôpital pour fixer correctement les sondes de Foley (figure 8). Le dispositif de fixation Grip-lok® devint alors le système de fixation standard. En parallèle, les infirmiers(ères) de référence effectuaient des audits pour vérifier si les sondes Foley étaient fixées correctement.
Figure 8

En ce qui concerne les ICC, un ensemble de bonnes pratiques pour la pose de cathéters fut également mis au point et, comme pour les cathéters vésicaux, un système uniforme de fixation des cathéters fut adopté, étant donné que différents types étaient – parfois mal – utilisés. En outre, pour réduire le nombre de voies veineuses centrales, les anesthésistes allaient davantage opter pour la mise en place de cathéters veineux périphériques longs (midline).
IV. Les surveillances organisées par Sciensano
a) WHOCARE
Comme évoqué plus haut, le rôle de l’ICT est devenu de plus en plus important au fil des ans. En plus des surveillances précédemment évoquées, celles organisées par l’Institut d’Hygiène et d’Épidémiologie (IHE) de l’époque (devenu ensuite l’Institut Scientifique de Santé Publique [ISP], puis Sciensano) nécessiteront également un des supports informatiques spécifiques. C’est dans ce contexte qu’en 1992, l’IHE nous proposa un programme intitulé « WHOCARE », livré sur une disquette et nécessitant un PC avec 505 RAM et 6 MB d’espace libre (!) fonctionnant sur DOS. Le programme était conçu pour la surveillance des ISO et des SEP (Figures 9 et 10). Il fut utilisé jusqu’en 1999.
Figure 9

Figure 10

b) NSIH (Surveillance nationale des infections nosocomiales)
A partir de l’an 2000, nous avons participé aux surveillances des SEP et ISO à l’aide de programmes développés par l’ISP. Ceux-ci utilisaient le système d’exploitation Windows (NSIHwin). Cependant, les données de l’an 2000 étaient encore exportées via une disquette envoyée à l’ISP par la poste (Figure 11). Par la suite, il fut également possible d’envoyer les données exportées par courrier électronique.
Figure 11

Entre 1994 et 2007, la surveillance du SARM nécessitait encore des formulaires d’enregistrement papier, qu’il fallait envoyer à l’ISP par la poste. En 2006, l’ISP commença à travailler sur une version Internet pour la participation à la surveillance du SARM, qui avait pour avantage d’autoriser une transmission en ligne des données et des rapports informatisés (NSIHweb). Cet enregistrement en ligne allait ensuite devenir également possible pour les SEP, l’hygiène des mains, Clostridium difficile (CDIF) et les antibiotiques.
En 2012, le protocole SEP fut modifié (principalement en ce qui concerne les contaminants cutanés), empêchant malheureusement la comparaison des données avec les périodes antérieures à 2012.
L’enregistrement des infections dans les unités de soins intensifs (USI) selon le protocole HELICS (SEP, PNEU, IVU) était effectué par les médecins. Entre 1997 et 2000, la version obsolète du programme sous DOS (SINERGIZ) était encore utilisée à cette fin. Les formulaires d’enregistrement papier étaient collectés chaque semaine par l’EOHH, qui saisissait ensuite les données dans le programme d’enregistrement. On passa ensuite à « Helics.Win.Net » (Access). En 2001, c’est le secrétariat de l’USI, qui fut chargé de l’encodage des données avec comme corollaire un accroissement important de sa charge de travail. La participation à cette surveillance fut finalement interrompue, également en partie à cause du manque de convivialité du logiciel de l’ISP. Dans le cadre de l’accréditation JCI (voir plus loin), la surveillance des pneumonies acquises sous ventilation mécanique (PAVM) allait quant à elle être poursuivie à l’USI.
À partir de 2011, la surveillance des entérobactéries productrices de carbapénémases (EPC) vint également s’ajouter à la liste des surveillances. Cependant, la transmission des données était laborieuse : il fallait d’abord télécharger un document spécifique via le site de l’ISP, puis l’envoyer par courrier postal. Par ailleurs, les données de surveillance étaient également envoyées par la poste pour d’autres MDRO, avant de pouvoir être envoyées par courrier électronique. A partir de 2016, la surveillance de l’EPC ne se fit plus par le biais d’un formulaire de déclaration, mais fut intégrée à la surveillance des autres bactéries résistantes aux antibiotiques.
Nouveau changement en 2017 : la surveillance allait s’effectuer via HD4DP (Healthdata for data providers) pour les SEP et CDIF ; par après, la saisie d’indicateurs de qualité fut également possible. Pour traiter nos propres résultats, nous recourions/recourons au téléchargement dans Healthdata d’une part et aux analyses des données introduites via healthstat.be d’autre part.
Initialement, la participation aux différentes surveillances susmentionnées était facultative. La surveillance du SARM fut ensuite imposée par AR en 2006. L’AR de 2007 rendit obligatoire l’enregistrement du CDIF en plus de l’enregistrement du SARM. Une autre condition imposée par cet AR de 2007 était la participation additionnelle à au moins un protocole au choix parmi la liste des surveillances facultatives suivantes : pneumonies et bactériémies dans les unités de soins intensifs, septicémies à l’échelle de l’hôpital, infections du site opératoire et bactéries à Gram-négatif multi-résistantes (MDRO). En 2015, cette obligation fut mise à jour : enregistrement obligatoire du SARM et du SEP, des MDRO à Gram-négatif, indicateurs de qualité et choix d’un protocole supplémentaire : CDIF, ERV, ISO, pneumonies et bactériémies dans les unités de soins intensifs.
c) Epinet™
En plus des surveillances des infections associées aux soins, nous avions également participé en 2003 à l’enregistrement des accidents exposant au sang. Nous utilisions à cet effet un programme proposé par l’ISP, une version light de l’Epinet™ américain. Bien que cette participation fût facultative, le président du CHH encouragea vivement à prendre part au projet pilote en 2003. Nous allions par ailleurs également participer à une étude de sous-signalement en 2006-2007 qui montra que (au niveau national) plus de 45 % du personnel ne signalait pas les accidents par piqûre d’aiguille. Cependant, la surveillance nationale des accidents exposant au sang fut interrompue par l’ISP en 2008, de sorte qu’i n’y a pas de données plus récentes pour la Belgique. Pour ce qui concerne plus spécifiquement les accidents exposant au sang au bloc opératoire, nous avons publié dans Noso-info en 2006, en collaboration avec l’ISP, un article traitant des données de surveillance nationales ainsi que les mesures de prévention(17).
d) EARS-BE/EARSnet
A partir de 2009, nous avons participé à la collecte de données pour la Belgique (EARS-BE) dans le cadre du Réseau européen de surveillance de la résistance aux antimicrobiens (EARSnet). Il s’agissait de recueillir les données de laboratoire sur la résistance aux antibiotiques pour une série de bactéries, dont Klebsiella pneumoniae, Escherichia coli, Staphylococcus aureus, Pseudomonas aeruginosa, Enterococcus faecium, Enterococcus faecalis et Streptococcus pneumoniae. Cette surveillance fut interrompue en 2021, en partie à cause de la crise du coronavirus, la charge de travail étant trop importante.
V. Neo-Kiss
Pour la surveillance à l’Unité de soins intensifs néonataux (USIN), le service avait opté pour « Neo-Kiss ». Il s’agit d’un système de surveillance des infections nosocomiales chez les nouveau-nés prématurés de moins de 1 500 g à la naissance (VLBWI = very low birth weight infants), développé en Allemagne (KISS = Krankenhaus-Infektions-Surveillance-System).
La participation à cette surveillance permet de se comparer à la base de données allemande qui contient les données de plus de 200 USIN. En 2012, 11 des 19 USIN belges y avaient pris part. Dans le cadre de cette surveillance, les infections nosocomiales associées aux cathéters centraux et périphériques et à la ventilation invasive (intubation) et non invasive (nasale, sans intubation) étaient enregistrées.
Les données relatives aux SEP étaient transmises par l’EOHH au médecin responsable de l’USIN une fois par mois et étaient également utilisées par l’EOHH pour la surveillance nationale (NSIH), moyennant adaptation au protocole de la NSIH (18).
VI. Surveillance de l’hygiène des mains
a) Campagnes nationales d’hygiène des mains
À partir de 2005, l’EOHH répondit systématiquement de manière positive aux invitations à participer aux campagnes nationales d’hygiène des mains. Des données y étaient recueillies sur l’utilisation de l’alcool pour les mains, les exigences de base en matière d’hygiène des mains et le respect des indications en matière d’hygiène des mains. Les données étaient saisies en ligne dans le programme de l’ISP (NSIHWeb2), autorisant ainsi le traitement des données des hôpitaux participants. L’année 2022 allait être marquée par la migration de NSIHweb2 vers Healthdata. En outre, au cours des dernières années, des outils de promotion de l’hygiène des mains furent également proposés par les autorités dans le cadre des campagnes, comme les badges « Vous êtes entre de bonnes mains », un module d’apprentissage en ligne, une lampe UV pour vérifier la technique de lavage des mains, etc. Enfin, des campagnes thématiques furent également menées, comme la responsabilisation du patient ou la prévention des septicémies associées aux cathéters.
b) Manifeste « mains propres » (« Manifest schone handen »)
Des observations menées à la mi-2005 dans le cadre de la campagne nationale d’hygiène des mains avait permis de constater que seulement 35 % des infirmiers(ères) respectaient pleinement le principe de base d’absence de port de bijoux. C’est pourquoi une nouvelle action d’amélioration de l’hygiène des mains fut lancée à l’automne 2005 à l’initiative de la direction des soins aux patients et de l’EOHH. Tous les collaborateurs du département infirmier furent invités à signer un « manifeste » (figure 12). L’objectif était de les impliquer davantage dans la problématique de l’hygiène des mains. En outre, la mise à disposition des solutions hydro-alcooliques pour les mains s’est accrue et une rétro-information a été fournie aux unités de soins concernant consommation d’alcool pour les mains, de même que concernant l’observation des principes de base d’hygiène des mains. Suite à cette
action corrective, le médecin-chef a adressé une lettre à tous les médecins indiquant que les directives destinées au département infirmier s’appliquaient également aux médecins.
La combinaison de la campagne nationale d’hygiène des mains et d’une campagne interne visant à accroître le respect de l’hygiène des mains a entraîné une augmentation de la consommation d’alcool pour les mains ainsi qu’une amélioration du respect des principes de base. Bien qu’aucun lien de causalité avec la campagne n‘ait pu être établi, une diminution de l’incidence nosocomiale du SARM a été observée. ((PDF) Manifest « schone handen » dans (researchgate.net)).
Figure 12 : Manifeste « mains propres » à l’UZA

c) Responsabilisation du patient
Avant même la campagne thématique sur la responsabilisation du patient (voir plus haut), nous avions déjà mené des recherches sur ce thème en 2014, en interrogeant directement les patients. Il en était ressorti, entre autres, qu’environ la moitié des personnes interrogées estimaient que les patients devaient être impliqués dans la sensibilisation des professionnels de la santé à l’hygiène des mains. Toutefois, seulement un quart des répondants ont indiqué qu’ils oseraient interpeler directement un médecin si ce dernier ne pratiquait pas l’hygiène des mains. Les autres professionnels de la santé ne seraient également abordés que par un tiers des répondants le cas échéant (19). Par ailleurs, il ressortait de l’interrogatoire des patients à propos de la brochure d’information sur l’hygiène des mains qui leur était destinée que celle-ci était largement méconnue (20).
d) SATURN (Impact of Specific Antibiotic Therapies on the prevalence of hUman host ResistaNt bacteria)
C’est le chef de l’USI qui prit l’initiative de participer au projet européen SATURN en 2011. L’objectif était de déterminer l’effet de deux stratégies antibiotiques différentes (cycle et mélange) sur la prévalence des bactéries résistantes dans 10 USI. Ce projet nécessitait également la collecte de données relatives à l’hygiène des mains dans les USI. L’EOHH a fourni les données nécessaires pour l’UZA.
e) VIP2 (Vlaams Indicatorenproject voor Patiënten en Professionals – Projet flamand d’indicateurs pour les patients et les professionnels)
Enfin, il y eut également le projet VIP², qui mesure la qualité des soins dans les hôpitaux généraux flamands. Cependant, la participation à ce projet impliquait un investissement de temps important (4 jours), car il fallait, entre autres, observer les exigences de base en matière d’hygiène des mains dans d’autres hôpitaux et saisir les résultats dans NSIHweb. Depuis et en partie à cause de la crise du coronavirus, la participation à ce projet a été interrompue.
f) Scanner d’hygiène des mains Semmelweis
Le scanner d’hygiène des mains Semmelweis (figure 13) est un dispositif mobile permettant de former de manière interactive à l’hygiène des mains. En quelques secondes, le personnel soignant peut voir si les mains sont correctement désinfectées et où se trouvent exactement les zones mal désinfectées sur les mains.
En 2017, l’EOHH proposa d’acheter ce scanner d’hygiène des mains.
En collaboration avec l’ICT, une connexion en temps réel aux données du personnel fut établie pour avoir accès à leurs résultats. Le scanner a déjà été installé dans plusieurs services au cours des dernières années, donnant au personnel la possibilité de s’entraîner à l’hygiène des mains pendant plusieurs jours.
Figure 13

VII. ICT et communication des règles d’hygiène
Diverses actions de communication des règles et principes d’hygiène ont été menées dès 2005, notamment au travers des campagnes nationales d’hygiène des mains. À cet effet, des écrans numériques ont été installés à différents endroits stratégiques, par exemple, dans le hall d’entrée ou dans les services, afin de sensibiliser les visiteurs et les patients à l’importance de l’hygiène des mains.
Ce mode de communication s’est également avéré utile lors de la crise du coronavirus pour communiquer rapidement les mesures nécessaires et les ajuster si nécessaire.
La communication des résultats de la surveillance aux employés de l’UZA fait également appel à l’équipe ICT. Depuis plusieurs années, toute une série d’indicateurs, notamment ceux relatifs à l’hygiène hospitalière, est consultable sur n’importe quel PC via ce que l’on appelle un site de centre d’aide (Business Intelligence Center, BI Center) (figure 14). Il s’agit notamment des résultats mensuels d’indicateurs par service et pour l’ensemble de l’hôpital en matière d’IUAC, d’ICC, d’ISO et du respect des règles de l’hygiène des mains.
Figure 14

VIII. ICT et contrôle des infections nosocomiales
Jusqu’en 2001 inclus, on recourait à des autocollants SARM (figure 15), que l’on collait dans le dossier du patient afin que les mesures nécessaires puissent être prises dès la réadmission. Toutefois, cette pratique s’est avérée inopérante dans la pratique. De plus, les autocollants étaient parfois collés à l’extérieur du dossier patient, encore en papier à l’époque, ce qui pouvait compromettre la confidentialité des données médicales.
Figure 15

Ainsi, en 2002, il fut convenu avec le service informatique et le service d’administration des patients de créer un système de signalement automatique.
Concrètement, cela signifiait que l’EOHH communiquait par e-mail chaque nouveau patient SARM à l’administration patient, qui complétait la liste des SARM. Cette liste de noms était associée à un message libellé de manière neutre afin de ne pas donner lieu à une quelconque stigmatisation. Le message qui apparaissait à l’écran de la personne qui inscrivait le patient était le suivant : « Fait l’objet d’un suivi hygiène hospitalière. Prévenir les hygiénistes hospitaliers (ou le directeur des soins aux patients de garde en dehors des heures) ».
Le message « Fait l’objet d’un suivi hygiène hospitalière » signifiait que le patient concerné devait être admis dans une chambre individuelle pour des raisons médicales et que le dépistage devait être effectué le jour même (20).
En dehors des heures de bureau, la personne qui inscrivait le patient devait prévenir le directeur soins aux patients.
Toutefois, ce mode de fonctionnement a généré de nombreux appels téléphoniques émanant des consultations et de services souhaitant obtenir plus d’informations sur les mesures à prendre. En outre, vu la nécessité de plusieurs actions manuelles comme le remplissage de la liste des noms par l’administration patients, cette méthode de travail a perdu en précision au fil du temps.
Après plusieurs années de fonctionnement, l’EOHH a développé un nouveau système d’alerte sur la base de codes saisis dans le système d’information hospitalier (SIH). Cela signifiait qu’à partir de ce moment-là, en plus du SARM, des alertes pouvaient également être introduites pour d’autres MDRO, notamment ERV et EPC et, depuis 2020, pour les patients positifs au COVID. Ce système offrait également l’avantage de pouvoir associer chaque code de manière spécifique avec les mesures à instaurer lors de la consultation ou de l’admission, et aussi de pouvoir les imprimer. La visualisation du statut des patients a été rendue possible grâce à des icônes spécifiques affichées dans le dossier électronique et sur les synthèses numériques des patients (Figure 16). Ces différentes mesures ont contribué à réduire de manière drastique le nombre d’appels téléphoniques par rapport au système d’alerte initial.
Une adaptation des critères de dépistage du portage de u SARM chez les patients à l’admission a été effectuée en 2014. Ainsi, si un patient était vétérinaire ou éleveur de bétail ou s’il avait séjourné dans un autre établissement de santé au cours des six derniers mois, une fenêtre contextuelle apparaissait dans le dossier médical électronique afin de le dépister pour le SARM. Plus tard, le dépistage des EPC allait y être ajouté. Avec l’introduction de la mise à jour du dossier patient informatisé (DPI) en 2021, le pop-up fut remplacé par un ordre automatique de dépistage du patient.
Figure 16

IX. L’impact du bug de l’an 2000
À l’approche de l’an 2000, les rumeurs concernant l’imminence du bug de l’an 2000 s’intensifièrent. À en croire les catastrophistes, les ordinateurs et les appareils assistés par ordinateur allaient défaillir. Le nœud du problème était que les dates ne s’écrivaient qu’avec deux chiffres dans les programmes (99 pour 1999, par exemple), et l’année 2000 aurait été interprétée comme 1900. Dès 1998, un groupe de projet fut constitué à l’UZA pour se pencher sur cette problématique. Le fonctionnement de l’hygiène hospitalière pouvait également être affecté, étant donné qu’un grand nombre de données de surveillance étaient introduites dans un programme Microsoft Access, dont les versions n’étaient apparemment pas toutes compatibles avec l’an 2000. Il fallut donc passer à d’autres versions et renseigner les années en 4 chiffres.
X. Endémies, foyers (épidémies) et pandémies
Au cours des 30 dernières années, l’UZA, comme d’autres hôpitaux, n’a pas été épargné par les épidémies majeures ou mineures (infections avec flambée épidémique). Cependant, il n’a pas toujours été possible d’en identifier les causes, ce qui entraînait parfois de grandes frustrations. Dans un certain nombre d’épisodes épidémiques qui sont décrits plus loin, il a été possible d’identifier une cause claire ou probable ou en cas de non-détection de la cause à tout le moins de maitriser le foyer grâce à la mise en œuvre d’une série de mesures.
a) Légionellose
La légionellose était endémique à l’UZA depuis 1988. En 1989, dès le début des activités d’hygiène hospitalière, une incidence accrue de pneumonies à Legionella pneumophila a été constatée. Nous avions rapidement reçu l’instruction d’enregistrer quotidiennement un certain nombre de facteurs de risque possibles pour ces pneumonies chez les patients en USI, mais aucun facteur de risque clair ne put être identifié. Grâce aux liens étroits qui existaient entre l’IMT et le CDC, nous avons pu obtenir la collaboration des épidémiologistes du CDC afin de tenter d’identifier la cause de ces pneumonies. Cela allait donner lieu à une recherche intensive des facteurs de risque, au cours de laquelle le personnel du CDC parcourait méticuleusement, juste avec un crayon et du papier, les piles de dossiers de patients, les microfilms et les radios. Ceci a constitué pour nous une première approche sur la manière dont une investigation épidémiologique était menée, à savoir avec une patience d’ange et de manière très ponctuelle. A l’issu de cette enquête, il s’est finalement avéré que la cause était une température trop basse de l’eau et que la toilette des patients au lavabo constituait un facteur de risque majeur de légionellose pour les patients immunodéprimés ; en revanche, le lavage au lit se révéla être un facteur de protection (22, 23,24,25).
b) Burkholderia cepacia
En 1995, nous avions été alertés par le laboratoire de microbiologie sur la survenue chez plusieurs patients d’hémocultures positives pour Burkholderia cepacia. Tous les patients concernés avaient été admis en cardiologie et avaient subi un cathétérisme cardiaque, laissant suggérer que l’origine de ces cas devait être recherchée au niveau du laboratoire de cathétérisme. Parallèlement parallèle à l’arrêt temporaire des activités dans ce service, une étude épidémiologique fut initiée. Celle-ci permit d’identifier la dilution de la solution d’héparine au service de cardiologie comme un facteur de risque potentiel. L’héparine était en effet diluée avec une solution de glucose à 5 % prélevée dans une poche à perfusion de 1 litre; cette poche à perfusion était conservée à température ambiante toute la journée près d’un évier du poste infirmier. Les analyses microbiologiques pratiquées montrèrent une contamination de la solution de glucose par la même souche de B. cepacia que celle retrouvée dans les hémocultures chez les sept patients. Ces constatations allaient entrainer la tenue d’une nouvelle réunion urgente des infirmiers.ères en chef pour souligner la dangerosité de telles pratiques et la nécessité d’utiliser des solutions stériles unidoses pour préparer les dilutions d’héparine intraveineuses. Cette épidémie a également mis en évidence l’importance du hasard dans la découverte de la source de contamination; En effet, la poche de perfusion incriminée dans le service avait déjà été éliminée à la poubelle, mais elle put être récupérée par chance juste avant la collecte des déchets et contenait encore suffisamment de liquide pour une analyse microbiologique (26).
c) Toxi-infection alimentaire collective dans un service infirmier
En octobre 1999, l’infirmière en chef d’un service de soins infirmiers signala à l’EOHH la survenue de plusieurs cas de gastro-entérite au sein du personnel. L’infection était apparemment survenue après consommation d’un tiramisu, que l’une des infirmières avait préparé avec des œufs crus. Au total, 10 membres du personnel et huit proches du membre du personnel étaient tombés malades. Chez deux membres du personnel, la coproculture se révéla positive pour des salmonelles (Salmonella enterica serotype enteritidis).
La contamination d’œufs crus par ce type de salmonella étaient à l’époque souvent à l’origine d’infections d’origine alimentaire signalées en Flandre et partout en Belgique. Cette toxi-infection alimentaire collective démontra une fois de plus le risque lié à la présence d’œufs crus dans les plats. Les œufs utilisés pour préparer le tiramisu avaient été achetés dans un supermarché, où ils avaient été conservés à température ambiante (27).
d) Un mini foyer de SARM à l’USIN
Bien que les SARM fussent rares dans les USIN, un mini-foyer de SARM nosocomial du même type clonal fut tout de même observé chez trois nouveau-nés en 2002. Le SARM avait très probablement été introduit dans le service par une maman porteuse de ce staphylocoque doré. Après enquête, cette dernière s’est avérée être une professionnelle de la santé qui travaillait dans une maison de repos et de soins (28).
e) Cafards
La recherche de foyers d’infection ne se limitait pas aux micro-organismes classiques. Nous avons également été confrontés à l’infestation par des parasites de plusieurs services de notre hôpital. A noter que la lutte contre les parasites n’allait être confiée au service de prévention et à une entreprise externe de lutte anti-nuisible qu’à partir de 2019. Un foyer atypique de ce type s’était produit en 2003-2004 alors qu’un patient avait introduit des cafards dans l’hôpital via ses bagages. Ainsi, des cafards avaient été observés dans plusieurs services où le patient avait été hospitalisé(29).
f) Entérocoques résistants à la vancomycine (ERV)
Un foyer épidémique d’ERV dans le service d’hématologie (2014-2015) a pu être maitrisé grâce à la mise en œuvre de plusieurs mesures. Un dépistage systématique d’ERV a été instauré à partir d’échantillons de selles et de frottis rectal chez tous les patients admis dans le service confronté à l’épidémie. En plus du dépistage à l’admission dans le service des contrôles répétés étaient instaurés sur base hebdomadaire et à la sortie du patient afin de détecter les patients colonisés non connus. Enfin, les patients porteurs d’ERV étaient placés en isolement de contact en chambre seul, les chambres étaient nettoyées et désinfectées tous les jours et les patients porteurs d’ERV étaient soumis à une toilette corporelle quotidienne avec des gants de toilette antimicrobiens jetables (30,31).
g) Pseudomonas aeruginosa-VIM
Durant la pandémie de COVID, une augmentation significative de l’incidence de Pseudomonas aeruginosa-VIM fut enregistrée au sein de la cohorte 2021-COVID-USI à l’UZA. L’analyse de la consommation d’antibiotiques permit d’écarter rapidement l’éventualité d’un recours accru aux antibiotiques. Le regroupement des patients du COVID-19, au sein duquel les précautions standard n’étaient pas toujours correctement observées, comme le changement de gants en temps opportun, pouvait être à l’origine de la contamination croisée. Grâce à l’introduction de quelques précautions supplémentaires, le nombre d’infections/colonisations a pu être rapidement endigué. Dans la pratique, cela signifiait porter une blouse à usage unique supplémentaire en plus de l’équipement de protection individuelle (EPI) et la changer entre chaque patient, tout en soulignant l’importance de changer de gants en temps opportun. Comme un lien put être établi avec la présence de Pseudomonas aeruginosa-VIM isolé dans les siphons de l’USI, l’utilisation de l’eau du robinet fut proscrite et les siphons désinfectés tous les jours. La problématique de la contamination des éviers et des siphons par des bactéries environnementales a également été à l’origine d’une incidence accrue de Sphingomonas paucimobilis en 2005 à l’USI(32).
XI. Se préparer aux « maladies hautement infectieuses » et/ou aux maladies infectieuses émergentes (« New Emerging Infectious Diseases »)
Les fièvres hémorragiques virales (FHV) on fait l’objet d’une attention particulière en décembre 2000, suite à l’annonce par l’hôpital militaire (Neder-over-Heembeek) de son retrait d’engagement de se porter garant des installations nécessaires au transport, à l’admission et au traitement des patients souffrant de FHV. L’IMT, également partenaire de cet accord, attira l’attention du ministre sur ce point. Dans le cadre de l’accord existant entre l’UZA et l’IMT, le directeur adjoint de l’UZA de l’époque demanda de mettre au point une procédure pour réglementer l’accueil des patients atteints de FHV. Un groupe de travail multidisciplinaire comprenant les hygiénistes hospitaliers et des délégués de l’IMT et du service des urgences (URG) fut formé. Il allait en ressortir une série de points d’action, comme l’élaboration d’une procédure relative au diagnostic de laboratoire de l’IMT des quatre FHV (virus Lassa, virus de Marburg, virus Ebola et fièvre hémorragique de Crimée-Congo). L’objectif était de parvenir à un diagnostic rapide (dans les 48 à 78 heures). Une procédure de précautions fut également mise au point par l’EOHH pour la manipulation d’échantillons de laboratoire infectés par une FHV et les précautions à prendre lors de la prise en charge de patients (suspectés d’être) infectés par une FHV.
Une épidémie survenue en 2014 dans certains pays africains remit la FHV sous les feux de la rampe. Les procédures furent affinées, notamment celles pour enfiler et ôter les EPI. Il était initialement prévu que ces patients soient admis au service de soins infirmiers de médecine tropicale (ou à l’USI si nécessaire), mais finalement on opta pour une « unité d’isolement de haut niveau » (HLIU, séparée physiquement de l’hôpital) (Figure 17) pour accueillir ces patients sous la supervision d’un coordinateur catastrophe. En 2014, les discussions allaient encore bon train au niveau ministériel au sujet d’un « centre Ebola » à l’hôpital militaire de Neder-Over-Heembeek. Cela n’a pas empêché la composante médicale de la défense d’organiser en partenariat avec l’UZA des exercices périodiques, de simulation de transfert de patient infecté de Zaventem en ambulance de la défense vers le HLIU de l’UZA (Figure 18).
Figure 17

Figure 18

Outre Ebola, des maladies infectieuses jusque-là inconnues furent également mises en lumière, à savoir le SRAS en 2003, puis le MERS-CoV en 2012 et la grippe A H7/N9 en 2013. Des directives spécifiques furent mises au point pour les collaborateurs, comme les définitions de cas et les précautions à prendre.
Suite à l’épidémie de SRAS en 2003, on décida de mettre en place un groupe de travail afin d’uniformiser les directives relatives au SRAS à l’UZA. Ce groupe de travail comprenait des délégués des services concernés (USI, URG, médecine tropicale). Trois unités mobiles furent également prévues au service d’URG pour accueillir les patients (présumés) atteints du SRAS.
En 2009, une pandémie de grippe mexicaine ou grippe porcine (H1N1) fut suspectée (figure 19). Au cours de l’été 2009, le CHH prit les dispositions nécessaires pour un plan d’urgence contre la grippe, prévoyant le triage des patients et du personnel, l’hospitalisation des patients, le déploiement du personnel, la vaccination et la communication. C’est surtout l’aspect communication qui fut un point d’action pour l’EOHH. L’infection s’étant avérée plutôt bénigne, l’OMS annonça la fin de la pandémie dans le courant de l’été 2010. Le plan initial de lutte contre la pandémie de l’UZA n’était déjà plus tout à fait d’actualité en octobre 2009, comme l’achat d’un thermomètre infrarouge.
Figure 19 (Source : De Morgen, 27 avril 2009)

En octobre 2011, un germe « pan-résistant » fut signalé chez un patient admis à l’USI qui avait été transféré d’un hôpital de Crète. Ce patient s’avéra être porteur d’un germe multi-résistant qui sera par la suite communément appelé entérobactérie productrice de carbapénémase (EPC). Avant cela, des directives nationales avaient déjà été diffusées, indiquant que les patients transférés d’un hôpital situé dans une zone à haut risque devaient être isolés et soumis à un dépistage dès leur admission. Vu l’impact de l’épidémie majeure occasionnée par une souche de Klebsiella pneumoniae (EPC) productrice de carbapénémase de type OXA-48 à l’hôpital Maasland de Rotterdam, on n’attendit pas les textes officiels du gouvernement, et les directives existantes de l’ISP furent une nouvelle fois diffusées. En parallèle, des actions furent menées en matière de nettoyage, d’hygiène des mains, de politique d’isolement…
Certains(es) infirmiers(ères) en chef se montrèrent également vigilants.es lors de l’admission de patients provenant d’un hôpital asiatique (dépistage, isolement). Pour des raisons de faisabilité, il fut décidé de délimiter les groupes à haut risque (par exemple en provenance d’Asie et/ou du Moyen-Orient) et de déterminer comment ces groupes à haut risque pouvaient être le plus facilement localisés via les URG. Le nombre annuel de nouveaux patients porteurs de cette EPC allait s’élever à 44 (nosocomiaux et non nosocomiaux confondus) en 2017.
En 2018, l’OMS ajouta une nouvelle maladie à sa liste des maladies les plus redoutées « la maladie X », qui n’existait pas, mais était susceptible arriver….
XII. Nouveaux procédés et dispositifs médicaux
Au fil des ans, l’EOHH a joué un rôle important dans l’adaptation des procédures et l’introduction de nouveaux dispositifs médicaux dont la littérature avait démontré l’importante contribution à la prévention des infections. Certains d’entre eux sont décrits ci-après.
a) Hygiène des mains
Parmi les innombrables procédures, celle pour laquelle les adaptations et mises à jour furent les plus déterminantes sont sans aucun doute celles relatives de l’hygiène des mains. En 1994 déjà, l’EOHH publiait un article détaillant les avantages de l’utilisation d’alcool pour la désinfection es mains (33). Le recours à l’alcool pour les mains fut donc adopté assez rapidement par l’UZA comme norme d’hygiène des mains (34). Cependant, à cette époque, le lavage classique des mains à l’eau et au savon était encore encouragé par le Conseil supérieur de la santé (CSS) (Figure 20).
Figure 20 (Brochure Campagne Hygiène des mains (1991) basée sur les directives du CSS).
Passage de l’alcool pour les mains « fait maison » à l’alcool pour les mains commercial. Initialement, l’alcool utilisé pour la désinfection des mains était fabriqué à la pharmacie centrale de l’hôpital. Des supports métalliques en acier inoxydable avaient même été fabriqués sur mesure pour les conteneurs ronds relativement petits de 250 ml (figure 21).
Figure 21

Fin 2007, on décida de passer à des produits commerciaux satisfaisant également aux normes EN1500 et EN12791, respectivement pour la désinfection hygiénique et chirurgicale des mains. Cela impliquait par la même occasion la nécessité de devoir remplacer tous les petits supports métalliques, vu que ceux-ci n’étaient pas adaptés aux flacons d’alcool commerciaux. Un travail colossal pour le service technique qui dut installer les nouveaux supports et/ou remplacer les anciens dans toutes les chambres de patients, salles de consultation, toilettes, etc. L’occasion fut saisie pour suspendre les supports dans les chambres des patients plutôt que dans le couloir à côté de la porte de la chambre du patient. En effet, en 2001, le service d’incendie habilité avait fait remarquer que les couloirs devaient être considérés comme des voies d’évacuation et donc exempts d’obstacles supplémentaires susceptibles de présenter un danger.
Désinfection chirurgicale des mains
En 2003 un projet pilote fut lancé au quartier opératoire. Celui-ci consistait en l’introduction de la désinfection chirurgicale des mains à l’alcool chirurgical en remplacement du lavage des mains avec du savon désinfectant. Cependant, certains chirurgiens réticents insistèrent pour conserver les savons antiseptiques, car l’alcool asséchait trop la peau. Le CHH recommanda alors de réserver les savons désinfectants aux chirurgiens chez qui l’alcool pour les mains risquait effectivement de causer des problèmes de peau. Les effets indésirables de l’alcool pour les mains étaient probablement dus au fait qu’on ne laissait pas l’alcool sécher complètement avant d’enfiler les gants (35).
Solutions désinfectantes pour les mains sans alcool
L’alcool pour les mains étant trop irritant pour un petit groupe de collaborateurs souffrant de problèmes de peau chroniques, les affections cutanées persistaient parfois, ce qui nuisait également au respect de l’hygiène des mains, voire même chez certaines personnes l’abandon de la désinfection des mains. Ces membres du personnel venaient sporadiquement signaler des problèmes d’irritation cutanée à l’EOHH ou au médecin du travail. En 2010, une alternative sans alcool fut recherchée sur le marché, en concertation avec le service de médecine du travail. Les années suivantes, la gamme de produits sans alcool changera régulièrement, certaines marques ayant disparu du marché ou de nouveaux produits étant apparus (36).
b) Connecteurs sans aiguille
En avril 2000, une note de service sur l’utilisation des connecteurs sans aiguille fut distribuée à l’UZA. Elle stipulait que ces dispositifs ne pouvaient plus être utilisés. En effet, des connecteurs sans aiguille avaient été utilisés dans un service sans l’approbation du comité du matériel médical, et donc de manière incorrecte. Il fut décidé qu’à l’avenir ceux-ci puissent être utilisés après évaluation approfondie préalable et avis favorable du CHH. Au cours des années qui ont suivi, les infirmiers(ères) demandèrent régulièrement quand ces connecteurs sans aiguilles pourraient être à nouveau utilisés.
Cependant, il allait falloir encore attendre plusieurs années avant l’introduction des connecteurs sans aiguille dans les services, malgré les pressions exercées par différentes entreprises et leur utilisation dans d’autres hôpitaux. Cette décision s’avéra finalement judicieuse lorsque des rapports publiés en 2006 firent état d’une incidence accrue d’infections sanguines avec l’utilisation de certains types de connecteurs sans aiguille à pression positive. Ce n’est qu’en 2017, après avis positif du CHH, que le groupe de travail sur les soins impliquant l’utilisation d’un cathéter décida d’introduire l’usage des connecteurs sans aiguille à l’échelle de l’hôpital. Le connecteur sans aiguille deviendra la norme pour tous les cathéters veineux périphériques et centraux à partir de 2018, une fois les caractéristiques techniques auxquelles il doit satisfaire (translucidité, absence de déplacement de liquide dans le cathéter lors de la connexion ou de la déconnexion, septum fendu) clairement définies.
c) Décolonisation, et suivi du SARM
En 2009, plusieurs mesures furent prises à l’UZA pour améliorer et mieux suivre les résultats des traitements de décolonisation du SARM. Le fait de passer d’une décolonisation limitée aux seuls sites positifs connus à un traitement plus large (décolonisation du nez, de la gorge et de la peau) permit d’apporter une première amélioration, le pourcentage de patients ayant un dépistage de contrôle négatif augmentant après un premier traitement de décolonisation. L’introduction d’un système de suivi électronique du traitement entraîna par ailleurs une amélioration modeste de l’effet de décolonisation. L’introduction de gants et de bonnets de shampoing antibactériens augmenta une nouvelle fois le taux de réussite du traitement de décolonisation (37).
d) Ajustement des procédures d’isolement
Des procédures d’isolement simplifiées, selon la devise « keep it simple », s’avérèrent plus efficaces dans la pratique que les procédures sophistiquées, aussi bien intentionnées fussent-elles au départ. Ainsi, les différentes fiches d’isolement qui existaient aux premiers temps de l’hygiène hospitalière eurent le vent en poupe. En effet, au milieu des années 80, des fiches d’isolement étaient déjà utilisées, de couleurs différentes selon le type d’isolement (isolement strict, isolement de contact, isolement tuberculose, précautions entérales, isolement respiratoire, précautions pour le drainage de fluides corporels, précautions vis-à-vis du sang et des fluides corporels et isolement protecteur). Cette approche était largement basée sur les directives du CDC de 1983. En 1993, elles furent remplacées par deux types de fiche d’isolement : un pour l’isolement septique et l’autre pour l’isolement protecteur.
Isolement septique
En 1999, la procédure d’isolement fut adaptée aux directives américaines (1996), car la procédure de l’UZA s’était avérée incomplète en termes d’indications et peu claire quant à son utilisation (par exemple, l’isolement est-il nécessaire en cas de présence d’un germe multi-résistant dans l’urine ?). Afin de palier à son caractère incomplet (ne couvrant pas l’ensemble des situations rencontrées), il a procédure originelle stipulait, que les situations autres que celles énumérées étaient « à discuter avec l’hygiéniste hospitalier ». L’utilisation de produits désinfectants pour la décontamination terminale fut également revue et l’utilisation empirique des mesures de précaution et les définitions de germes multi-résistants furent clarifiées. Le terme « isolement septique » sera utilisé à partir de ce moment-là.
En 2007, la fiche d’isolement fut à nouveau adaptée : des pictogrammes furent ajoutés et les précautions à suivre furent étoffées. Les fiches exemplatives préremplies en fonction du mode de transmission et/ou du micro-organisme allaient pouvoir être consultées par la suite grâce au système de gestion des documents (« DocBase ») et un outil dit « de lutte contre les infections ». L’outil de lutte contre les infections s’est avéré être le fruit d’une intense collaboration, initiée dès 2016, entre le service de prévention et l’hygiène hospitalière et visant à élaborer un programme informatique sur l’intranet de l’UZA. Ce programme renseigne par germe les informations nécessaires sur les voies de transmission, les mesures de précaution, etc…des liens furent également ajoutés vers les procédures internes dans DocBase.
Parallèlement au remaniement du DPI en 2021, le remplissage de la fiche d’isolement a été informatisé, permettant ainsi d’obtenir automatiquement les mesures de précaution adéquates à appliquer en fonction de l’indication choisie.
Isolement des patients porteurs de d’entérobactéries productrices de BLSE
Tous les patients porteurs de bactéries productrices de BLSE étaient pris en charge dans une chambre individuelle jusqu’à la fin de l’année 2006 avec application des règles d’isolement, sans qu’une distinction soit effectuée entre les patients à haut risque et les autres. Au milieu de l’année 2007, la Belgian Infection Control Society (BICS) a proposé des directives en matière de prise en charge des patients porteurs de BLSE. Suite à celles-ci, le CHH a décidé de limiter l’isolement les patients porteurs à partir du 01/07/2007 uniquement dans les services à haut risque (USI, onco-hématologie, USIN, pneumologie/médecine tropicale et néphrologie). Par ailleurs, les critères d’isolement des patients au sein des services à risques, prenaient également en considération l’espèce bactérienne (Escherichia coli producteur de BLSE vs espèces productrices de BLSE autres que E. coli). Cette distinction avait comme implication que même dans des services à risques, les patients porteurs de E. coli producteurs de BLSE n’étaient plus isolés, sauf en cas de clusters de cette bactérie (sur base d’un antibiogramme). L’évaluation de cette nouvelle politique d’isolement réalisée après 4 ans a montré une diminution considérable du nombre de patients porteurs de bactéries BLSE+ placés en isolement (150 patients dans les services non à risques) sans que ceci n’entraîne par ailleurs une augmentation de l’incidence nosocomiale d’E. coli et de Klebsiella spp.,producteurs de BLSE, dans les services non à risques. A noter qu’une surestimation du nombre de cas nosocomiaux est fort possible étant donné qu’aucun screening systématique de présence de bactéries productrices de BLSE n’était réalisé chez les patients à l’admission. (38,39,40).
A partir de 2015, en conformité avec les nouvelles directives de l’EUCAST (The European Committee on Antimicrobial Susceptibility Testing), la présence de BLSE n’a plus été rapportée par le laboratoire. En conséquence, la procédure d’isolement a été modifiée de manière à ce que seule la catégorisation I ou R sur les résultats d’antibiogramme ne serve de critère pour la détection des MDRO (en accord avec les définitions de Sciensano) et l’isolement éventuel des patients (en. La même stratégie que celle utilisée pour les BLSE fut appliquée à ces MDRO, à savoir la distinction entre les services à haut risque et non à risque, et la prise en considération de l’espèce bactérienne MDRO : E. coli ou non-E. coli.
Isolement protecteur
Dès 1983, le CDC avait déjà cessé d’inclure cette forme d’isolement dans ses directives relatives aux précautions d’isolement dans les hôpitaux (Guideline for Isolation Precautions in Hospitals). En effet, l’efficacité de l’isolement protecteur n’a jamais pu être formellement établie comme une mesure protectrice des patients immunodéprimés (patients avec greffes d’organes ou neutropénie sous chimiothérapie) vis-à-vis de l’infection. Cependant, les patients ayant subi une transplantation d’organe à l’UZA ont continué à être placés en isolement protecteur après l’opération. En 2012, la procédure d’isolement des patients transplantés sera révisée en accord avec le conseil local de transplantation. Au final, une limitation de la durée de l’isolement des patients (une semaine au maximum) dans la phase immédiate de post-transplantation (une semaine au maximum) allait finalement constituera l’ajustement principal.
Jusqu’en 2000, les patients gravement immunodéprimés du service d’hématologie séjournaient dans des pièces vitrées minuscules, dont la dimension permettait juste d’accueillir un filtre à air, un lit, une table et une chaise percée. Ces chambres étaient appelées à tort « chambres stériles ». En cette période, le service d’hématologie disposait encore d’une cuisine séparée dans le service pour la préparation d’une « alimentation stérile» Malgré ces dispositions, plusieurs cas d’aspergillose furent signalés chez des patients dans l’unité. La source de ces infections pût être rattachée à la contamination de poivrons pré-emballés par de l’Aspergillus. En outre, jusqu’en 1998, le linge, les pannes de lit/urinaux et les ustensiles de cuisine en plastique étaient stérilisés pour les patients ayant subi une greffe de moelle osseuse (GMO). Il n’y avait pourtant aucun argument scientifique en ce sens, si bien qu’après plusieurs concertations avec le service d’hématologie, cette procédure fut finalement abandonnée. Les discussions portèrent également sur les inconvénients de la stérilisation à l’oxyde d’éthylène (OE).
En 2000, la rénovation du service d’hématologie a entraîné la suppression des petites chambres « stériles » dans lesquelles les patients devaient parfois séjourner fort longtemps. Les nouvelles chambres furent équipées de deux filtres à air (filtres HEPA, catégorie H13 avec une capacité de filtrage de > 99,95 %) installés dans le plafond. En complément de la filtration de l’air, et afin d’éviter l’introduction de particules de poussière et de micro-organismes de l’extérieur vers l’intérieur, un gradient de pression atmosphérique fut appliqué pour tout le service d’hématologie ; les chambres étant en surpression légère par rapport aux couloirs du service infirmier, les zones communes du service l’étant également vis-à-vis du reste de l’hôpital. De plus, l’ensemble du service infirmier était séparé du reste de l’hôpital par un sas. Grâce à ces rénovations, le nombre de chambres « stériles » fut porté de 6 à 20 avec une capacité de 29 lits (41).
e) Préparation préopératoire du patient
En 1999 déjà, le CDC recommandait l’utilisation de tondeuses plutôt que la lame de rasoir classique pour l’épilation préopératoire. Une autre recommandation portait sur la toilette/la douche préopératoire du patient avec un savon désinfectant, malgré la controverse concernant cette pratique. L’EOHH milita en faveur de l’application des recommandations du CDC. Celles-ci furent introduites à l’UZA à partir de 2001.
En parallèle, la mise en place d’une nouvelle technique mini-invasive de prélèvement par voie endoscopique de greffons veineux saphène (technique VasoView Hemopro 2®).dans le cadre de la chirurgie à cœur ouvert (pontages coronariens) permit de réduire considérablement l’incidence des ISO, de 2,95 % en 1992 à 0,43 % en 2001(42).
f) Claviers et dispositifs de pointage lavables
Lors de la mise en place du dossier électronique du patient à l’USI et à l’USI néonatale (Système de gestion de données de patients/Patient Data Management System (PDMS)/Metavision) en 2007, il fut décidé de recourir aux claviers standard lavables déjà utilisés à l’UZA sur les postes de travail du PDMS. Cependant, ces claviers présentaient l’inconvénient de laisser la saleté s’accumuler sous les touches. De plus, le clavier devait être démonté et retiré de la chambre pour son nettoyage, ce qui posait problème en cas d’isolement des patients. Les claviers n’étaient par conséquent pas nettoyés régulièrement. En 2003, l’EOHH lança un projet avec l’ICT pour trouver une meilleure alternative. Plusieurs claviers furent testés en conditions réelles, avec une surface parfaitement lisse et une bonne frappe pour principales exigences de qualité. Finalement, un clavier répondant à ces exigences fut retenu (Figure 22).
Figure 22

En 2006, les chariots de de soins des services infirmiers furent équipés d’ordinateurs portables. L’EOHH recommanda d’utiliser des claviers et des dispositifs de pointage (souris, trackball,…) lavables et désinfectables dans le contexte de leur utilisation dans un environnement clinique (au chevet du patient, au bloc opératoire, dans les chambres des patients, sur les chariots de visite et les chariots de soins). Initialement, une housse en plastique lavable recouvrait le clavier, mais cette approche s’est avérée peu concluante (43).
g) Nouvelle technique de prélèvement d’hémoculture
Depuis le début de ses activités en 1989, L’EOHH s’est impliquée activement dans la surveillance mensuelle du taux de contamination des hémocultures.
En 1999, une nouvelle procédure visant à réduire les taux de contamination associés à la réalisation d’hémocultures a été introduite dans l’hôpital. Ainsi, des bouchons stérilisés pour les flacons d’hémoculture furent distribués dans les services afin de ne plus devoir les désinfecter avant usage. De plus, un système de prélèvement sanguin avec adaptateur pré-assemblé (« Safety-Lok™ ») (figure 23) fut introduit afin de limiter les manipulations manuelles. Des séances de formation continue sur la prévention de la contamination des hémocultures furent organisées.
Figure 23
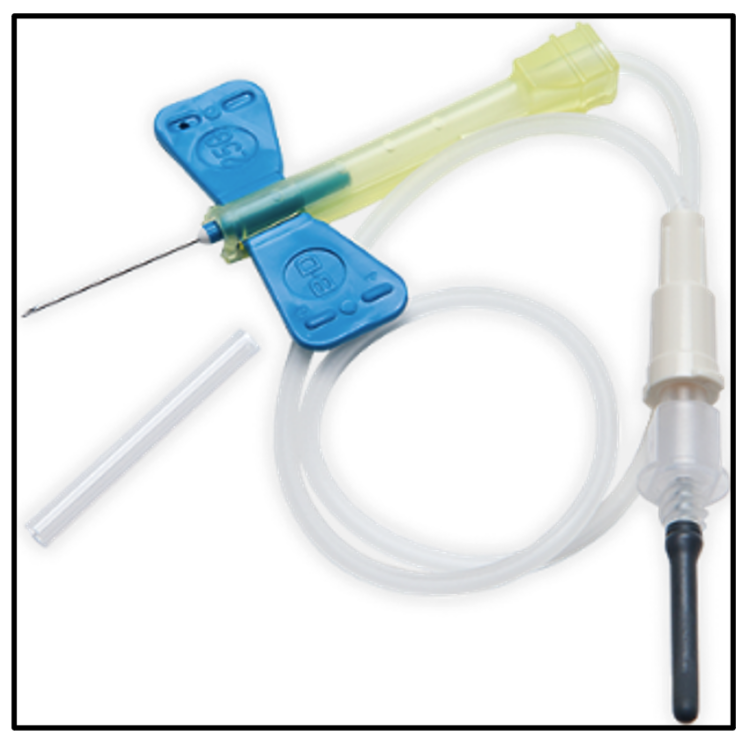
L’ensemble des mesures prises eurent un impact favorable sur le taux de contamination des hémocultures. Comparativement à 1998, le taux de contamination enregistra une baisse statistiquement significative en 2000.
h) Endoscopes
En 1995, les différents types d’endoscopes (flexibles et rigides) utilisés dans l’hôpital furent inventoriés. Les procédures de nettoyage et de désinfections furent également examinées. A cette époque, le nettoyage et désinfection manuelle étaient encore pratique courante avec l’utilisation de produits désinfectants très variés selon les disciplines médicales (alcool 70 %, Sekusept Forte 2 à 3 %, Gigasept 2 %, Aletex-28 et HAC 1 %). Par ailleurs, Il n’y avait pas d’uniformité en ce qui concerne les temps de contact des produits. En terme de moyens techniques, un dispositif de ventilation supplémentaire n’était disponible que pour les seules bronchoscopies afin d’extraire les vapeurs de glutaraldéhyde.
En 1996, les services concernés reçurent des directives concernant le nettoyage et la désinfection des endoscopes après usage. Il restait néanmoins de nombreux problèmes à résoudre, comme l’investissement pour la dotation d’endoscopes supplémentaires afin de respecter les temps de contact, l’installation de dispositifs de ventilation au bloc opératoire et en gastro-entérologie pour extraire les vapeurs de glutaraldéhyde et l’installation d’un poste d’eau stérile pour le rinçage des endoscopes après désinfection.
Un groupe de travail fut mis en place pour trouver une solution à cette problématique. Cela aboutit à l’achat de machines de nettoyage et de désinfection automatiques pour la gastro-entérologie en 1997. Suite au retour positif de leur utilisation, des machines automatiques de nettoyage et de désinfection supplémentaires furent ensuite également acquises pour la désinfection des bronchoscopes en 1999.
Pour les autres endoscopes (par exemple les sondes d’échocardiographie trans-œsophagienne), une désinfection manuelle de haut niveau au glutaraldéhyde fut d’abord appliquée avant de passer finalement au dioxyde de chlore (ClO2). En 2018, la désinfection des endoscopes rectaux et vaginaux se fit également au dioxyde de chlore, car les séances de stérilisation répétées endommageaient les sondes. Compte tenu du coût élevé de la désinfection au ClO2, une alternative moins onéreuse, mais aussi plus conviviale et efficace fut adoptée en 2020 sous la forme de lingettes désinfectantes.
i) Système de drainage urinaire en circuit fermé
L’introduction du système de drainage urinaire en circuit fermé fut critiquée en 1999. Les poches d’urine avec robinet à vider au chevet du patient étaient jugées « non hygiéniques ». Cependant, l’achat d’un nouveau type de collecteur n’avait pas été suffisamment préparé. Plusieurs problèmes furent rapidement constatés après le changement de système (fuites, gradation inexacte, nuisances olfactives…). Il fallut dès lors revenir temporairement aux collecteurs d’urine d’origine. Ce n’est qu’après discussion au sein de la Commission de matériel médical (CMM) et après avoir testé plusieurs types que le système de drainage urinaire en circuit fermé fut finalement adopté.
j) Fermeture (lock) et rinçage des cathéters au sérum physiologique
En 2016, le groupe de travail sur les soins impliquant l’utilisation d’un cathéter décida de ne plus rincer et fermer les cathéters qu’avec du sérum physiologique. Les infirmiers(ères) accueillirent favorablement le remplacement de la solution d’héparine par le sérum physiologique. En effet, il ne fallait plus diluer l’héparine, et des seringues de sérum physiologique prêtes à l’emploi étaient également fournies pour le rinçage et le verrouillage des cathéters.
k) Les animaux à l’hôpital
Dans un avis de 2005, le Conseil supérieur de la santé (CSS) décrétait qu’il fallait interdire l’accès des animaux de compagnie aux établissements de soins aigus, sous réserve d’un avis contraire motivé du CHH. Suite à cela, le CHH de l’UZA approuva en 2005 une procédure relative à l’autorisation des chiens d’assistance au sein de l’hôpital. Cependant, la procédure semblait être mal connue du personnel d’accueil et les animaux se voyaient donc refuser l’entrée. Une niche était également prévue aux URG pour accueillir temporairement ces chiens, mais elle ne sera finalement jamais utilisée à cette fin. Un groupe de travail fut mis en place en 2008 pour retravailler la procédure et aboutir à une procédure actualisée en 2009. Une brochure fut notamment mise à disposition à l’accueil de l’hôpital (figure 24).
Figure 24

Le 01/01/2014, le décret flamand modifié relatif à l’accessibilité des lieux publics aux personnes accompagnées de chiens d’assistance entra en vigueur. Suite à cela, le président de la Fédération belge des chiens d’assistance (BDAF) rappela à la ministre de la Santé publique que les chiens d’assistance étaient encore interdits dans de très nombreux hôpitaux. Dans l’intervalle, à l’UZA, la procédure avait été retravaillée au printemps 2014. Cette procédure modifiée avait pour but de fixer les modalités concernant les lieux de l’UZA où les chiens d’assistance étaient ou non admis et dans quelles conditions, et ce conformément à la réglementation en vigueur et aux conseils en la matière.
l) Systèmes de chauffage – refroidissement (Heater-cooler units)
En 2006, suite à un audit de l’EOHH, plusieurs recommandations en matière d’hygiène furent formulées concernant l’utilisation des générateurs thermiques (heater-cooler units) utilisés au bloc opératoire en chirurgie cardiaque sous circulation extra-corporelle.
Lorsque le CSS formula un avis (N°9327) en 2016 concernant la prévention des risques d’infection à Mycobacterium chimaera lors de l’utilisation d’un système de chauffage-refroidissement, la procédure appliquée à l’UZA fut également évaluée. Une nouvelle version de la procédure fut élaborée en 2017 par un groupe de travail réunissant le chef des perfusionnistes de circulation extracorporelle du bloc opératoire, le conseiller en prévention, le service technique et l’EOHH. Il fut ainsi déterminé comment et pour quel type de dispositif l’eau devait être traitée, et des dispositions furent prises en termes d’échantillonnage pour la mise en culture du M. chimaera.
XIII. Matériel et méthodes obsolètes
a) Désinfection au formaldéhyde (Aseptor® et Formovap®)
L’Aseptor® était une chambre fermée destinée à la désinfection au formaldéhyde (Figure 25) et se trouvait dans le couloir entre le bloc opératoire et l’USI. Il s’agissait d’un processus automatisé qui ne pouvait pas être interrompu, sauf en cas de concentration insuffisante de formaldéhyde. Un cycle durait 10 heures et nécessitait 500 ml de formol et 140 ml d’ammoniaque (pour la neutralisation). Après le cycle, les appareils et le mobilier devaient être nettoyés manuellement pour retirer les dépôts d’ammoniac sur les parties métalliques (poudre blanche). L’Aseptor® était utilisée pour désinfecter les respirateurs, les matelas chauffants et le matériel de scopie du bloc opératoire. Pour le service d’hématologie, on y désinfectait les livres, les revues et les PC des patients, tandis que pour l’USI et l’USIN, c’était tout le matériel de l’emplacement de soins dans lequel un patient était soigné selon les règles d’isolement (lit, table de chevet, appareils, couveuses, etc.) qui était concerné.
Aucun contrôle n’était effectué à l’aide de bio-indicateurs, de sorte que l’efficacité de la désinfection à l’Aseptor® ne pouvait être vérifiée.
Figure 25 (Source: British Journal of Anesthesiae, 1972 ; Volume 44, n° 8 : 7)

A partir de 1987, il fut décidé de ne plus recourir à une désinfection à base de vapeur de formol (Formovap®) des chambres de patients, des salles d’opération, etc.. On décida alors que la désinfection des chambres des patients pouvait se faire en toute sécurité selon les règles de l’isolement (par exemple pour la tuberculose) à l’aide d’une solution antiseptique (par exemple Velicin® forte).
Il était décrit dans la littérature que des résidus toxiques de formaldéhyde pouvaient se former sur les incubateurs, les respirateurs, etc. et avait des effets mutagènes et cancérigènes avérés chez l’homme. Le formaldéhyde était reconnu également pour son rôle agressif sur certains matériaux (plastique, caoutchouc). L’Aseptor® figurait également sur la liste des « mesures de désinfection inutiles et absurdes » (Daschner F. Hygiene, Müllreduktion und Umweltschutz in Kliniken, 1988).
Sur les conseils de l’EOHH, il fut décidé d’abandonner l’Aseptor® et d’adopter des méthodes alternatives de désinfection telles que décrites par le CDC en 1994.
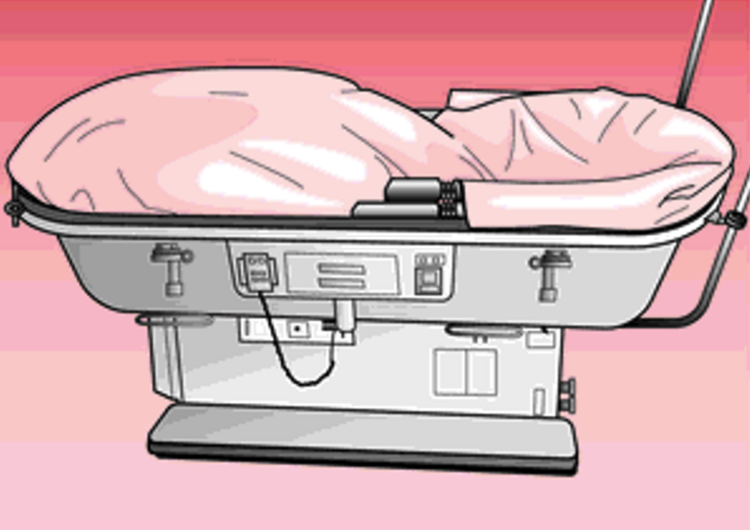
b) Lits Clinitron
Au début de l’EOHH en 1989, un lit Clinitron (figure 26) fut utilisé à l’UZA pour la prévention des escarres. Le principe reposait sur la création d’une surface remplie d’un matériau ressemblant à du sable (microsphères), sur laquelle le patient restait allongé. Cette méthode était très onéreuse et il fallait suivre une procédure spéciale pour l’obtenir. Par ailleurs, des préoccupations d’ordre hygiénique étaient également émise : ainsi, le lit devait être maintenu à une température constante de 24 °C en attente à la centrale de prêt, et était réchauffé à 36 °C sur demande. Cette période de chauffe durait environ six heures. Le lit, extrêmement lourd, devait ensuite être transporté dans l’unité de soins qui en avait fait la demande. Les microsphères étaient recouvertes d’une membrane filtrante qui devait être remplacée après usage ou lorsqu’elle était souillée. Des fluides corporels risquaient d’entrer en contact avec les microsphères ; en outre, l’utilisation de savons et de pommades était proscrite, car ils pouvaient altérer les microsphères. Les infections croisées liées à l’utilisation d’un tel lit ne pouvant être exclues, son utilisation fut abandonnée sur les conseils de l’EOHH.
Figure 26 : (Source : Elkin et al., 2000).
d) Stérilisation au gaz et restérilisation ou réutilisation des dispositifs médicaux
L’UZA renonça à la stérilisation au gaz à l’aide d’oxyde d’éthylène (EO) dès 1998 pour des raisons environnementales et de santé au travail pour la confier à l’entreprise externe Griffith. Le volume de matériaux confiés à la société Griffith pour stérilisation au gaz était déjà considérablement réduit à l’automne 1999. Une liste des articles éligibles à la stérilisation au gaz (265 articles différents) fut alors établie par le service de stérilisation centrale (SSC). Sur la base des enregistrements, il apparut que 17 % du matériel proposé ne pouvait pas être réutilisé ; il s’agissait principalement de matériel qui n’avait pas été utilisé (par exemple, du matériel à usage unique non utilisé dont l’emballage était ouvert). D’un point de vue terminologique, une distinction claire fut faite entre « réutilisation » et « re-stérilisation » : la première concernait les matériaux utilisés chez un patient, la seconde des matériels qui avaient été déstérilisés sans avoir été utilisés chez le patient (emballage ouvert ou date de péremption dépassée).
Depuis 2022, Il n’y a plus que les cathéters d’examen électrophysiologique (EEP) du cœur réalisés au laboratoire de cathétérisme du service de cardiologie qui sont réutilisés à l’UZA. Suite à l’arrêté royal du 12 mai 2021 portant exécution de la loi du 22 décembre 2020 relative aux dispositifs médicaux (MB 19.05.2021), nous nous sommes joints à l’UZ de Louvain et à l’hôpital Jessa de Hasselt pour engager un bureau de consultants afin d’analyser les aspects pratiques et financiers du retraitement de ces cathéters. Après analyse, Il fut décidé de poursuivre le retraitement. Pour cela, la qualité des cathéters réutilisés doit être évaluée par un organisme indépendant notifié afin de vérifier si les exigences légales sont respectées. Par ailleurs, le retraitement doit être communiqué à l’Agence fédérale des médicaments et des produits de santé (AFMPS), le dossier doit être approuvé et, enfin, la stérilisation centrale (SSC) doit également fonctionner selon une norme ISO.
d) Désinfection circulaire
Plusieurs études ont suggéré que la désinfection cutanée (par exemple avant la pose d’un cathéter) à l’aide de la technique dite « back-and-forth » (friction en va-et-vient) était plus efficace que la désinfection circulaire pour réduire la flore cutanée (Figures 27 et 28). Sur base de ce constat, il fut décidé d’abandonner la technique de désinfection circulaire et de promouvoir son remplacement par la technique du va-et-vient à partir de 2019 via des cours aux infirmières de référence en hygiène hospitalière.
Figures 27 et 28 (Source : Lynne Kerrigan, 2018)
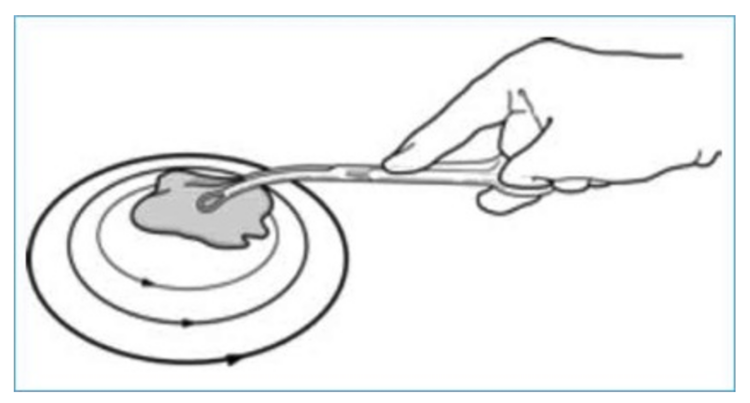

e) Tenue spécifique à la zone de travail
En 2002, des tenues spécifiques aux zones de travail furent inventoriées à l’UZA. Les tenues vertes étaient utilisées au bloc opératoire et dans le service des greffes, les bleues à l’USIN et les jaunes en stomatologie, au laboratoire de cathétérisme, à la clinique de fertilité et en gastroentérologie. Cependant, seules deux procédures de zone pour lesquelles les tenues spécifiques de travail étaient préconisées avaient été approuvées par le CHH de l’UZA dans le passé, à savoir celles pour la salle d’opération (y compris la salle d’accouchement) et pour l’USIN.
Comme aucun argument scientifique ne permettait de justifier le port d’une tenue spécifique dans les autres « zones » et aussi compte tenu de l’augmentation très importante du coût du linge (40 à 50 % d’augmentation), Il fut décidé de supprimer les tenues spécifiques dans toutes les zones de travail (à l’exception des tenues dédiées au bloc opératoire et à l’USIN).
XIV. Gestion des déchets
Une enquête réalisée en 1997 révéla que les déchets médicaux à haut risque n’étaient pas collectés de manière uniforme dans tous les services. Par ailleurs, tous les services ne disposaient pas des conteneurs adéquats. De surcroît, jusqu’en 1996, on utilisait des conteneurs à aiguilles avec couvercle à visser, ce qui donnait lieu à des accidents par piqûre. Il n’était pas rare alors que des bouteilles ou des bidons en plastique récupérés dans des établissements de santé soient utilisés pour collecter les objets piquants, comme le montre une illustration de 1989 (figure 29 )(2).
Une enquête que nous avions réalisée auprès d’infirmiers(ères) à domicile indépendants.es avait également révélé que les mesures de sécurité prises pour prévenir les accidents par piqûre étaient insuffisantes à cette époque (44,45).
Depuis 1996, l’UZA utilise des conteneurs à aiguilles spécifiques avec couvercles à rabat munis de fentes sur la surface supérieure pour retirer les aiguilles.
Figure 29 (Source: Herman Vanvinckenroye, IMT (1989).

Jusqu’en 1997, un certain flou régnait en Flandre quant à la manière de gérer les déchets médicaux. S’il y avait bien un décret de 1981 classifiant les déchets médicaux comme des déchets spéciaux, il fallut attendre 1997 et 2003 pour voir apparaître les décrets d’application (46,47,48).
XV. Visites et accréditation
a) Supervision par l’Agence flamande de la santé (Vlaams Agentschap Zorg en Gezondheid)

Dans les années 1990, une visite annuelle et annoncée de l’inspecteur adjoint de l’inspection sanitaire d’Anvers était effectuée pour contrôler les activités dans le cadre de la « Supervision du permis environnemental et de la prophylaxie des maladies infectieuses ». À chaque fois, une synthèse écrite des activités et des réalisations en matière d’hygiène hospitalière était fournie. Le 9 juillet 2008, l’Agence flamande de la santé adopta la position suivante concernant le « registre des décisions » imposé par l’AR de 2007 : afin de renforcer les avis du CHH, toutes les décisions devaient être consignées dans un registre selon un modèle standard. Elles devaient ensuite être transmises sous forme d’avis au directeur et mises à la disposition du médecin-inspecteur de l’agence pour vérification.
À partir de juillet 2012, le gouvernement flamand décida d’organiser différemment la surveillance des hôpitaux généraux. Dorénavant, deux types de surveillance étaient distingués, la surveillance du système et le contrôle de la compliance. Cette surveillance du système porte sur l’évaluation à l’échelle de l’hôpital des structures, des processus, des systèmes qualité, de l’audit interne… (L’ancien modèle de visite, donc). Dans le cadre du contrôle de la compliance, la supervision est étalée dans le temps, n’est pas annoncée et s’articule autour des trajets de soins. Les hôpitaux souhaitant obtenir une accréditation ne doivent plus passer par le modèle de visite qui implique une énorme charge de travail. Concrètement, cela signifiait que l’UZA — qui s’était engagé dans un processus d’accréditation (JCI (Joint Commission International)) ou avait déjà obtenu l’accréditation — était également systématiquement exempté de la surveillance du système. L’UZA avait également entamé la phase préparatoire pour obtenir l’accréditation JCI fin 2012 (49).
b) Accréditation JCI

Après la phase préparatoire, l’UZA devint l’un des premiers hôpitaux de Belgique à être accrédité par la JCI en 2015. En 2018, l’UZA obtint le label de qualité de la JCI pour la deuxième fois.
L’apport de l’EOHH fut déterminant à cet égard. En effet, un chapitre important de la norme JCI est consacré à la « Prévention et au contrôle des infections » (PCI). Le chapitre contient 11 normes, avec plusieurs éléments mesurables pour chaque norme (soit un total d’environ 80 indicateurs mesurables). Il fallait notamment rédiger de nombreux documents stratégiques et mettre à jour les procédures pour répondre aux exigences de qualité requises.
C) Agrément Magnet®

En 2017, l’UZA obtint l’agrément Magnet® en reconnaissance de la qualité des soins infirmiers. À cette fin, les données relatives à l’incidence des ICC et des IUAC sont collectées et enregistrées tous les trois mois dans une base de données centrale d’indicateurs de qualité (« National database of nursing quality indicators ») de l’American Nurse Association. En effet, les ICC et IUAC, ainsi que les chutes, les escarres… sont repris dans cet agrément Magnet® comme indicateurs importants de la qualité des soins infirmiers (« nurse sensitive quality indicators »).
XVI. Précautions lors des rénovations
Lors des rénovations effectuées en 1998 et 1999 à l’USIN, un ensemble de précautions avaient déjà été prises, tel le cloisonnement des zones de rénovations en cours. On avait également acquis de l’expérience avec les filtres à air mobiles. Ainsi, durant les rénovations de l’USIN, l’effet sur l’émission aérogène d’Aspergillus spp. à proximité des patients fut étudié. La mise en service de filtres à air mobiles entraîna une diminution significative des émissions d’Aspergillus spp. sur tous les sites, sauf dans la partie administrative et aux soins moyens (50,51,52,53).
En 2002, il fut décidé que les patients immunodéprimés devaient porter un masque FFP2 dans les zones en transformations pour les protéger de l’aspergillose. L’année suivante, les mesures de précaution furent étendues, des directives étant également données aux entreprises extérieures pour les rénovations.
En 2006, lorsqu’il apparut que les accords conclus n’étaient pas toujours respectés, des informations supplémentaires furent données aux médecins, aux infirmiers.ères en chef et au service interne de transport des patients.
En 2012, une nouvelle procédure entra en vigueur, en vertu de laquelle, sur proposition du chef des services techniques, un indice de risque pour les rénovations était déterminé en fonction des facteurs de risque des patients présents et de la nature des travaux. Suite à cela, les infirmiers.ères en chef furent à nouveau instruits sur les précautions à prendre lors de travaux de rénovation. Des mesures supplémentaires furent également décidées, comme le test d’un tapis adhésif retenant mieux la poussière et l’achat d’un filtre à air mobile supplémentaire vu le grand nombre de travaux de rénovation. À partir de ce moment, une check-list standard fut affichée sur les chantiers et put être utilisée lors des inspections par l’EOHH et le service technique (figure 30).
Figure 30 : check-list, tapis adhésif et appareil de décontamination de l’air sur un chantier.
XVII. À contre-courant
L’adaptation de certaines nouvelles méthodes de travail a suscité parfois des critiques et des réticences de la part des acteurs de terrain. Voir, par exemple, l’introduction de la désinfection chirurgicale des mains au quartier opératoire décrite plus haut.
a) Le « tablier blanc du bloc opératoire »
Autre exemple : la proposition du CHH, en 2010, de supprimer la surblouse (blanche) que les médecins et les infirmiers(ères) du bloc opératoire devaient porter en quittant le bloc. Dans la plupart des hôpitaux, il était/est de coutume que le personnel du bloc opératoire enfile une surblouse blanche par-dessus sa tenue de bloc lorsqu’il quitte le bloc pour, par exemple, prendre la pause déjeuner. Cette pratique était également avalisée à l’UZA jusqu’en 2010. Dans tout l’hôpital, des affiches (Figure 31) étaient accrochées à cet effet à des endroits stratégiques en 1995, reprenant les directives relatives à la tenue spécifique au bloc opératoire. En effet, on partait du principe que les uniformes (verts) portés au bloc pouvaient être contaminés en dehors du quartier opératoire. Plusieurs tentatives de suppression de cette directive se sont heurtées à chaque fois à la résistance des collaborateurs du bloc opératoire. Un consensus fut finalement trouvé en2010 pour supprimer ces surblouses blanches. En termes d’hygiène hospitalière, cela semblait être un pas en arrière pour certains membres du personnel, mais la décision fut prise sur la base d’une étude documentaire. En effet, aucune étude ne prouvait que le port d’une surblouse à la sortie du bloc opératoire contribue à éviter la fréquence de survenue des infections nosocomiales. Les seuls arguments avancés en faveur de la surblouse portaient sur « la discipline locale et l’esthétique », mais ils furent jugés insuffisants par le CHH pour pérenniser cette pratique. La suppression de la surblouse permit également de réaliser des économies, et le personnel du bloc opératoire lui-même put profiter d’une pause déjeuner en ce chaud mois de juillet 2010 plus léger (et soulagé ?) ! Sans compter que les tabliers étaient souvent portés trop longtemps avant d’être lavés. Dans ce contexte, on peut citer également le chef du laboratoire de microbiologie de l’époque, au début des années 1990, qui disait qu’en portant un tel tablier, avec la chaleur, les vêtements de travail devenaient de véritables bouillons de culture de germes…
Les tabliers blancs ne furent pas les seuls à être bannis, les couvre-chaussures en plastique que les collaborateurs externes au bloc devaient enfiler pour entrer dans la salle d’opération subirent le même sort. En effet, cette méthode présentait plus d’inconvénients que d’avantages, car le fait d’enfiler ces protections pouvait entraîner une contamination des mains.
Figure 31
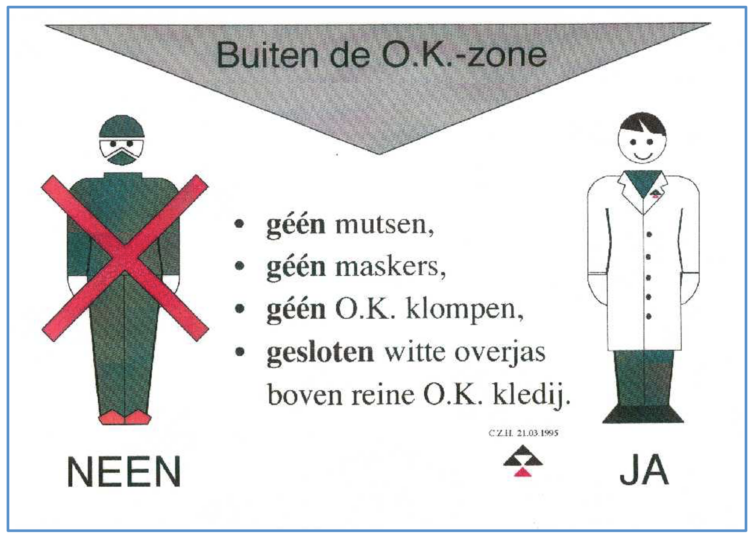
b) Le transport du patient dans son lit jusqu’à la salle d’opération
Des critiques ont parfois émané aussi des autorités. Ainsi, la commission de visite du gouvernement flamand dénonça en 2007 la procédure selon laquelle le lit du patient était conduit jusque dans la salle d’opération. Selon l’auditeur, il fallait à tout moment maintenir le nombre de micro-organismes dans l’air de la zone critique au niveau le plus bas possible. La manipulation de matelas et de literie ne pouvait pas être compatible avec une telle directive. L’auditeur recommanda une réévaluation critique de cette pratique en concertation avec le comité d’hygiène hospitalière. Les lignes directrices devaient ensuite être intégrées dans le règlement d’ordre intérieur. En réponse au manquement mentionné dans le rapport d’audit, l’EOHH invoqua les arguments nécessaires (en se référant au WIP néerlandais et au His-Working Party britannique, entre autres) pour conserver cette pratique. Néanmoins, la procédure fut affinée en précisant que le linge de lit devait être changé le jour de l’opération.
c) La toilette « sans eau »
L’introduction du concept de toilette sans eau en 2009 fut plus nuancée. Bien que cette pratique était démontrée présenter un avantage à la fois sur le plan de la prévention des infections et de l’investissement en temps, près de 16 % des infirmiers(ères) n’y étaient pas favorables, tandis que près de 27 % des infirmiers.ères considéraient que cette mesure ne permettait pas de laver les patients aussi bien qu’avec de l’eau et du savon (54,55).
Suite à des publications rapportant l’impact favorable de la toilette sèche à base d’antiseptique sur l’incidence des infections du sang, entre autres, il fut décidé en 2014 de passer à des gants de toilettes antimicrobiens imprégnés de chlorhexidine à 2 % (CHX) comme principe actif chez les patients hospitalisés à l’USI. Ce passage s’inscrivait dans le cadre d’un projet de recherche européen R-GNOSIS portant sur l’impact de différentes stratégies de décolonisation des patients sur le pronostic clinique et sur la prévalence du portage de bactéries résistantes aux antibiotiques (Ecological Effects of Decolonisation Strategies in Intensive Care).
Figure 32

Une corrélation put être établie entre l’introduction du lavage quotidien des patients à l’USI avec des gants de toilette contenant 2 % de CHX et une diminution importante de l’incidence des ICC et des MDRO dans l’unité. Il est cependant probable que cette diminution ait été probablement multifactorielle, car, d’une part, l’eau du robinet avait été éliminée en tant que source potentielle de bactéries pathogènes et, d’autre part, des mesures supplémentaires visant à prévenir les infections nosocomiales avaient été adoptées (56,57).
d) Abstention du port de gants en cas de MDRO
Un cluster survenu à l’UZA en juin 2005 montra que l’importance des gants comme moyen de prévention de la transmission des micro-organismes pouvait être remise en question. En effet, à la suite d’une épidémie de SARM dans un service de soins infirmiers, il fut décidé que les gants ne devaient plus être portés en cas de contact avec des patients atteints de SARM (sauf en cas de contact avec des fluides corporels ou lors de la manipulation d’agents anticancéreux). La décision fut prise à un moment où 11 patients atteints de SARM étaient présents dans le service concerné (sur un total de 23). L’accent fut toutefois mis sur l’importance du renforcement de l’hygiène des mains avec de la solution hydroalcoolique. Malgré le fait que ni les médecins ni les infirmiers(ères) ne portaient de gants, aucun autre patient porteur de SARM ne fut recensé dans le service au cours des semaines suivantes, malgré un dépistage hebdomadaire de tous les patients présents.
Ne pas porter de gants en cas de MDRO allait devenir la norme à l’UZA. Ce faisant, nous allions carrément à l’encontre des recommandations en la matière, comme celles du CSS. Cependant, nous estimions que, à la lumière de l’étude de la littérature et des observations de l’hygiène des mains dans la pratique, il y avait suffisamment d’arguments pour mettre l’accent sur la désinfection des mains plutôt que sur le port de gants (58,59).
e) Prolongation de la durée de mise en place des cathéters périphériques
Jusqu’en 1994, un cathéter périphérique ne pouvait rester in situ plus de 72 heures. En 1994, cette durée fut portée à 96 heures à l’UZA. À cette époque, les directives du CSS mentionnaient encore qu’un cathéter périphérique devait être remplacé toutes les 48-72 heures. En 2019, suite aux résultats d’une étude réalisée en interne et sur la base de données de la littérature, il fut décidé d’ajuster à nouveau cette durée. En effet, l’étude en interne avait révélé que le risque de phlébite était plus grand lorsque les cathéters étaient laissés en place pendant 96 heures. À partir de 2019, les cathéters périphériques ne furent remplacés que sur indication clinique, ce qui généra des économies importantes et évita aux patients des douleurs inutiles liées au remplacement systématique des cathéters en l’absence d’indication clinique (60).
XVIII. Le comité du matériel médical
En 2007, deux arrêtés royaux furent publiés, stipulant, d’une part, que l’EOHH devait contrôler tout ce qui avait trait à l’hygiène dans les activités hospitalières, comme l’achat de matériel et, d’autre part, qu’un médecin hygiéniste et un(e) infirmier(ère) hygiénistes hospitaliers(ères) devaient participer au comité du matériel médical 61). À l’UZA, un(e) infirmier(ère- hygiéniste hospitalier(ère) participait activement à l’achat des dispositifs médicaux (DM) tels que seringues, aiguilles, valves à trois voies, etc. depuis le début des années 1990 déjà.
À partir de 1993, une procédure fut élaborée concernant l’évaluation de DM pour le département de soins infirmiers. Avec le temps, cette procédure s’avéra inopérante, car des DM étaient encore régulièrement mis en service sans passer par la procédure d’évaluation préalable (voir connecteurs sans aiguille plus haut). C’est pourquoi, en 2008, des dispositions furent prises avec la direction des services logistiques de l’établissement et le pharmacien en chef pour exclure les circuits illégaux de test ou d’achat de matériel.
Concrètement, cela signifiait que des nouveaux produits qui n’avaient pas passé la procédure de test officielle ne pouvaient jamais être achetés.
La même année, une réunion d’équipe de test (RET) fut également mise en place, à laquelle un(e) infirmier(ère) hygiéniste hospitalier(ère) participait activement, comme pour le compte rendu des réunions. Cette réunion finit par devenir un groupe de travail du comité du matériel médical. Au cours des années suivantes, l’infirmier(ère)-hygiéniste hospitalier(ère) décidera avec le service des achats de l’élaboration ou du renouvellement de nouveaux contrats dans le cadre de dossiers où la connaissance des normes européennes s’avèrera de plus en plus importante au fil des ans.
En 1989, cependant, il n’existait pratiquement aucune norme européenne pour les DM, à l’exception des EPI comme les masques respiratoires ou « respirateurs », qui devaient être conformes au règlement européen 89/686/CEE et porter une étiquette CE avec un numéro d’enregistrement.
Le choix de la marque de DM était donc déterminé par les résultats de ses propres tests et/ou les normes américaines (ASTM) lorsqu’elles étaient disponibles. Les emballages des gants chirurgicaux proposés par les fabricants à cette époque manquaient généralement d’informations essentielles (figure 33). La directive européenne 93/42/CEE change progressivement la donne. De nombreux produits sont considérés comme des dispositifs médicaux, ce qui signifie qu’ils doivent porter le label CE. Les années suivantes, les normes se succéderont ou des modifications seront apportées à celles qui existent déjà. À titre d’exemple : EN 455-1 : 1993 pour les gants médicaux, EN 13795:2004 pour les vêtements et champs chirurgicaux ou EN 14683:2005 pour les masques chirurgicaux (modifiée par EN 14683:2014) (62,63,64,65,66).
Figure 33
L’infirmier(ère) hygiéniste hospitalier(ère) jouera également un rôle important dans le suivi des tests du matériel médical. Mais la recherche de matériel alternatif par l’infirmier(ère)-hygiéniste hospitalier(ère) en collaboration avec la centrale d’achat et l’entrepôt central en cas de rupture de stock atteindra son paroxysme lors de la crise du coronavirus en 2020.
XIX. Désinfectants
Comme pour les DM, l’importance de la connaissance les normes européennes relatives aux désinfectants augmentera également au fil des ans. Ainsi, la norme EN 14883 « Antiseptiques et désinfectants chimiques » parut en 2006. Cette norme énumère les normes disponibles permettant de déterminer l’efficacité d’un désinfectant. Elle sera amendée à plusieurs reprises au cours des années suivantes. En 2013, le « Règlement concernant la mise à disposition sur le marché et l’utilisation des produits biocides » entrera également en vigueur, distinguant les désinfectants qui doivent être considérés comme un biocide par rapport à ceux qui sont considérés comme un dispositif médical.
Les désinfectants utilisés à l’hôpital ont changé plusieurs fois au cours des dernières années. Les produits toxiques pour la désinfection des DM ou de l’environnement comme le glutaraldéhyde ou les dérivés phénolés ont été remplacés par des produits moins nocifs. Ainsi, Velicin® forte (dérivé phénolé) et Sekusept® Forte (glutaraldéhyde) furent encore utilisés à l’UZA jusqu’en 2002 pour la désinfection terminale des chambres d’isolement et pour la désinfection de certains instruments. En 2005, un produit à composés de 2 alcools et d’ammonium quaternaire (isopropyl-tridécyl-diméthylammonium), dont la toxicité (DL50 >2000 mg/kg) était 10 fois moindre que celle du produit à base de glucoprotamine utilisé jusqu’alors, fut retenu comme désinfectant standard pour l’environnement et les DM. La facilité d’utilisation était également prise en compte et, en même temps que le changement, il fut décidé d’équiper tous les services de pompes doseuses automatiques, ce qui permit d’éviter les erreurs de dilution ou le gaspillage de désinfectant suite à un surdosage.
L’hypochlorite de sodium (« eau de Javel »), utilisé pour la désinfection des Clostridioides difficiles, entre autres, fut remplacé par des mono-doses d’acide peracétique. Bien que la Javel n’ait jamais posé aucun problème en termes d’hygiène professionnelle, le produit fut banni de l’hôpital autant que possible pour des raisons environnementales. Les patients s’étaient également plaints de nuisances olfactives (67,68).
En outre, le dosage de plusieurs désinfectants fut également ajusté. Ce fut le cas en 1999, entre autres, pour la CHX en solution aqueuse présente dans l’antiseptique HAC qui était alors encore utilisé de manière standard pour la décontamination du dans les services ; et dont la concentration fut portée de 1 % à 3,5 %. Dans le cadre du « Central line bundle », la concentration de CHX dans l’alcool fut portée de 0,5 % à 2 % pour la désinfection du site d’insertion en 2003. En 2002, on décida de passer à la Bétadine alcoolique pour la désinfection préopératoire de la peau, en remplacement de la solution aqueuse utilisée jusqu’alors.
En 2006, un formulaire « Nettoyage et désinfection des plaies » fut élaboré à l’UZA au sein du groupe de travail sur les soins de plaies. Le nombre de types de désinfectants fut limité par la même occasion. Ainsi, l’éosine ne fut plus reprise comme désinfectant. Cependant, comme l’éosine est un médicament enregistré, qui peut être prescrit par un médecin (par exemple pour les plaies de pied de diabétique), une quantité limitée d’éosine en unidose fut conservée à la pharmacie.
Parmi les désinfectants retenus, on optait prioritairement pour des produits unidoses afin de réduire le risque de contamination des désinfectants à base d’eau. En effet, dans les années 1980, plusieurs pseudoépidémies (hémocultures faussement positives) de Burkholderia (Pseudomonas) cepacia avaient été documentées à l’UZA, à cause de fioles (250 ml) de CHX à 0,5 % en solution aqueuse contaminées lors de la production. Le groupe de travail sur les soins de plaies définit également les indications pour la désinfection des plaies. Ainsi, les plaies chirurgicales fermées de façon primaire ne furent plus désinfectées, mais seulement nettoyées.
À partir de 2007, la procédure « Désinfectants » définit clairement la durée de conservation après première utilisation d’un désinfectant. Après avoir été étendue aux produits de soins en 2013, cette procédure fut ensuite mise à jour annuellement en concertation avec le pharmacien en chef.
Tous les désinfectants utilisés dans l’hôpital étaient inventoriés chaque année en concertation avec le coordinateur environnement depuis 2011. Suite à l’arrêté royal du 08/05/2014 relatif à la mise à disposition sur le marché et à l’utilisation des produits biocides, les produits appartenant au circuit fermé furent également contrôlés à partir de 2016 (69).
En 2015, un nébuliseur mobile pour la désinfection des pièces avec du peroxyde d’hydrogène à 12 % fut acheté sur le budget de l’hygiène hospitalière. Dorénavant, l’appareil allait être utilisé par le service de nettoyage pour désinfecter les chambres d’isolement après le séjour de patients atteints de SARM, de CDIF, d’ERV, d’EPC et, enfin, de Sars-CoV-2.
À plusieurs reprises dans le passé, l’EOHH avait été contactée pour avis en cas de rupture de stock ou d’arrêt de la production de désinfectants. Cela fut encore le cas récemment en 2020 pour les lingettes désinfectantes à usage unique destinées aux bébés prématurés (Stellisept®) qui n’étaient plus distribués en Belgique ou encore en 2022 pour la chloramine 0,5 % en raison de la rareté des produits de base chez le fabricant.
XX. Collaboration avec des hôpitaux néerlandais
En 1994, un premier contact eut lieu entre l’EOHH de l’UZA et des cardiologues de Vlissingen afin d’orienter des patients néerlandais nécessitant une chirurgie cardiaque vers l’UZA. À cette époque, cependant, il y avait peu de patients néerlandais, si bien que ces accords ne furent pas prolongés. En décembre 1999, certains hôpitaux de Breda et l’UZA travaillèrent en concertation pour élaborer des directives claires concernant les conditions de transferts de nouveau-nés de l’UZA vers les hôpitaux de Breda et inversement. Cette décision fut prise en raison de la faible incidence du SARM à l’UZA et de l’existence de règles d’isolement pour empêcher la propagation du SARM. Pour les hôpitaux de Breda, ces données motivaient la mise en place d’une politique adaptée pour pouvoir réadmettre des nouveau-nés provenant de l’UZA et ainsi déroger à la politique des Pays-Bas concernant les réadmissions de patients à partir d’hôpitaux étrangers. Un protocole fut élaboré et mis en œuvre. La question du transfert vers l’UZA de patients Hollandais pour des soins cardiologiques se posa à nouveau en 2001 suite à une pénurie de cardiologues aux Pays-Bas. Rapidement, au printemps 2001, des accords furent conclus avec les hôpitaux de Vlissingen et de Goes, non seulement pour les patients de cardiologie et les nouveau-nés, mais aussi pour tous les patients des unités de soins intensifs/unités de soins critiques toutes spécialités confondues. Un protocole de transfert fut élaboré en s’inspirant de celui de l’hôpital Ignatius de Breda. Par la suite, des accords furent également conclus entre l’UZA et l’hôpital Ruwaard à Spijkenissen, l’hôpital Ikazia à Rotterdam, l’hôpital Franciscus à Roosendaal et l’hôpital Albert Schweizer à Dordrecht. En 2002, les médias firent état d’« immigration médicale » ou de « tourisme hospitalier ». Par ces termes, ils désignaient le phénomène selon lequel des patients étrangers se réfugiaient dans les hôpitaux belges faute de capacité d’accueil suffisante dans leur pays. Finalement, seule la coopération avec l’hôpital de Vlissingen/Goes durera des années avant de s’éteindre à la suite de la crise du coronavirus (70,71).
XXI. Projet IRIS (Infection Risk Scan)
Figure 34

Il s’agit d’un projet interrégional impliquant des hôpitaux belges et néerlandais. L’IRIS (infection risk scan – analyse préventive du risque infectieux) est une méthode de surveillance qui identifie les procédures et les résultats en matière de prévention des infections, tant au niveau qualitatif que quantitatif. À l’UZA, cette analyse fut réalisée en 2017 et 2018 dans quatre services différents pendant deux mois. L’IRIS permet d’avoir une vision globale du service en matière de prévention des infections.
Dans ce cadre, une étude de prévalence de la colonisation intestinale par MDRO fut menée dans les quatre services. Outre les données administratives des patients inclus, des données concernant l’utilisation d’antibiotiques, la présence de cathéters vésicaux et intravasculaires, le score de MacCabe, un séjour antérieur dans un autre établissement de santé (étranger) et l’admission ou non en chambre individuelle avec salle de bain privative furent également collectées. Outre ces indicateurs liés aux patients, des indicateurs propres au service furent également recueillis : pollution environnementale, données sur l’hygiène des mains, vêtements et conditions structurelles (équipement de protection, rince-pannes, etc.).
Les données étaient saisies dans le programme IRIS et traitées en externe.
XXII. Audits dans les services
Un groupe de travail « hôpital propre » fut mis en place en 2006, se concentrant notamment sur les zones accessibles au public (hall d’entrée, toilettes) et de stockage des produits de nettoyage. Outre l’EOHH, le service technique, le service de prévention, le directeur des soins infirmiers, le service de communication et le service logistique faisaient également partie de ce groupe de travail.
Dans le cadre de la semaine de la sécurité et du projet « hôpital propre », l’année suivante, l’EOHH, en concertation avec le directeur des soins infirmiers, prit l’initiative de réaliser des audits dans plusieurs services de soins infirmiers choisis au hasard. Lors de ces visites inopinées des hygiénistes hospitaliers, divers aspects liés à l’ordre, à la propreté et à l’hygiène étaient examinés. Les services concernés recevaient un retour d’information afin de leur permettre de mettre en œuvre les actions correctives nécessaires.
Dans le cadre de la préparation pour l’accréditation JCI, des « visites d’établissement » étaient organisées avec le service technique, la direction des soins infirmiers et l’EOHH. Los de ces visites, l’accent était mis sur la séparation entre « sale » et « propre » dans les services infirmiers (par exemple, pas de produits de soins dans l’espace de rinçage). Il en résultera une procédure : « les dix commandements de la propreté ».
La liste de contrôle pour les audits, déjà élaborée par l’EOHH en 2007, fit peau neuve en 2016: les contrôles sur place pouvaient être enregistrés sur une tablette via une « application traceur de l’hygiène hospitalière » et transmis en temps réel à un tableau de bord afin que les résultats (scores) soient accessibles à tous sur l’intranet.
Sur suggestion des auditeurs de la JCI, une matrice de tous les services fut établie et on détermina pour chaque service la date et la fréquence de réalisation de l’audit. Cette forme d’audit a finalement été supprimée en concertation avec le Service Qualité en raison de la charge importante de travail qu’elle représentait.
L’EOHH se concentra plutôt sur les contrôles d’environnement grâce à l’ATPmétrie.
En 2018, un groupe de travail « carton tertiaire » fut créé. Ce groupe comprenait l’EOHH et des représentants de la pharmacie, de l’entrepôt, du service qualité et du service des achats. L’objectif était de réduire la présence d’emballage tertiaire dans les services. En l’occurrence, la pharmacie et l’entrepôt central étaient au centre de l’attention, puisque ces deux secteurs d’activité constituaient les principaux distributeurs de matériel acheminés vers les différents services. Il s’agissait de vérifier régulièrement la présence de carton tertiaire dans les chariots de transport. En 2019, l’objectif fut atteint avec seulement moins de 10 % de cartons tertiaires présents dans les services par rapport à la valeur de base de 30% lors du premier audit.
En plus des audits précités, d’autres audits furent réalisés sur la gestion du linge (y compris la blanchisserie externe), la cuisine centrale (traiteur externe) et la biberonnerie en collaboration avec le département des services logistiques.
XXIII. Hygiène alimentaire
En 2002, le CSS publia un avis sur les infections néonatales causées par Enterobacter sakazakii en lien avec la préparation de poudre de lait non stérile. Suite à cela, un groupe de travail fut mis en place pour évaluer l’application du principe HACCP dans la préparation des aliments lactés (à la fois dans la biberonnerie centrale et de manière décentralisée dans les services). Le groupe de travail se composait de représentants de l’EOHH, de l’USIN et du service de diététique. Il en résulta des pratiques adaptées en matière de préparation, de transport et de stockage ; la question de l’allaitement maternel fut également abordée. Par ailleurs, des audits furent également réalisés périodiquement dans les services concernés. Le groupe de travail resta actif jusqu’en 2009 et fut intégré en 2010 au groupe de travail sur la sécurité et l’hygiène alimentaire dans lequel siégeaient également le traiteur externe et le service logistique.
En 2018, un audit fut réalisé par l’Agence fédérale pour la sécurité de la chaîne alimentaire (AFSCA) pour la première fois dans une cuisine de service sélectionnée au hasard dans une unité de soins infirmiers de l’UZA. Jusque-là, l’audit de l’AFSCA s’était limité à la cuisine centrale de l’hôpital. Cet audit plus complet permit d’affiner la procédure relative à la sécurité alimentaire dans une unité de soins (72).
XXIV. Lutte contre les nuisibles
Un premier plan de lutte contre les nuisibles fut élaboré par l’EOHH et le service de prévention en 1999. Cependant, le flou persista jusqu’à la fin de l’année 2019 quant à savoir qui était responsable de la lutte contre les nuisibles, à savoir le service de prévention, le département des services logistiques ou l’hygiène hospitalière. Finalement, en 2020, il fut décidé de conclure un nouveau contrat avec une entreprise de lutte contre les nuisibles afin que les interventions puissent avoir lieu plus rapidement notamment durant les week-ends. Le signalement des nuisibles pendant la journée devait se faire via le service de prévention.
Par le passé, c’était l’EOHH qui était contactée à chaque fois que des nuisibles étaient présents et les interventions étaient discutées en concertation avec le service de prévention (73,74).
a) Puces
Lors de la construction de l’UZA en 1979, le choix s’était porté sur un tapis plain dans le hall d’entrée central de l’hôpital. Cependant, pendant les mois d’été en particulier, le personnel administratif travaillant dans des zones recouvertes de moquette signalait régulièrement des problèmes de piqûres de puces. Il est très vraisemblable que les larves de puces étaient introduites dans l’hôpital par les chaussures. Le traitement insecticide était géré par le service de prévention. Face à ce problème, l’EOHH recommanda en 1999 de ne plus placer de tapis plain lors de la rénovation du hall d’entrée.
b) Asticots
Les premiers incidents impliquant des asticots furent signalés en 1999 dans la salle d’autopsie qui où était également réalisées des autopsies pour le compte du Parquet (médecine légale). Leur élimination fut confiée à l’entreprise de lutte contre les nuisibles.
c) Insectes volants
La présence d’insectes volants a été signalée à de nombreuses reprises. En particulier, un incident lié à la présence de mouches à fruits dans le service d’hématologie contraignit le service à ne plus autoriser que l’introduction de fruits par les visiteurs dans le service. En fait, les fruits restaient trop longtemps dans la chambre du patient, ce qui provoquait une infestation de mouches à fruits.
D’autres insectes comme les coccinelles et les mouches étaient parfois nichés dans les coffrages des volets ou des stores, nécessitant l’intervention du service technique. Dans certain cas, sur les conseils de l’EOHH, une pulvérisation d’insecticide était effectuée dans la pièce à l’aide du dispositif Nocospray®. Cette méthode fut également utilisée à partir de 2018 dans les chambres où avaient été admis des patients atteints de gale.
d) Cafards
Depuis 1994, l’UZA fait contractuellement appel à une société d’extermination pour mener des interventions préventives dans certaines zones de l’hôpital. Grâce à cette approche, aucun cafard ne fut signalé pendant des années. Cependant, en 2003 des cafards ont été découverts dans plusieurs services. Il s’est avéré qu’ils avaient été introduits dans l’hôpital par un patient via ses bagages (voir plus haut).
e) Rongeurs
La dératisation (rats et souris) est confiée à une entreprise d’extermination externe qui travaille avec des boîtes à appât (qui ne peuvent être ouvertes qu’avec une clé). L’appât est vérifié et remplacé tous les deux mois. L’entreprise garantit l’absence de rongeurs depuis 1999.
L’EOHH fut néanmoins contactée en 2007 suite à la présence de déjections de rats dans la cuisine centrale. Une « enquête » plus poussée révéla qu’il s’agissait en réalité de noyaux d’olives…
f) Punaises de lit
Lorsque des punaises de lit furent signalées par le service infirmier de pédiatrie en 2019, une procédure fut élaborée en concertation avec le service de prévention pour déterminer comment reconnaître les punaises de lit, qui contacter (service de prévention) et quelles précautions prendre (comme l’isolement, les conseils au patient et à la famille). Il fut également stipulé qu’aucun insecticide ne devait être utilisé de sa propre initiative, mais que la lutte devait être confiée à une entreprise externe de lutte contre les nuisibles, car les punaises de lit sont très résistantes.
XXV. Infirmiers.ères-hygiénistes hospitaliers.ères de référence
Suite à l’AR 2007, le directeur général de l’Organisation des établissements de santé souligna l’utilité de créer un réseau d’infirmiers(ères)-hygiénistes hospitaliers(ères) de référence. L’année suivante, l’EOHH élabora un programme de formation en interne des premiers(ères) infirmiers(ères) de référence. Toutefois, il fut décidé en concertation avec la direction soins infirmiers que leurs attributions ne se limiteraient pas aux seuls aspects de l’hygiène hospitalière, mais qu’elles porteraient aussi sur la sécurité des patients. Par conséquent, le titre devint « Infirmier(ère) de référence en matière d’hygiène et de sécurité des patients ». Un profil de compétence fut également établi. En 2022, quatre réunions de concertation ont été organisées avec les infirmier(ères) de référence, au cours desquelles furent abordées diverses thématiques liées à l’hygiène hospitalière.
XXVI. La plateforme régionale anversoise pour l’hygiène hospitalière
En 1992, le service d’hygiène hospitalière de l’A.Z. St-Jan (Bruges) eut l’idée novatrice à l’époque de créer un groupe de travail régional regroupant les hygiénistes de plusieurs hôpitaux de Flandre-Occidentale afin d’améliorer la prévention et le contrôle des infections nosocomiales. En 1997, sous l’impulsion du Prof. H. Goossens (UZA/UA), un groupe de travail similaire fut instauré dans la région d’Anvers.
Une première réunion se tint le 6 octobre 1997, 46 personnes y assistèrent. Des groupes de travail furent rapidement mis en place. L’EOHH de l’UZA participa activement à plusieurs d’entre eux (gestion des déchets, prévention de la légionellose, gestion et maintenance des endoscopes, prions, et les gants).
La participation de l’équipe d’hygiène hospitalière aux réunions de la plateforme régionale deviendra ultérieurement un des indicateurs structurels de qualité en hygiène hospitalière.
XXVII. Partage d’expérience et de connaissances
Au cours des trente dernières années l’EOHH a réalisé de nombreuses publications et synthèses de qui furent publiées dans des revues nationales et internationales. Plusieurs livres sur l’hygiène hospitalière furent également publiés entre 2000 et 2006. En effet, ceci répondait aux missions d’un hôpital universitaire de partager l’expérience et les connaissances le plus largement possible. De nombreuses conférences et leçons furent également réalisées dans des écoles, des établissements de santé, à des infirmiers(ères) à domicile et lors de conférences/symposiums.
La grande majorité de ces publications ont été publiées dans « Noso-info ». Si elles n’ont été publiées qu’en néerlandais et en français, nous nous sommes ralliés involontairement, aux critiques formulées par certains sur l’anglophilie du monde universitaire: en effet, la publication quasi exclusive des articles scientifiques en anglais laisse sous-entendre que le néerlandais ou le français ne sont plus considérés comme adaptés à la science et que nous n’autorisons plus l’accès à la connaissance à ceux qui parlent uniquement ou principalement le néerlandais ou le français (selon Freek Van de Velde, professeur de néerlandistique (KU Leuven) dans De Morgen 23/03/2022).
XXVIII. Conclusion
Il est possible qu’un certain nombre de sujets relatifs à l’hygiène hospitalière n’aient pas été abordés, ou seulement de manière limitée, mais il est difficile de résumer en quelques pages plus de 30 ans d’expérience en matière d’hygiène hospitalière. Cela étant, de tout ce qui précède, il ressort que le métier d’hygiéniste hospitalier est un métier dynamique, varié, offrant beaucoup de contacts, de nombreux échange et qui laisse une place importante à la concertation pluridisciplinaire (74).
Nombre des thèmes abordés ont aussi fait l’objet de publications, dont une version numérique peut être obtenue sur simple demande à l’adresse électronique suivante fvanlaer@telenet.be.
Avec tous mes remerciements à mes anciens collègues Regina, Jean-Paul, Frieda, Kurt, Miel, et à l’actuelle EOHH Hilde, Elise et Hannelore.
XXIX. Références
1. Van Laer F., Gillisjans F. Zorg dragen voor AIDS-patiënten. De rol van de verpleegkundige. Hera (Nieuwsbrief van het Interprovinciaal AIDS-coördinaat),1991 ; 3:22-24.
2. Van Laer F. Behoedzame zorg. De verpleging van AIDS-patiënten. Een terugblik. Hera (Tijdschrift voor AIDS- preventiewerkers),1989;1:14-17.
3. Van Laer F. Hygiëne en preventie in de huiskamer. Hera,1989;4:3.
4. Van Laer F. Hiv- en aids-patiënten. Specifieke zorgen bij hiv-geïnfecteerden. Thuiszorg Nieuwsbrief, 1999;17:1-3.
5. Van Laer F. Hiv- en aids-patiënten. Preventiemaatregelen. Thuiszorg Nieuwsbrief, 1999;18:1-4.
6. Sion J.P., Van Laer F. Observation of surgical site infection in orthopaedics until after discharge. Abstract n° F5/3 at the 3rd International Conference of the Hospital Infection Society, Londen 1994.
7. Van Laer F., Sion J.P., Nuyts R. Postoperatieve wondinfecties op orthopedie. De invloed van follow-up na ontslag. Tijdschrift voor Hygiëne en Infectiepreventie,1994;1:14-18.
8. Van Laer F, Goossens H, Jansens H, Ieven M. Cijfers antibioticaresistentie. Methodologische problemen bij de berekening. Tijdschrift voor Hygiëne en Infectiepreventie, 1999;4:101-104.
9. Frank Van Laer, Elke Coenen. Impact des aiguilles à ailettes sécurisées sur l’incidence des accidents par piqûres à l’UZA Noso-info, 2017 ; 21(4) : 2-4
10. Frank Van Laer, Tim Mertens. Accidents par piqûres avec des aiguilles à pointes de Huber à l’Hôpital Universitaire d’Anvers (UZA) Noso-info, 2020 ; 24(4) : 2-4
11. Knaepkens L, Van Laer F. Preventie van prikongevallen bij gebruik van een insuline-injectiepen (Prévention des accidents par piqûre lors de l’utilisation d’un stylo
d’injection pour insuline). Noso-info,2008;12(4):2-4.
12. Van Laer F. De problematiek van de insuline-injectiepennen – Aanvulling. Noso-info, 2009;13(3):2-3.
13. F. Van Laer. Glucometer-lancetten en –prikpennen. Risico’s voor de gezondheidswerker en de patiënt (Lancettes et stylos autopiqueurs de glucomètre. Risque pour le personnel de santé et le patient). Noso-info, 2010;14(1):2-6.
14. Van Laer F, Roelandt R, Coenen E. Letter to the editor. Occupational risk of blood-borne viruses in healthcare workers. Infection Control and Hospital Epidemiology, 2002;23:712.
15. F. A. Van Laer , E. Coenen , H. Jansens. Occupational risk of blood-borne viruses in healthcare workers: a 20-year surveillance. Antimicrobial Resistance and Infection
Control 2019, 8(Suppl 1):148. Poster session P220.
16. Ieven M, Vercauteren, Descheemaeker P, Van Laer F, Goossens H. Comparison of Direct Plating and Broth Enrichment Culture for Detection of Intestinal Colonization
by Glycopeptide-Resistant Enterococci among Hospitalized Patients. Journal of Clinical Microbiology, 1999; 37(5): 1436-1440
17. Leens E, Van Laer F. Accidentele bloedcontacten in het operatiekwartier (Accidents exposant au sang au bloc opératoire). Noso-info, 2006;10(3):4-9.
18. Frank Van Laer. CLABSI-definities in de neonatologie. Noso-info, 2019; 23(4): 5-7
19. F. Van Laer, D. Verhelst, H. Jansens, E. Goovaerts. Responsabilisation du patient. Le patient est-il prêt ? Noso-info, 2015 ; 19(1) : 2-6
20. Frank Van Laer, Filip Bosschaerts, Philippe Prosperi, Ann Segers, Hilde Jansens, Emiel Goovaerts. Evaluatie van de patiëntenfolder over handhygiëne in het UZA. (Évaluation
de la brochure patient concernant l’hygiène de mains à l’UZA) Noso-info, 2012;16(1): 4-5
21. Jansens H, Van Laer F, Ieven M, Goossens H. Evaluation of an early warning system for methicillin-resistant Staphylococcus aureus. Abstract 147 at the 13th annual scientific meeting of the Society for Healthcare Epidemiology of America, 2003, Arlington, Virginia.
22. Van Laer F, Jansens H, Claeys R, Goossens H. Legionellose. Surveillance na een outbreak. Het Belgische Ziekenhuis, 1998;4:38-41.
23. Frank Van Laer, Hilde Jansens, Emiel Goovaerts. Surveillance de la légionellose après une éruption Noso-info, 2013 ; 17(4) : 10-14
24. Frank Van Laer, Hilde Jansens, Emiel Goovaerts. Surveillance van legionellose in een universitair ziekenhuis tussen 1984 en 2013. Vlaams Infectieziektebulletin, 2014;5: 4-7
25. Van Laer F. Het nieuwe Vlaamse legionellabesluit. Noso-info, 2007;11(3):17-18.
26. Van Laer F., Raes D., Vandamme P., Lammens C., Sion JP., Vrints C., Snoeck J., Goossens H. An outbreak of Burkholderia cepacia with septicemia on a cardiology ward. Infection Control and Hospital Epidemiology, 1998;19:112-113.
27. Van Laer F. Een collectieve voedselinfectie op een verpleegafdeling. Epidemiologisch Bulletin van deVlaamse Gemeenschap, 2001;36:2-4.
28. Jansens H, Van Laer F, Ieven M, Lammens C, Goossens H. A mini-outbreak of methicillin-resistant Staphylococcus aureus infections in a neonatal intensive care unit.
Abstract 171 at the 13th annual scientific meeting of the Society for Healthcare Epidemiology of America, 2003, Arlington, Virginia.
29. Van Laer F. Een patiënt bracht kakkerlakken mee in zijn bagage (Le patient amenait des cafards dans ses bagages). Noso-info, 2004; 13 (3): 2-3
30. H Jansens, F Van Laer , E Goovaerts , K Loens. Successful control of vancomycin-resitant enterococci outbreak in a hematology unit. Antimicrobial Resistance and Infection
Control 2015, 4(Suppl 1):P199.
31. Frank Van Laer, Hilde Jansens, Emiel Goovaerts. Beheersing van een uitbraak van vancomycine resistente enterokokken op een hematologische afdeling in het UZA.
Noso-info, 2016; 20(2): 2-4
32. Frank Van Laer, Elise Van Cauwenberg, Hilde Jansens. Quel impact de la pandémie de COVID-19 sur l’incidence des infections nosocomiales à l’UZA ? Noso-info, 2021 ;
25(1) : 2-3
33. Van Laer F., Claeys R. Controversen i.v.m. handhygiëne. Handalcohol versus water en zeep. Verpleegkundigen en Gemeenschapszorg,1994;5:157-159.
34. Frank Van Laer, Hilde Jansens. Kommentaar op het abstract van D. Pittet in Noso-info vol IV n°4, 2000, pg 18. Multiresistente bacteriën en ziekenhuishygiëne. Noso-info,
2001;5(2):12.
35. Frank Van Laer. Désinfection chirurgicale des mains. Noso-info, 2007;11(2):11.
36. Frank Van Laer. Alcoholvrije handrubs (Solutions désinfectantes pour les mains sans alcool). Noso-info, 2010; 14(2): 11.
37. E. Goovaerts, F. Van Laer, H. Jansens. Resultaten van het gewijzigd MRSA-dekolonisatiebeleid in het Universitair Ziekenhuis Antwerpen. Noso-info, 2013; 17(2): 2-6
38. Van Laer F, Jansens H, Goovaerts E, Goossens H. Epidemiologie van ESBL-producerende micro-organismen in het Universitair Ziekenhuis Antwerpen (UZA)
(Épidémiologie des germes producteurs de betalactamase à spectre étendu à l’Universitair Ziekenhuis Antwerpen (UZA)). Noso-info, 2006;10(2):8-11.
39. H. Jansens E. Goovaerts F. Van Laer. Evaluation of the implementation of a change in isolation precautions for extended-spectrum betalactamase producing
Enterobacteriaceae (ESBL-E). The Journal of Hospital Infection, 2010; 76(Supplement 1): S56. Poster session P17.14.
40. Frank Van Laer, Hilde Jansens, Emiel Goovaerts. De incidentie van ESBL-positieve Enterobacteriaceae. Vier jaar na toepassing van de BICS-richtlijnen. (L’incidence
des entérobactéries productrices de BLSE quatre ans après l’application des directives du BICS). Noso-info, 2012; 16(2): 2-4
41. Frank Van Laer, Hilde Jansens, Karin Bal, Steven Van Eester. Preventie en surveillance van aspergillose bij hematologische patiënten in het Universitair Ziekenhuis
Antwerpen (UZA). Noso-info, 2019; 23(1): 5-8
42. Frank Van Laer, Kurt De Maeyer, Hilde Jansens, Inez Rodrigus. De invloed van gewijzigde pre- en peroperatieve procedures op de incidentie van postoperatieve
wondinfecties in de cardiochirurgie. Gastpresentatie op de 2de NSIH-dag. WIV, Brussel. Endoscopische chirurgie (wiv-isp.be).
43. Van Laer F. Hygiënisch omgaan met klavieren en aanwijsapparaten (muizen) (Manipulation hygiénique des claviers et dispositifs de pointage (souris). Noso-info,2009 ;
13(2) : 2-4
44. Van Laer F A. Compliance with universal precautions among self-employed home-care nurses. Archives of Public Health, 1996;54,243-249.
45. Van Laer F, Vanherck M-J. Preventie van bloedoverdraagbare aandoeningen door Vlaamse zelfstandige thuisverpleegkundigen. Een vergelijking van twee studies. (Prévention des affections transmissibles par voie sanguine auprès des infirmiers à domicile indépendants flamands. Une comparaison de deux études). Noso-info, 2006 ; 10(1) : 12-14.
46. Van Laer F., Sion J.P. Ziekenhuisafval. Een poging tot rationele benadering van specifiek ziekenhuisafval. Tijdschrift voor Hygiëne en Infectiepreventie,1993;1:15-20.
47. Van laer F. Verwarring omtrent ziekenhuisafval. V.B.V.K.- tijdschrift,1993;juli/aug.:2-3.
48. Van Laer F. Afvalbeheer in een rustoord en/of RVT. Verpleegkundig Kader, 1999;4:23-25.
49. Frank Van Laer, Hilde Jansens. Van visitatie naar accreditatie. Noso-info, 2013;17(2):7-8.
50. Mahieu L, De Dooy J, Van Laer F, Jansens H. Emissie van Aspergillus species tijdens verbouwingswerken op de dienst Neonatologie van het Universitair Ziekenhuis
Antwerpen. Epidemiologisch Bulletin van de Vlaamse Gemeenschap, 2000;31:1-5.
51. Mahieu L, De Dooy J, Van Laer F, Jansens H, Ieven M. Surveillance van de emissie van Aspergillus species tijdens verbouwingswerken op de dienst Neonatologie van
het Universitair Ziekenhuis Antwerpen. Noso-info, 2000;1:2-7.
52. Mahieu LM, De Dooy JJ, Van Laer FA, Jansens H, Ieven MM. A prospective study on factors influencing aspergillus spore load in the air during renovation works in a neonatal
intensive care unit. Journal of Hospital Infection, 2000;45:191-197.
53. Frank Van Laer. Luchtdecontaminatie zonder HEPA-
filtratie, Noso-info, 2008; 12(2):1-2.
54. Frank Van Laer. Eenmalig te gebruiken geïmpregneerde washandjes. Ervaringen in het UZA, Noso-info, 2016;20(3):12-17.
55. F. Van Laer, Hilde Jansens, Emiel Goovaerts. Gecontamineerde geïmpregneerde washandjes voor eenmalig gebruik (Contamination des gants de toilette imprégnés à usage unique) Noso-info, 2012;16(1): 4-5
56. Frank Van Laer, Elise Van Cauwenberg, Hilde Jansens. Eenmalig te gebruiken chloorhexidine-geïmpregneerde washandjes. Impact op MDRO en CLABSI bij patiënten
op de intensieve zorgenafdeling van het UZA. Noso-info, 2020;24(2): 2-5
57. F. A. Van Laer, E. Van Cauwenberg, H. Jansens. Effect of daily chlorhexidine bathing on hospital acquired infection in intensive care units. Antimicrobial Resistance and
Infection Control 2019, 8(Suppl 1):O41
58. Van Laer F. Aanvullingen bij de keuze van wegwerphandschoenen. Noso-info, 2002;6(4):22.
59. Van Laer F, Jansens H, Goovaerts E. Onderzoekshandschoenen: vloek of zegen? (Gants
de protection : malédiction ou bénédiction ?) Noso-info, 2005;9(4):17-20.
60. Frank Van Laer, Hilde Jansens, Emiel Goovaerts. Evaluatie van het verlengen van de verblijfsduur van korte perifere katheters. Noso-info, 2017;21(3): 7-10
61. Frank Van Laer. Materialenkennis en ziekenhuishygiëne. Noso-info, 2015;19(2): 8-11
62. Van Laer F, Haxhe JJ. Maskers: welke, wanneer en hoe? (Des masques : lesquels, quand et comment ?). Noso-info, 2003 ; 7(2) : 4-7.
63. Van Laer F. De Europese norm EN 13795 voor chirurgisch afdekmateriaal en operatiekleding (Normes européennes EN 13 795 des champs chirurgicaux et des vêtements de quartier opératoire : Mise en conformité). Noso-info, 2004;8(4):13-14.
64. Van Laer F. Chirurgische maskers (Masques chirurgicaux). Noso-info, 2005;9(2):15-17.
65. Van Laer F. Graad van bescherming van beschermingspakken tegen biologische agentia. Noso-info, 2014, Vol XVIII, n° 4 : 5-6 Van Laer F. Degré d’efficacité
des combinaisons de protection contre les agents biologiques. Noso-info, 2014;18(4):5-6.
66. Frank Van Laer. Isolatieschorten conform EN 13795, EN 14126, AATCC 42, of ASTM F 1670?. Noso-info, 2016 ; 20(2) : 11-13.
67. Van Laer FA, Verdyck R, Jansens H, Coenen E. Disinfectants Containing Chlorine: An Occupational Hazard? Infect Control Hosp Epidemiol 2008;29:474–474.
68. Van Laer FA, Verdyck R, Jansens H, Coenen E. Chloorhoudende ontsmettingsmiddelen en arbeidsveiligheid, Noso-info, 2008;12(2):1-2.
69. Frank Van Laer. Biociden van het gesloten circuit. Noso-info,2021;25(3):5-7.
70. Van Mier M, Van Laer F. MRSA zonder grenzen. Tijdschrift voor Hygiëne en Infectiepreventie, 2003;2:31-34.
71. Van Laer F, Van Mier M. MRSA zonder grenzen. (MRSA sans frontières). Noso-info, 2003;7(2):12-16.
72. Van Laer F. Zilvervisjes [brief]. The Belgian Pest Control Magazine, 1996;6:9.
73. Van Laer F, Verdijck R, Jansens H. Ongediertebestrijding. Een ongediertebestrijdingsplan in een universitair Ziekenhuis. Tijdschrift voor Hygiëne en Infectiepreventie, 2001;2:38-40.
74. Hoe ziekenhuishygiëne in dertig jaar evolueerde. Netwerk verpleegkunde, 2022, nr.3:19-21.


