Context
Antimicrobiële resistentie (AMR) is wereldwijd een groeiend probleem. Het vermindert de doeltreffendheid van antimicrobiële middelen bij de behandeling van infectieziekten bij mens en dier, wat leidt tot een hogere morbiditeit en mortaliteit en hogere kosten. Het staat vast dat er een sterk verband bestaat tussen het gebruik van antimicrobiële middelen en de ontwikkeling van resistentie. Daarom moet een verantwoord en verstandig gebruik van antimicrobiële middelen worden aangemoedigd. Het belang van het monitoren van het gebruik van antimicrobiële middelen werd in juni 2017 benadrukt in het « One Health Action Plan against Antimicrobial Resistance » van de Europese Commissie (1).
Het nieuwe Belgische nationale actieplan « One Health » tegen AMR (2021-2024) bevat ook verschillende benaderingen om het verstandig gebruik van antimicrobiële middelen te verbeteren en nieuwe indicatoren om het effect van deze benaderingen op antimicrobiële consumptie en resistentie te monitoren (2).
Het European Surveillance of Antimicrobial Consumption Network of ESAC-Net wordt gecoördineerd door het Europees Centrum voor ziektepreventie en -bestrijding (ECDC, Stockholm, SE). Dit netwerk verzamelt gegevens over het gebruik van antimicrobiële geneesmiddelen in de ambulante en de ziekenhuissector volgens een gemeenschappelijke methode voor alle deelnemende landen (3). Naast ESAC-Net, dat alleen geaggregeerde gegevens voor alle Belgische ziekenhuizen bevat, is ook een meer gedetailleerde monitoring van de antimicrobiële consumptie per ziekenhuis opgezet. Tussen 2007-2013 dienden de ziekenhuizen in het kader van het project Antibiotic Use in Hospitals (ABUH) jaarlijks hun factureringsgegevens voor antimicrobiële consumptie in te voeren op de NSIH website van Sciensano. In het huidige project (Belgian Hospitals – Surveillance of Antimicrobial Consumption, BeH-SAC) worden administratieve gegevens van het Rijksinstituut voor ziekte- en invaliditeitsverzekering (RIZIV) gebruikt en in nationale rapporten gepubliceerd op het interactieve Healthstat-platform. Elk ziekenhuis kan ook aanpasbare ziekenhuisrapporten krijgen ter vergelijking (benchmarking) met stratificatie per soort, type of grootte van het ziekenhuis en/of per regio, door in te loggen met een elektronische identiteitskaart die gekoppeld is aan een eHealth-account (4).
Methodologie
Eenmaal per jaar verstrekt Sciensano geaggregeerde antimicrobiële consumptiegegevens voor de ambulante sector en de ziekenhuissector, ontvangen van het RIZIV, aan ECDC. Geschat werd dat in 2021 ongeveer 98% van de Belgische bevolking een ziektekostenverzekering had en daarom in de RIZIV-gegevens werd opgenomen. Deze gegevens werden geëxtrapoleerd om de gehele Belgische bevolking te dekken (cijfers van Eurostat) voordat ze naar ECDC werden gestuurd. In ESAC-Net worden deze cijfers vervolgens vertaald in Defined Daily Dose (DDD)/1000 inwoners/dag (DID). Antimicrobiële middelen worden ingedeeld in groepen volgens de Anatomical Therapeutic Chemical Classification (ATC) van de Wereldgezondheidsorganisatie (WHO) (5). Er kan opgemerkt worden dat sinds 2018 (6,7) een schatting van de totale consumptie van fluoroquinolones wordt gemaakt op basis van een vergelijking tussen gegevens over de totale verkoop (IQVIA, vergoede en niet-vergoede verkoop) en RIZIV-gegevens (Farmanet, alleen vergoede consumptie), waarbij het jaar 2017 als referentiejaar wordt gebruikt.
Voor de BeH-SAC-surveillance worden ook administratieve gegevens van het RIZIV verzameld. Deze gegevens omvatten tellergegevens (het aantal verbruikte eenheden antimicrobiële middelen ingedeeld volgens de WHO ATC code) en noemergegevens (het aantal ligdagen en het aantal opnames), opgesplitst per jaar, kwartaal, ziekenhuis, afdeling waaronder chirurgie, interne geneeskunde, geriatrie, pediatrie, intensieve en niet-intensieve neonatologie, materniteit, infectieziekten, brandwondenafdeling, intensieve zorgen afdeling en andere gespecialiseerde diensten.
Het verbruik wordt momenteel uitgedrukt als DDD/1000 ligdagen en DDD/1000 opnames. De ziekenhuizen worden ingedeeld naar soort (acute, categorische, psychiatrische), naar type (primair, secundair, tertiair), naar grootte (klein < 400 bedden, gemiddeld 400-600 bedden, groot > 600 bedden) en naar regio (Vlaanderen, Wallonië, Brussel) op basis van een lijst van ziekenhuizen die door de Federale Overheidsdienst Volksgezondheid, Veiligheid van de Voedselketen en Leefmilieu is verkregen.
Het volledige BeH-SAC-surveillance protocol, de recentste gebruikte lijst van DDDs (2023) en de instructies zijn te vinden op de Sciensano-webpagina (8).
Resultaten
De resultaten van de surveillance van het antimicrobiële verbruik in de ambulante en ziekenhuissector worden in de volgende paragrafen voorgesteld overeenkomstig de gekwantificeerde doelstellingen die in het Belgische nationale actieplan « One Health » ter bestrijding van AMR (NAP-AMR 2021-2024) zijn vastgesteld (2).
Ambulante sector
Doelstelling 1: Geleidelijke daling van 5-10% per jaar van het totale antibioticaverbruik om te komen tot een globale daling van 40% ten opzichte van 2019.
De afgelopen tien jaar is het verbruik van antibacteriële middelen voor systemisch gebruik (ATC-groep J01) in de ambulante sector aanzienlijk gedaald (-33,2%), wat geldt voor elk van de J01-subgroepen. Met name werd tussen 2019 en 2021 een daling van 19% van het totale verbruik vastgesteld (van 19,8 naar 16,0 DID) – wat een aanzienlijke vooruitgang betekent in de richting van de doelstelling van een vermindering van 40% van de NAP-AMR tegen 2024 (2). Dit is echter geen jaar-op-jaar vermindering, maar eerder een vermindering met 23% tussen 2019 en 2020, gevolgd door een marginale stijging het jaar daarop (+4,9%). Deze trends houden allicht grotendeels verband met getroffen maatregelen in verband met de COVID-19-pandemie en bijhorende gedragsveranderingen. Het zal belangrijk zijn na te gaan of de consumptie in 2022 terug toeneemt of de vermindering van de totale J01-consumptie zich voortzet. Het verbruik in de Belgische ambulante sector blijft echter boven het Europese gemiddelde (14,8 DID in 2021, Figuur 1, blauwe lijn) en er zullen aanzienlijke inspanningen nodig zijn om de voor 2024 gestelde doelen te bereiken (11,9 DID in 2024, Figuur 1, rode lijn) (9).
Figuur 1 ● Evolutie van de totale en per subgroep consumptie van systemische antibacteriële middelen (ATC-groep J01) uitgedrukt in DID in de Belgische ambulante sector en Europese gemiddelde, 2012-2021.
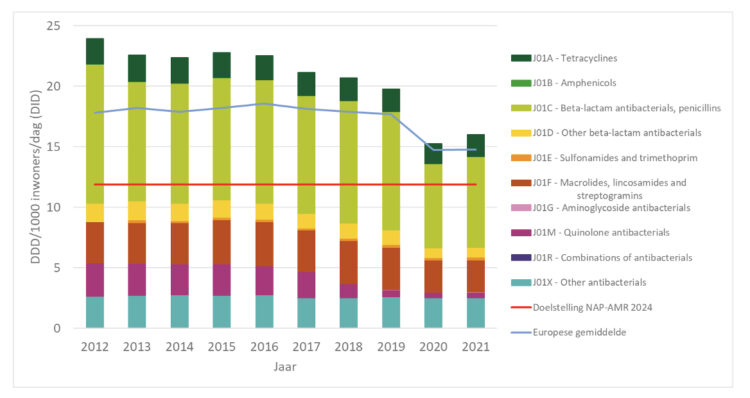
Bron: ESAC-Net. ATC : Anatomical Therapeutic Chemical Classification ; DID : DDD/1000 inwoners/dag ; NAP-AMR : National Action Plan on Antimicrobial Resistance.
Doelstelling 2: Daling van het gebruik van quinolones, om ten laatste tegen 2024 een maximumverbruik van 5% quinolones ten opzichte van het totale antibioticaverbruik te bereiken.
De vermindering van de consumptie van fluoroquinolones tot 5% van de totale consumptie van antimicrobiële middelen van ATC-groep J01 is sinds 2014 een nationale doelstelling ( ). Om het gebruik ervan te verminderen, zijn de terugbetalingscriteria voor fluoroquinolones op 1 mei 2018 gewijzigd, zodat ze nu alleen worden terugbetaald voor de behandeling van een klein aantal welomschreven infecties (6,7). Door deze wijzigingen worden de totale verkoopgegevens gecombineerd met terugbetalingsgegevens om de totale consumptie van fluoroquinolones in België te schatten. Deze maatregelen hebben geleid tot een aanzienlijke vermindering van het verbruik van fluoroquinolones, met een relatieve vermindering van 57,4% van 2012 tot 2021 in termen van DID (van 2,77 tot 1,18 DID). Hoewel het aandeel van de consumptie van fluoroquinolones in de totale antimicrobiële consumptie tussen 2012 en 2021 is gedaald van 11,5% naar 7%, blijft het boven de doelstelling van 5% en is het tussen 2019 en 2021 zelfs gestegen (Figuur 2).
Figuur 2 ● Percentage consumptie van fluoroquinolones (J01MA) ten opzichte van totale consumptie van antibacteriële middelen voor systemisch gebruik (J01) in de ambulante sector, 2012-2021, België. Belgique.
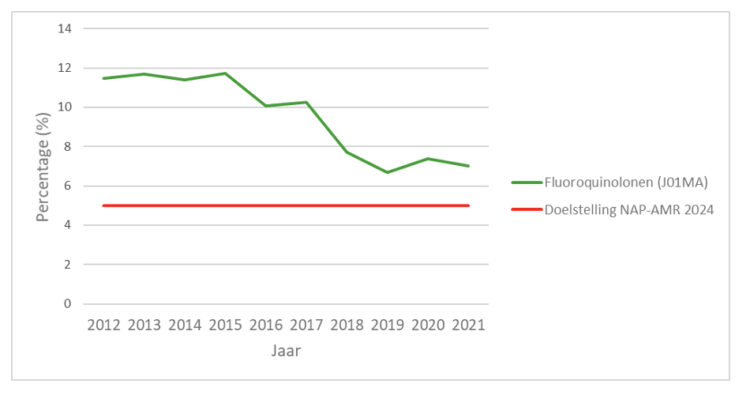
Bron: ESAC-Net gegevens gecombineerd met totale verkoopgegevens (IQVIA) voor fluoroquinolones. NAP-AMR: National Action Plan on Antimicrobial Resistance.
Doelstelling 3: Voortdurende verbetering van de kwaliteit van het voorschrift : afname van het voorschrijven van breedspectrum-antibiotica ten aanzien van het totaal aantal antibiotica; stijging van de verhouding amoxicilline/amoxicilline-clavulaanzuur van 51/49 in 2019 naar een streefwaarde van 80/20 in 2024.
De verhouding tussen het gebruik van breedspectrum en smalspectrum antimicrobiële middelen, zoals gedefinieerd in ESAC-Net, is gedaald van 2,4 in 2012 tot 1,9 in 2021 (Figuur 3) ( ). De situatie in België is over het algemeen beter dan in Europa, waar de gemiddelde ratio is gestegen van 2,7 in 2012 tot 3,7 in 2021 (bereik van de landen in 2021: 0,1-20,7). De Belgische ratio is echter stabiel gebleven sinds 2019 en is hoger dan die in de meeste van onze buurlanden: in 2021, België = 1,9, Frankrijk = 1,0, Duitsland = 1,6, Luxemburg = 3,1, Nederland = 1,5.
Figuur 3 ● Verhouding tussen de consumptie (DID) van breedspectrumpenicillines, cefalosporines, macroliden (behalve erythromycine) en fluoroquinolones (J01(CR+DC+DD+(FA-FA01)+MA)) en de consumptie van smalspectrumpenicillines, cefalosporines en erythromycine (J01(CA+CE+CF+DB+FA01)) in de ambulante sector in België, Frankrijk, Duitsland, Luxemburg, Nederland en de EU/EER, 2012-2021.
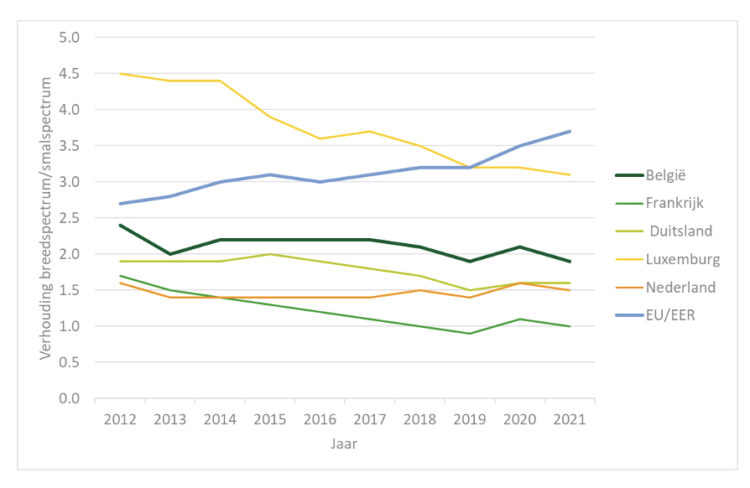
Bron: ESAC-Net. DID : DDD/1000 inwoners/dag ; EU/EER : Europese Unie/Europese Economische Ruimte.
Tussen 2012 (46/54) en 2019 (51/49) werd een geleidelijke verbetering voor de verhouding amoxicilline/amoxicilline-clavulaanzuur waargenomen; maar sinds 2019 is de indicator enigszins verslechterd, met waarden van 47/53 en 48/52 in respectievelijk 2020 en 2021. Er moet worden opgemerkt dat deze waarden nog steeds ver verwijderd zijn van de in het Belgische nationale actieplan vastgestelde en door de rode lijn in figuur 4 aangegeven streefverhouding van 80/20 (2,9).
Figuur 4 ● Verhouding consumptie (DID) van amoxicilline en amoxicilline-clavulaanzuur in de ambulante sector in België, 2012-2021.
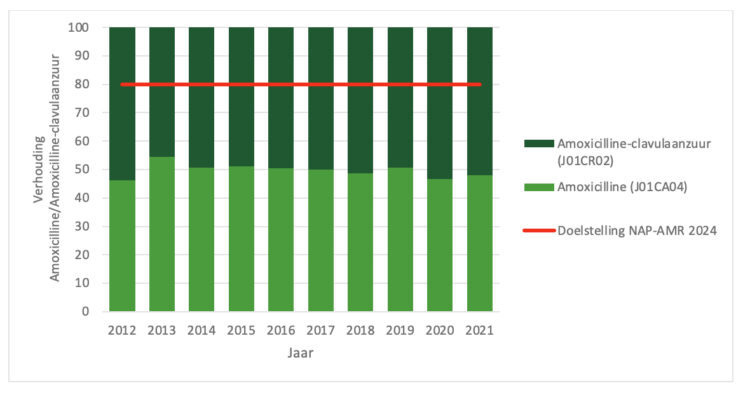
Bron: ESAC-Net. DID : DDD/1000 inwoners/dag; NAP-AMR: National Action Plan on Antimicrobial Resistance.
Ziekenhuissector
Doelstelling 1: Geleidelijke daling van het totale antibioticaverbruik, op te volgen naargelang de nationale en internationale epidemiologische context.
Uitgedrukt in DID daalt het verbruik van terugbetaalde antibiotica (J01) in de Belgische ziekenhuissector tussen 2012 en 2021 met 17,8% en ligt het sinds 2013 onder het Europese gemiddelde (Figuur 5). Deze daling betreft alle antibacteriële subgroepen, in het bijzonder quinolones (J01M) en penicillines (J01C), waarvan het verbruik tussen 2012 en 2021 met respectievelijk 43,4% en 18,6% is gedaald. De grootste jaarlijkse daling van het verbruik van terugbetaalde antibiotica (J01) deed zich voor tussen 2019 en 2020 (-11,8%), waarschijnlijk als gevolg van de COVID-19-pandemie. Daarna bleef het stabiel tussen 2020 en 2021 (1,40 DID). In 2021 was België de achtste Europese verbruiker in de ziekenhuissector, na Nederland (0,70 DID) en Luxemburg (1,28 DID) maar vóór Frankrijk (1,69 DID).
Figuur 5 ● Evolutie van het totale en per subgroep gebruik van systemische antibacteriële middelen (ATC-groep J01) uitgedrukt in DID in de Belgische ziekenhuissector (acute/categorische/psychiatrische ziekenhuizen) en Europese gemiddelde, 2012-2021.
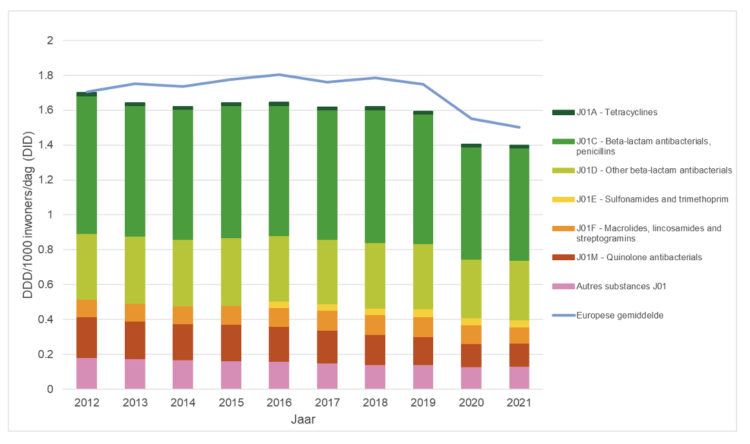
Bron: ESAC-Net. ATC : Anatomical, Therapeutic Chemical Classification ; DID : DDD/1000 inwoners/dag
Wanneer het antibioticagebruik (J01) in Belgische acute ziekenhuizen (N=104) wordt uitgedrukt in DDD/1000 ligdagen, wordt een significante stijging van 7,45% van het mediane verbruik waargenomen tussen 2012 en 2021 (respectievelijk 482,73 en 518,70 DDD/1000 ligdagen), met een opmerkelijke stijging van 4,8% tussen 2019 en 2020, gevolgd door een lichte daling tussen 2020 en 2021 (-2,2%) (Figuur 6A). Wanneer de mediane consumptie echter wordt uitgedrukt in DDD/1000 opnames, wordt een significante negatieve trend van -4,4% waargenomen tussen 2011 en 2020 (respectievelijk 3566,44 en 3409,72 DDD/1000 opnames), ondanks een stijging van 6,5% tussen 2019 en 2020 (Figuur 6B). Het antibioticagebruik varieert aanzienlijk tussen de verschillende soorten ziekenhuizen en afdelingen: het is significant hoger in tertiaire ziekenhuizen (N=6, mediaan: 613,24 DDD per 1000 ligdagen) en op intensive zorgen afdelingen (N=98, mediaan: 1102,35 DDD per 1000 ligdagen).
Figuur 6 ● Evolutie van het antibioticagebruik voor systemisch gebruik (J01) in Belgische acute ziekenhuizen (Z.), uitgedrukt als DDD/1000 ligdagen (links) en DDD/1000 opnames (rechts).
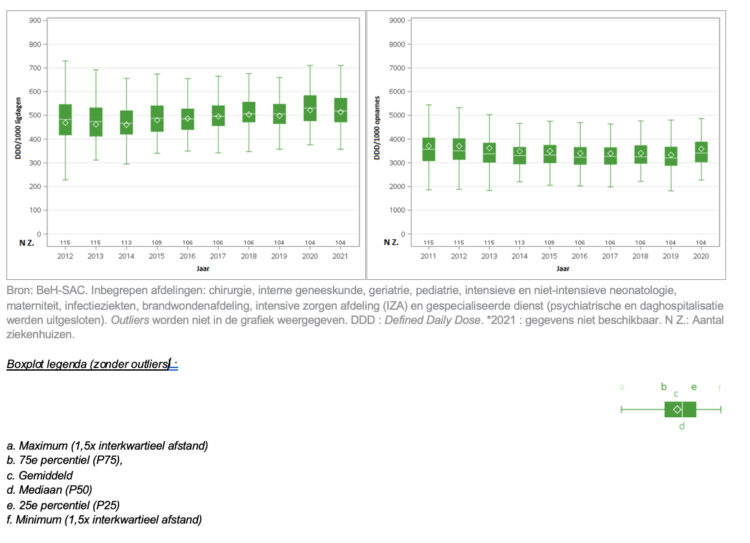
Doelstelling 2: Daling van het gebruik van breedspectrum antibiotica ten opzichte van het totale antibioticaverbruik en een toename van het voorschrijven van smalspectrum antibiotica met 3% (op basis van de AWaRe classificatie van de WHO).
In 2021 bedragen de mediane percentages van het gebruik van breedspectrumantibiotica ten opzichte van het totale antibioticagebruik (J01) respectievelijk 30,23%, 32,83% en 37,4% in primaire, secundaire en tertiaire acute ziekenhuizen. Hoewel er tussen 2012 en 2021 geen significante trend wordt vastgesteld in de evolutie van deze percentages, is er een zeer lichte stijging in primaire (+3,7%) en tertiaire (+4,1%) ziekenhuizen en een geringe daling in secundaire ziekenhuizen (-2,4%) (Figuur 7).
Figuur 7 ● Evolutie van het gebruik van breedspectrumantibiotica ten opzichte van het totale gebruik van systemische antibiotica (J01) in Belgische acute ziekenhuizen (Z.), per ziekenhuistype, 2012-2021.
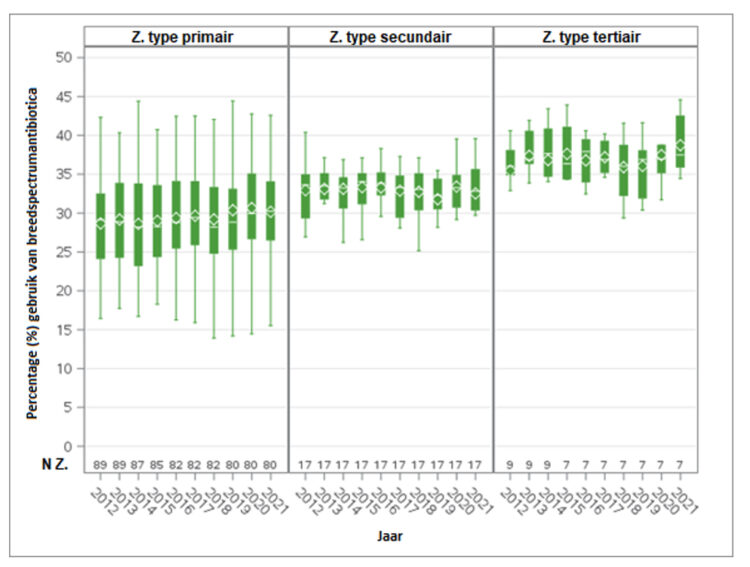 Bron: BeH-SAC. Inbegrepen afdelingen: chirurgie, interne geneeskunde, geriatrie, pediatrie, intensieve en niet-intensieve neonatologie, materniteit, infectieziekten, brandwondenafdeling, intensive zorgen afdeling (IZA) en gespecialiseerde dienst (psychiatrische en daghospitalisatie werden uitgesloten). Berekening van het gebruik van breedspectrumantibiotica: % Defined Daily Dose (DDD) J01(CR05+DD+DE+DF+DH+MA+XA+XB+XX08+XX09+XX11)/J01. Outliers worden niet in de grafiek weergegeven. Z.: Ziekenhuis. N Z.: Aantal ziekenhuizen.
Bron: BeH-SAC. Inbegrepen afdelingen: chirurgie, interne geneeskunde, geriatrie, pediatrie, intensieve en niet-intensieve neonatologie, materniteit, infectieziekten, brandwondenafdeling, intensive zorgen afdeling (IZA) en gespecialiseerde dienst (psychiatrische en daghospitalisatie werden uitgesloten). Berekening van het gebruik van breedspectrumantibiotica: % Defined Daily Dose (DDD) J01(CR05+DD+DE+DF+DH+MA+XA+XB+XX08+XX09+XX11)/J01. Outliers worden niet in de grafiek weergegeven. Z.: Ziekenhuis. N Z.: Aantal ziekenhuizen.
In 2017 heeft de WHO de AWaRe-tool ontwikkeld om de toenemende antimicrobiële resistentie in te dammen en het gebruik van antibiotica veiliger en effectiever te maken ( ). Deze tool deelt antibiotica in drie groepen in:
•Access : antibiotica waarvan de toegankelijkheid essentieel is
•Watch : antibiotica voor selectief gebruik
•Reserve : reserve antibiotica
De WHO heeft als doelstelling gesteld dat ten minste 60% van het totale antibioticagebruik op nationaal niveau Access-antibiotica moeten zijn ( ).
De laatste tien jaar werd in de Belgische ziekenhuizen voor acute zorg een significante trend naar minder frequent gebruik van Access-klasse antibiotica vastgesteld (van 57,7% in 2012 tot 55,0% in 2021) ten voordele van Watch en Reserve klasse antibiotica. De Belgische ziekenhuizen voor acute zorg zijn dus net verwijderd van de WHO-doelstelling van 60% (Figuur 8, rode lijn).
Figuur 8 ● Evolutie van het totale antibioticagebruik voor systemisch gebruik (J01) in Belgische acute ziekenhuizen volgens de WHO AWaRE classificatie, 2012-2021.
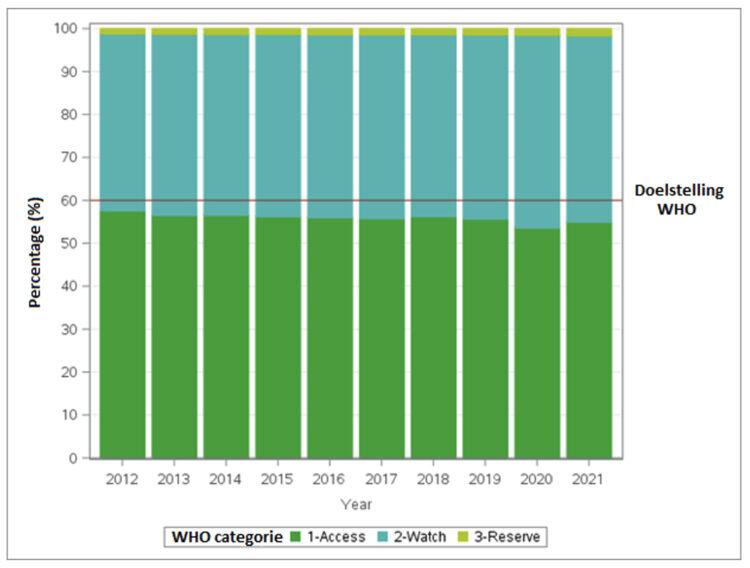
Bron: BeH-SAC. Inbegrepen afdelingen: chirurgie, interne geneeskunde, geriatrie, pediatrie, intensieve en niet-intensieve neonatologie, materniteit, infectieziekten, brandwondenafdeling, intensive zorgen afdeling (IZA) en gespecialiseerde dienst (psychiatrische en daghospitalisatie werden uitgesloten).
De meest gebruikte groep antibiotica in 2021 is de combinatie van penicilline met een beta-lactamase-inhibitor (J01CR), die al voor 32,9% uitmaakt van het totale aantal DDD voor J01, gevolgd door fluoroquinolones (J01MA) (9,5% van het totale aantal DDD voor J01) en eerste generatie cefalosporines (J01DB) (8,8% van het totale aantal DDD voor J01). Figuur 9 toont de top 10 van meest gebruikte producten in Belgische acute ziekenhuizen tussen 2017 en 2021. Van deze 10 producten behoren er vier tot de categorie Access (J01CR02, J01DB04, J01CF05 en J01CA04), vijf tot de categorie Watch (J01CR05, J01MA02, J01DD04, J01DC02 en J01DH02). Het laatste product is een schimmelwerend product (antimycoticum J02AC01).
Figuur 9 ● Evolutie van de 10 meest gebruikte antimicrobiële middelen (J01 en J02) in Belgische acute ziekenhuizen, uitgedrukt in DDD/1000 ligdagen, 2017-2021.
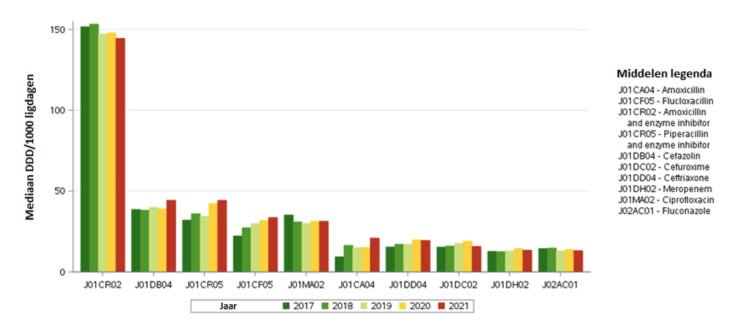
Bron: BeH-SAC. Inbegrepen afdelingen: chirurgie, interne geneeskunde, geriatrie, pediatrie, intensieve en niet-intensieve neonatologie, materniteit, infectieziekten, brandwondenafdeling, intensive zorgen afdeling (IZA) en gespecialiseerde dienst (psychiatrische en daghospitalisatie werden uitgesloten). DDD: Defined Daily Dose.
Conclusie
De afgelopen tien jaar werd gekenmerkt door een algemene daling van het terugbetaalde antibioticagebruik (J01) in de ambulante sector. Tussen 2019 en 2020 werd een bijzonder grote daling vastgesteld, als gevolg van de COVID-19-pandemie in dat jaar en de daarmee gepaard gaande veranderingen in besmettingsrisico, bedrijvigheid van gezondheidzorg en heur voorschrijfgedrag. Ondanks deze daling lijkt de consumptie van breedspectrumantibiotica te stabiliseren, terwijl er een duidelijke daling is in het gebruik van quinolones. In vergelijking met andere Europese landen is het antibioticagebruik in de ambulante sector hoog, en er zijn verdere inspanningen nodig om de NAP-AMR-doelstellingen in 2024 te halen.
Voor de ziekenhuissector tonen de contrasterende resultaten bij gebruik van verschillende noemers het belang aan van verschillende maatstaven in aanmerking te nemen bij de beoordeling van het antimicrobiële verbruik in deze sector. De noemers moeten relevant zijn voor de surveillancepopulatie en alleen ziekenhuispatiënten vertegenwoordigen.
Algemeen werd een significante toename van het antibioticagebruik in ziekenhuizen voor acute zorg vastgesteld in DDD/1000 ligdagen en een significante afname in DDD/1000 opnames. De toename van DDD/1000 ligdagen kan waarschijnlijk worden verklaard door de evolutie naar kortere ziekenhuisverblijven met een intensievere antibioticabehandeling. De laatste jaren is een frequenter gebruik van breedspectrumantibiotica waargenomen, hoewel er geen significante trend is vastgesteld.
Antimicrobial stewardship blijft een van de belangrijkste strategieën om antimicrobiële resistentie te bestrijden. Daarom moet worden gepleit voor een verantwoord gebruik van antimicrobiële middelen. Meer gedetailleerde surveillance, met inbegrip van indicaties op voorschrift, zou een meer gerichte feedback mogelijk maken.
Referenties
(1) European Commission. European One Health Action Plan against Antimicrobial Resistance (AMR). Juin 2017. Beschikbaar op : https://health.ec.europa.eu/system/files/2020-01/amr_2017_action-plan_0.pdf
(2) FOD Volksgezondheid, Veiligheid van de Voedselketen en Leefmilieu. Belgisch Nationaal Actieplan « One Health » voor de bestrijding van antimicrobiële resistentie 2020-2024. Beschikbaar op : https://www.health.belgium.be/sites/default/files/uploads/fields/fpshealth_theme_file/nl-amr_one_health_national_plan_final.pdf
(3) European Center for Disease Prevention and Control – TESSy – ESAC-Net. Antimicrobial consumption (AMC) reporting protocol 2022. Beschikbaar op : https://www.ecdc.europa.eu/sites/default/files/documents/ESACNet_protocol_2022.pdf
(4) Healhstat.be. Your portal to Belgian health statistics. Beschikbaar op : https://www.healthstat.be
(5) World Health Organization (WHO). Collaborating Centre for Drugs Statistics Methodology. Classification ATC. Beschikbaar op : https://www.whocc.no/atc_ddd_index/
(6) Vermeulen H, Coenen S, Hens N, Bruyndonckx R. Impact of changing reimbursement criteria on the use of fluoroquinolones in Belgium. J Antimicrob Chemother. 2021 Oct 1;76(10):2725–32. Beschikbaar op : https://doi.org/10.1093/jac/dkab255
(7) Belgisch Staatsblad – Moniteur Belge, “Koninklijk besluit tot vaststelling van de procedures, termijnen en voorwaarden inzake de tegemoetkoming van de verplichte verzekering voor geneeskundige verzorging en uitkeringen in de kosten van farmaceutische specialiteiten – Arreté Royal du 1er février 2018 fixant les procédures, délais et conditions en matière d’intervention de l’assurance obligatoire soins de santé et indemnités dans le coût des spécialités pharmaceutiques.” Beschikbaar op : https://www.inami.fgov.be/SiteCollectionDocuments/specialites_pharmaceutiques_AR_20180201.pdf
(8) BeH-SAC – Belgian Hospitals – Surveillance of Antimicrobial Consumption. Sciensano web page. Beschikbaar op : https://www.sciensano.be/en/projects/belgian-hospitals-surveillance-antimicrobial-consumption
(9) European Centre for Disease Prevention and Control. Antimicrobial consumption dashboard (ESAC-Net). Latest surveillance data on antimicrobial consumption. Beschikbaar op : https://qap.ecdc.europa.eu/public/extensions/AMC2_Dashboard/AMC2_Dashboard.html#eu-consumption-tab
(10) Balligand E, Costers M, Gastel EV. Belgian Antibiotic Policy Coordination Committee 2014-2019. Beschikbaar op : https://beratungsgremien.gesundheit.belgien.be/sites/default/files/documents/policy_plan_2014-2019_ex-summary_deutsch.pdf
(11) ECDC, Antimicrobial consumption in the EU/EEA (ESAC-Net) Annual Epidemiological Report for 2021. Beschikbaar op : https://www.ecdc.europa.eu/sites/default/files/documents/ESAC-Net_AER_2021_final-rev.pdf
(12) World Health Organization (WHO). 2021 AWaRe classification. WHO access, watch, reserve, classification of antibiotics for evaluation and monitoring of use. Beschikbaar op : https://www.who.int/publications/i/item/2021-aware-classification
(13) World Health Organization (WHO). Thirteenth General Programme of Work (GPW13): metadata for impact measurement indicators. Geneva: WHO; 2020. Beschikbaar op : https://www.who.int/about/what-we-do/thirteenth-general-programme-of-work-2019—2023