1. Inleiding
Het rotavirus is in België lang de voornaamste oorzaak geweest van virale gastro-enteritis bij kinderen jonger dan 5 jaar, wat soms tot ziekenhuisepidemieën leidde. Het klinisch beeld wordt meestal gekenmerkt door een waterige diarree gedurende 3 à 7 dagen, die gepaard gaat met een risico op dehydratatie, ionische onbalans en bijzonder ernstige metabole acidose bij kinderen onder de 2 jaar. Op neonatologie zijn de symptomen meer variabel en atypisch (eerder slijmerige en hemorragische stoelgang, opgeblazen gevoel in de buik, hemodynamische instabiliteit, bradycardie, apneu …). Mogelijks bestaat er een verband met necrotiserende enterocolitis maar daar bestaat controverse over.1-3 Asymptomatisch dragerschap is op alle leeftijden mogelijk.
Het virus wordt rechtstreeks of onrechtstreeks via fecaal-orale weg of het braaksel van de patiënt overgedragen. De besmettelijkheid is maximaal tijdens een symptomatische periode maar kan, op geringer niveau weliswaar, tot 10 dagen na het einde van de diarree blijven duren. De gebruikelijke incubatieperiode bedraagt minder dan 48 uur.
De Europese commercialisatie in 2006 door GSK van Rotarix®, een monovalent oraal levend verzwakt vaccin, heeft de epidemiologie van dit virus danig gewijzigd. Na dit eerste vaccin volgde in 2007 een tweede oraal pentavalent vaccin, RotaTeq® (Sanofi Pasteur MSD). België was samen met Oostenrijk, Luxemburg en Finland een van de eerste West-Europese landen die het in hun vaccinatieprogramma hebben opgenomen. De eerste dosis kan vanaf 6 weken worden toegediend en de tussentijd tussen twee dosissen bedraagt minstens 4 weken. Van Rotarix® zijn twee dosissen nodig, van RotaTeq® drie.
De impact van deze vaccinatie is onlangs geëvalueerd op basis van gegevens die tussen 2005 en 2013 in 11 Belgische ziekenhuizen zijn ingezameld.4 Zo kon tussen 2006 en 2012 een daling van 70 à 80% van het absolute aantal positieve diagnostische tests worden geobjectiveerd. De geringere incidentie van deze pathologie onder de volledige populatie zorgt onrechtstreeks voor een betere bescherming van zuigelingen jonger dan 2 maanden die nog niet kunnen worden ingeënt. In deze leeftijdsgroep wordt de daling van het aantal gevallen sinds de invoering van de vaccinatie, op 50% geschat.
2. Standpunt van de bioloog6
De rotavirus-diagnose wordt meestal gesteld door het rechtstreeks opsporen van de virusbestanddelen op een stoelgangstaal. Ook op andere biologische staalnamen (bloed, cerebrospinaal vocht) kan een bijkomende analyse gebeuren maar dat behoort nog steeds tot het stadium van het experimenteel onderzoek.
Voor dat soort opsporing worden meestal immuno-chromatografische testen gebruikt, die op hun beurt gebruik maken van antilichamen gericht tegen het virale eiwit VP6. Deze eenvoudige en snelle techniek levert uitstekende theoretische analytische prestaties op (sensitiviteit 80% en specificiteit 100% in vergelijking met PCR) en heeft bovendien het voordeel dat verschillende enterische virussen tegelijkertijd kunnen worden opgespoord (rotavirus, adenovirus, minder vaak norovirus).
De diagnose kan ook worden gesteld met een immuno-enzymatische test (ELISA), die ongeveer net zo goed is als de immuno-chromatografische test. Deze techniek is meer geschikt voor grote analysereeksen dan voor routinetesten in perifere laboratoria.
Tenslotte is ook het opsporen van het viraal genoom via de RT-PCR-test mogelijk. De prestaties zijn beter dan bij de twee andere technieken. De test is echter te duur om die routinegewijs uit te voeren.
Een positief resultaat wijst op de aanwezigheid van het rotavirus in de stoelgang maar sluit een mogelijke co-infectie door andere enteropathogenen (10% van de gevallen) niet uit. Wanneer in het spijsverteringsstelsel geen symptomen aanwezig zijn, wijst een positieve test gewoon op asymptomatisch dragerschap.
3. Standpunt van de hygiënist7
Het zeer besmettelijke rotavirus wordt door rechtstreeks of onrechtstreeks contact via de stoelgang of het braaksel van de patiënt overgedragen. Belangrijk is dus om de voorzorgsmaatregelen te versterken en extra maatregelen te treffen tegen de via contact overgedragen kiemen.
Dit vereist een grondige handhygiëne inclusief aanwezigheid van een handalcohol in de kamer, het dragen van handschoenen en van een schort voor eenmalig gebruik, verblijf in een 1-persoonskamer, dagelijkse schoonmaak van de kamer met een detergent-ontsmettingsmiddel van het type Incidin® (ontsmettingsmiddel zonder aldehyden, op basis van 1-propanol en 2-propanol) en de aanwezigheid in de kamer van verzorgingsmateriaal dat enkel voor de patiënt is bestemd (bloeddrukmeter, personenweegschaal, perfusiehouder, stethoscoop, …) en dat vóór gebruik bij een volgende patiënt, grondig zal worden schoongemaakt en ontsmet met Incidin®. Het virus is overigens ook gevoelig voor ethanol 95%, formol 2%, natriumhypochloriet 2% en een combinatie van quaternair ammonium en alcohol, maar dan wel na een verlengde blootstelling.
Deze maatregelen moeten worden toegepast zolang de symptomen zich bij de patiënt voordoen, gedurende zo’n 7 dagen dus.
Na het vertrek van de patiënt moet het onderhoudspersoneel de kamer schoonmaken met een detergent en daarna met bleekwater met een concentratie van 1000 ppm of 2%.
4. Afzonderlijke gevallen
De dienst neonatologie van de Cliniques Universitaires Saint-Luc telt 28 bedden verdeeld over 5 zalen en behandelt jaarlijks zo’n 300 à 350 kinderen. Op deze dienst heeft er zich in september 2014 een ernstige K. pneumoniae OXA-48 epidemie voorgedaan, waarna bij het personeel een sterke bewustwording is gegroeid rond het belang van regels ter preventie van infectieoverdracht.
In februari 2015 heeft de dienst, na een positieve rotavirustest die was voorgeschreven omwille van een milde temperatuursverhoging, contact opgenomen met het team ziekenhuishygiëne. Aangezien dit indexgeval niet met diarree gepaard ging, werd isolering niet aanbevolen. Wel werden maatregelen aangeraden inzake handhygiëne en het dragen van handschoenen bij de behandelingen. Alle andere patiënten op de eenheid hadden een negatief testresultaat.
Twaalf dagen later werd de dienst hygiëne opnieuw gecontacteerd voor een tweede positief geval. Het ging hier om een meisje van 5 dagen oud, dat uit een andere instelling was overgebracht, waar ze reeds positief op het rotavirus had getest. Er werd beslist het meisje te isoleren na vaststelling van weliswaar lichte spijsverteringssymptomen.
Drie dagen later werd een derde asymptomatische patiënt, die vooraf negatief had getest, ook positief bevonden. Het klinische beeld dat aan het voorschrijven van die test voorafging kon niet worden verduidelijkt. Aangezien het hier ging om een zorginfectie, verworven op de betrokken eenheid, werd de patiënt geïsoleerd met extra contactvoorzorgsmaatregelen (handschoenen, schort). Daarop werd beslist om alle niet-gedocumenteerde positieve patiënten (15) in de eenheid te screenen. Geen enkele vertoonde symptomen maar door de kwetsbaarheid van de aanwezige patiënten en de documentatie van gevallen van necrotiserende enterocolitis geassocieerd met het rotavirus, zag het team zich verplicht om maximale beschermingsmaatregelen te treffen. De epidemische drempel werd vastgelegd op 2 verworven gevallen.
Tien stoelgangstalen werden de dag zelf naar het laboratorium opgestuurd en drie daarvan testten positief op het rotavirus. De crisiscel werd geactiveerd, de positieve patiënten geïsoleerd en de kinderen en het verzorgend personeel gecohorteerd.
Ondanks die strenge maatregelen kwamen nieuwe gevallen van asymptomatisch dragerschap aan het licht. Bepaalde positieve patiënten werden later negatief getest, om enkele dagen daarna opnieuw positief te testen.
Door de niet-reproduceerbaarheid van de resultaten en het gebrek aan inzicht in de oorzaken van de oprukkende epidemie, werd de betrouwbaarheid van de gebruikte diagnosetest in vraag gesteld. Het laboratorium gebruikte al jaren de immunoenzymatische test (Elisa) Premier Rotaclone® van de firma Meridian Bioscience Inc. De analytische prestaties ervan werden zowel door de firma als door de literatuur als meer dan bevredigend bestempeld (Gevoeligheid = 81-100%, specificiteit = 92-100%).8-10 Deze test wordt trouwens ook gebruikt door het Belgisch Nationaal Referentiecentrum (NRC) in het UZ Leuven. Elke dag voert een ervaren en goed opgeleid team van technologen de test uit. De kit werd bewaard in een koelkast, waarvan de temperatuur wordt opgevolgd, zoals door de procedure is aanbevolen, en bij elke nieuwe analysereeks controleert men de vervaldatum. De resultaten werden weergegeven door visuele waarneming, zoals door de firma aanbevolen: de putjes met een fellere blauwe kleur dan de negatieve controle werden als positief beschouwd. Tot dan toe had er zich met de stalen die afkomstig waren van de afdeling neonatologie (+/- 35-40 geteste stalen per jaar) geen enkel probleem voorgedaan.
De positieve stoelgang (1/patiënt), die aan 4°C werd bewaard, werd vervolgens naar het NCR (UZ Leuven) opgestuurd voor het opsporen van het rotavirus via RT-PCR. Alle stalen bleken opnieuw negatief. Het ging hier dus om een pseudo-epidemie, die uiteindelijk een maand zou duren.
5. Discussie
Het rotavirus is een goed beschreven etiologie van een gastro-enteritis ziekenhuisepidemie. De incidentie van dat soort epidemieën is sinds de invoering van de inentingen gevoelig gedaald, toch blijven de niet-gevaccineerde zuigelingen nog steeds een risicogroep. Het is een moeilijk te diagnosticeren populatie. Soms hebben ze geen of zeer atypische symptomen en het aantal in de stoelgang uitgescheiden virusdeeltjes kan veel geringer zijn dan bij de rest van de populatie. Toch zorgen de door bepaalde auteurs beschreven associaties tussen het rotavirus en aandoeningen die de levensverwachting van die pasgeborenen in gevaar brengen (necrotiserende enterocolitis, secundaire bloedbaaninfecties, …) ervoor dat pediaters bijzonder waakzaam zijn voor deze ziekteverwekker.
Het laboratorium gebruikt al jaren de immunoenzymatische test (Elisa) Premier Rotaclone®, zonder dat er ooit maar enig incident te betreuren viel. Ook al wijst de firma op mogelijke vals negatieven bij neonatale stalen en ook al kan het aantal in de stoelgang uitgescheiden virusdeeltjes bij pasgeborenen zeer gering zijn, toch maakt ze geen melding van vals positieven in die leeftijdscategorie.8
Bij het nalezen van de te volgen procedure bleek dat twee analytische stappen voor verbetering vatbaar waren :
• enerzijds verdunde het technische team de stoelgang van de patiënten vóór analyse te weinig. De stoelgang werd verdund aan 1/10 in PBS (fosfaat gebufferde zoutoplossing zonder bewaarmiddel) en niet aan 1/30 in het door de firma geleverde verdunningsmiddel (gebufferde zoutoplossing met 0.02% thimerosal). Deze fout werd intussen rechtgezet.
• Anderzijds werden de kleurwijzigingen afgelezen met het blote oog en niet met behulp van een spectrofotometer, waardoor de test enigszins subjectief was. Dit sloot evenwel aan bij de aanbevelingen van de firma, die geen voorkeur voor de ene of de andere methode uitsprak. Het aflezen van de positieve tests van deze pseudo-epidemie met behulp van een spectrofotometer heeft twijfelachtige resultaten gerapporteerd (Absorptie op 450 nm na van de positiviteitsdrempel die door de firma is vastgelegd op 0.150), die als «zwak positief» werden bestempeld. Sindsdien is het niet langer toegelaten om twijfelachtige stalen of stalen die afkomstig zijn van de dienst neonatologie met het blote oog af te lezen.
Na die aanpassingen komt het aantal «zwak positieve» stoelgangstalen nog amper voor, zonder evenwel volledig te verdwijnen in de dagen na de identificatie van de pseudo-epidemie. Achteraf werd geen enkel twijfelachtig of zwak positief geval meer gemeld.
Een dienst neonatologie in Taiwan heeft in 2014 melding gemaakt van een gelijkaardige ervaring.11 In 2011 testten 7 jonge patiënten met abdominale symptomen over een periode van 2 maanden positief, resultaten die achteraf via RT-PCR zouden worden ontkracht. Het labo gebruikte toen een andere immunoenzymatische testkit dan die die in de Cliniques Universitaires Saint-Luc werd gebruikt (RIDASCREEN Rotavirus, R-Biopharm AG, Darmstadt, Germany). Het team had geen verklaring voor die vals positieve resultaten maar nadat de kit voor een andere versie was ingeruild, was de situatie uitgeklaard.
Ook andere gelijkaardige vals positieve resultaten en pseudo-epidemieën zijn in neonatologie beschreven voor andere pathogene virussen van het spijsverteringssysteem (tabel 1).12-16 De historiek van de pseudo-epidemieën is steeds dezelfde: een immunoenzymatische of immunochromatografische test op een stoelgangstaal wordt voorgeschreven om atypische symptomen te documenteren en wordt achteraf weer positief. In een volgende fase wordt de dienst gescreend, ongeacht of de patiënten al dan niet symptomen vertonen. Door de incoherente resultaten of de evolutie worden de stoelgangstalen voor bevestiging via PCR opgestuurd, om uiteindelijk opnieuw negatief te testen. De gebruikte tests zijn niet altijd dezelfde en worden niet door dezelfde firma gecommercialiseerd.
Over de oorzaak van die vals positieve resultaten bij pasgeborenen bestaat nog steeds onduidelijkheid. We mogen redelijkerwijs uitgaan van interferenties tussen bepaalde elementen in de stoelgang van pasgeborenen en de gecommercialiseerde immunologische testen. Welke factor(en) precies de oorzaak van die interferenties is/zijn blijft een vraagteken. Mogelijk zijn die elementen enkel episodisch of epidemisch aanwezig, wat het bestaan van vals positieve «clusters» kan verklaren. Zo heeft de firma Fisher Scientific bijvoorbeeld de aanwezigheid van een grote hoeveelheid Staphylococcus aureus A eiwitten in de stalen aangeduid als mogelijke oorzaak voor de vals positieve resultaten op de immunochromatografische testen voor de opsporing van het adenovirus. Er was wel niet bij vermeld op welk type staal deze interferentie was vastgesteld. 17
In ons geval heeft het probleem deels te maken met de foute verdunning van de stoelgangstaal maar aangezien er zich jarenlang geen dergelijk probleem heeft voorgedaan, moet er wel een bijkomende, microbiologische, medicamenteuze of andere factor bestaan die voor interferenties met de test zorgt. De extra verdunning van de stoelgangstaal zorgt dan mogelijks voor een extra verdunning van deze factor, die dan niet langer in voldoende aantal aanwezig zou zijn om de interferentie zichtbaar te maken.
Tabel 1: Kenmerken van verschillende pseudo-epidemieën met enteropathogene virussen die op de diensten neonatologie zijn gemeld
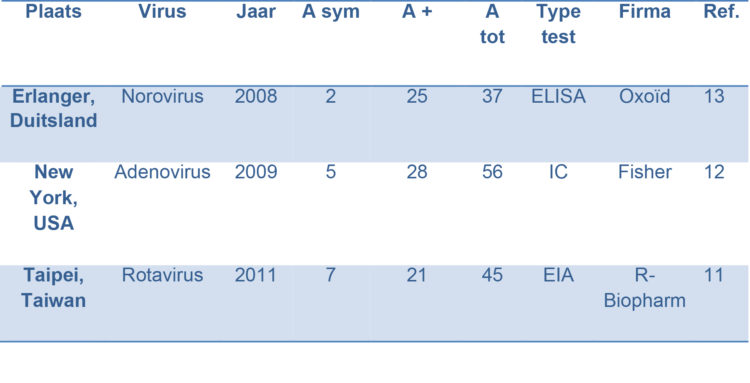
A sym = Aantal patiënten die lichte of duidelijke spijsverteringssymptomen vertonen.
A + = Aantal positief geteste patiënten
A tot = Totale aantal geteste patiënten.
IC = Immunochromatografie.
Een pseudo-epidemie kan worden gedefinieerd als een valse cluster van echte infecties of een echt cluster van valse infecties. 18-19
In de eerste situatie worden de effectief besmette patiënten verkeerdelijk verdacht als een epidemiegeval. Dit kan bijvoorbeeld het geval zijn wanneer een labo de diagnosemethode voor een pathologie wijzigt: indien de nieuw gebruikte test gevoeliger is dan de vorige, kan een valse stijging van de incidentie van de pathologie worden geobjectiveerd en verkeerdelijk als een epidemie worden geïnterpreteerd.
In het tweede geval gaat het om een foute diagnose die een enigszins met elkaar verbonden populatie treft, via de lokalisatie van de patiënten, hun leeftijdsgroep, of op een andere manier. Dit is mogelijk wanneer een test op een verkeerde manier wordt voorgeschreven en/of na een probleem in het labo (foute behandeling, besmettingen, vervallen reagentia,…).
Deze pseudo-epidemieën zijn zowel op menselijk als financieel vlak kostelijk, en zeker wanneer ze het gevolg zijn van een foute diagnose. Ze zorgen voor extra werk voor het verzorgingsteam, een foute behandeling van de patiënten, nodeloze stress voor iedereen en een verlies van vertrouwen in het labo wanneer dat een rol speelt bij de genese.20 De identificatie ervan is dus essentieel. Daarom is het belangrijk bij elke epidemie rekening te houden met deze mogelijkheid, vooral wanneer er onduidelijkheid bestaat (tegenstrijdige resultaten, atypische kiemen, klinisch-biologische discrepanties, …), en een pluri-disciplinaire discussie aan te gaan.
6. Conclusie
Pseudo-epidemieën zijn ongewenste en dure gebeurtenissen die een negatieve impact hebben op een kwaliteitsvolle opvang van de patiënten en op het vertrouwen tussen de verschillende actoren binnen de medische sector. Bij een epidemie moet in geval van incoherenties rekening worden gehouden met deze mogelijkheid. Het verzorgingsteam, het team ziekenhuishygiëne en het laboratorium kunnen dat best samen bespreken.
Blijkbaar doen er zich onopgehelderde interferenties voor wanneer immuno-enzymatische of immuno-chromatografische testen worden gebruikt op de stoelgang van patiënten die op neonatologie zijn gehospitaliseerd. Deze interferenties kunnen verantwoordelijk zijn voor vals positieve resultaten of pseudo-epidemieën. Om die te vermijden is het belangrijk inzicht te hebben in de door het labo uitgevoerde testen, en erop toe te zien dat die maar in beperkte mate en binnen een goed afgebakend symptomatologisch kader worden voorgeschreven.
7. Referenties
1. Haffejee IE. Neonatal rotavirus infection. Rev Infect Dis 1991 ; 13 :957-62
2. Sharma R et al. Clinical manifestations of rotavirus infection in the neonatal intensive care unit. Pediatr Infect Dis J 2002 Dec;21(12):1099-105.
3. Tai IC et al. Clinical manifestations of a cluster of rotavirus infection in young infants hospitalized in neonatal care units. J Microbiol Immunol Infect. 2012 Feb;45(1):15-21
4. Standaert B. et al Medium to long-term impact of rotavirus vaccination on hospital care in Belgium : a 7-yeat follow-up of the Rotavirus Belgium Impact Study (RotaBIS) Infect Dis Ther 2015 Dec 31 (epub)
5. Avis du Conseil Supérieur de la Santé n°9295 et 8883 :
Analyse du risque bénéfice de la vaccination contre le rotavirus en Belgique (réaction suite à une prise de position française récente). Juillet 2015.
6. REMIC Référentiel en microbiologie médicale 5ème édition 2015 (SFM, SFP, SFMM)
7. The Sanford Guide to Antimicrobial Therapy 2012-2013: 23ème edition Belgique/Luxembourg.
8. Meridian Bioscience, Inc. Premier® Rotaclone® product insert. Cincinnati, Ohia, USA. Révision: 01/2015.
9. Gautam R. et al. Comparison of Premier™ Rotaclone®, ProSpecT ™, and RIDASCREEN ® rotavirus enzyme immunoassay kits for detection of rotavirus antigen in stool specimens. J Clin Virol. 2013 Sep ; 58 (1) : 292-294
10. Evaluation of seven commercial assays for detecting group A rotavirus antigen.PHLS East Virology Advisory Committee, internal document.
11. Tan BF et al. Pseudo-outbreak of rotavirus infection in a neonatal intensive care unit. J Microbiol Immunol Infect. 2014 Nov 22.
12. Faden H et al. Pseudo-outbreak of adenovirus infection in a neonatal intensive care unit due to a false –positive antigen detection test. J Clin Microbiol. 2010 Nov;48(11):4251-2
13. Köhler H, Jüngert J and Korn K : Norovirus pseudo-outbreak in a neonatal intensive care unit. J Pediatr Gastroenterol Nutr 2008 Apr ; 46(4) :471-2
14. Terashita Gastelum D et al. Pseudo-outbreak of respiratory syncytial virus infection in a neonatal intensive care unit due to cross-reactivity of surfactant and a rapid immunoassay. Infect Control Hosp Epidemiol. 2009 Sep;30(9):890-2.
15. Rand KH, Houck HJ, Swingle HM. Rotazyme assay in neonates without diarrhea. Results of screening survey and preliminary analysis of false positive specimens. Am J Clin Pathol 1985 Dec; 84(6):748-51.
16. Niizuma T et al. False positive of an immunochromatography kit for detection of norovirus in neonatal feces. J Infect Chemother 2013 Feb ; 19(1) : 171-3.
17. Fischer Scientific Company. Sure-Vue™ Adeno Test Kit product insert. Pittsburgh, Pennsylvania, USA. Révision : 2002.
18. Curran ET. Outbreak Column 7: Pseudo-outbreaks part 1. Journal of infection prevention 2013 March ; 14(2) : 69-74
19. Curran ET. Outbreak Column 7: Pseudo-outbreaks part 2. Journal of infection prevention 2013 May ; 14(3) : 108-113
20. Shears P. Pseudo-Outbreaks. Lancet 1996 Jan ;347:138