De studie van F. Van Laer et coll. die in dit nummer van NOSO-Info aan bod komt is origineel en vernieuwend (ongetwijfeld een première voor België!). Om te beginnen heeft de studie de verdienste een fraai staaltje van multidisciplinaire samenwerking tussen het laboratorium voor microbiologie, het team van ziekenhuishygiënisten en de zorgteams op het terrein in de kijker te plaatsen.
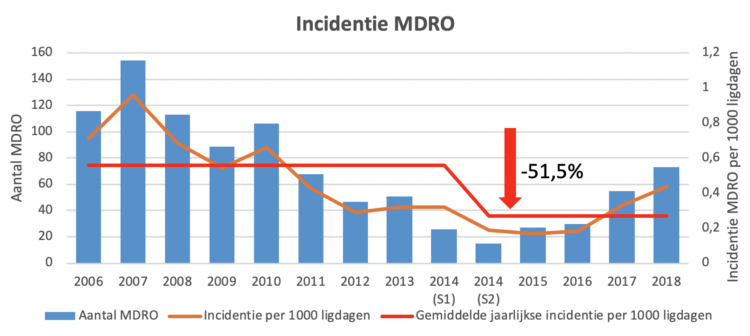
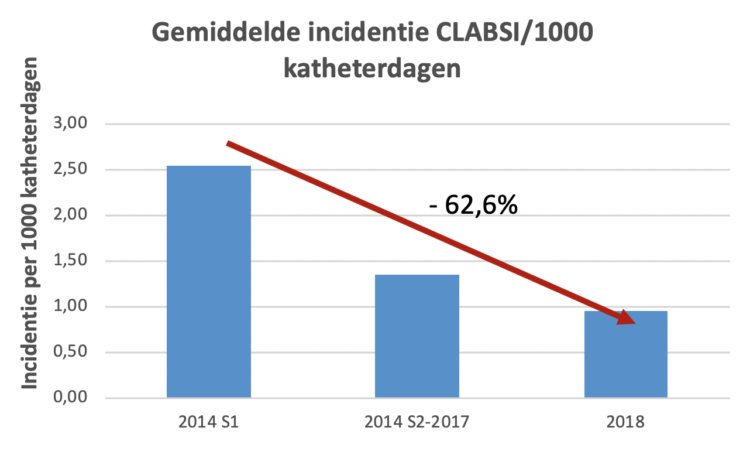
De evaluatie heeft betrekking op een periode van meerdere jaren en de resultaten doen een zeer gunstig effect vermoeden van het dagelijks wassen met 2%-chloorhexidine-geïmpregneerde washandjes op de incidentie van bepaalde ziekenhuisinfecties en op de ecologie van antimicrobiële resistentie bij patiënten op de dienst intensieve zorgen. De waargenomen dalingen met 50% van de incidentie van centrale kathetergerelateerde septicemieën (CLABSI) en multiresistente kiemen (MDRO) na interventie, ten opzichte van de uitgangssituatie zijn een spectaculair resultaat. Maar zoals de auteurs zelf aangeven, kan er op basis van deze gegevens geen direct causaal verband worden aangetoond tussen de invoering van wasbeurten met chloorhexidine en de verbetering van de twee bovengenoemde indicatoren.
Ondanks de talrijke studies die al meer dan 10 jaar in de internationale literatuur worden gepubliceerd, wordt het «wassen zonder water» nog te weinig toegepast, rekening houdend met de hardnekkige twijfel over de voordelen ervan. We moeten echter vaststellen dat deze praktijk nog niet echt is geaccepteerd en dat veel zorgverleners er nog steeds systematisch voor kiezen om, patiënten met zeep en water te wassen. Bovendien is er nog zeer weinig bekend over de risico’s van ongewenste effecten door het grootschalige gebruik van chloorhexidine (huidreacties, veranderingen in de samenstelling van de huidflora en de slijmvliezen, ontwikkelen van bacteriële resistentie tegen antiseptica maar ook tegen antibiotica, …).
Hoewel chloorhexidine een veelgebruikt en goedkoop ontsmettingsmiddel is dat over het algemeen goed wordt verdragen, moeten de extra kosten van eenmalig te gebruiken chloorhexidine-geïmpregneerde washandjes, de noodzakelijke aankoop van extra apparatuur voor deze praktijk (zoals een verwarmer) en de verschillende in de handel verkrijgbare vormen van voorverpakte verpakkingen, ook in aanmerking worden genomen vooraleer wordt beslist ze in zorgprotocollen op te nemen en is ook op lokaal niveau om een grondige evaluatie nodig.
Onderstaande bedenkingen moeten de lacunes en de vele onduidelijkheden belichten, die nog moeten worden aangepakt vooraleer deze zorgpraktijk algemeen kan worden aanbevolen.
Aangezien de onderlinge verschillen tussen de gepubliceerde studies groot zijn, is het niet makkelijk om ze te vergelijken en eenduidige conclusies te trekken in termen van effectiviteit en kosten-batenverhouding. Deze verschillen hebben betrekking op zowel de klinische contexten (lokale vs. multicentrische studie), de specialismen (medische, chirurgische, gemengde eenheden,…,), de patiëntenprofielen (case-mix), of doelgerichte parameters die van belang zijn (bijv. nosocomiale septicemieën van welke oorsprong dan ook (HA-BSI), centraal-veneuze kathetergerelateerde septicemieën (CLABSI), ventilatorgeassocieerde pneumonieën bij geïntubeerde patiënten (VAP), urineweginfecties (CAUTI), …).
Het aantal baseline infecties (vóór het gebruik van chloorhexidine), de duur van de studies (van enkele weken tot enkele jaren) en het aantal opgetreden gebeurtenissen die van belang zijn, lopen ook sterk uiteen. Zeer vaak ontbreekt het aantal hospitalisatiedagen met risico op infectie. Tot slot wordt amper de impact van een wasbeurt met chloorhexidine op de duur van het verblijf op intensieve zorgen, op de totale duur van het ziekenhuisverblijf of op de mortaliteit van de patiënten tijdens de hospitalisatie gemeten.
Ook de opzet van de gepubliceerde studies verschilt sterk en er zijn heel wat (niet-)publicatiebiassen. Meta-analyses omvatten alleen vergelijkende gerandomiseerde en gecontroleerde klinische proeven (randomized controlled trials) of cluster gerandomiseerde proeven (cross-over, cluster randomized trials). Observationele studies zonder controlegroep worden dan weer niet opgenomen omdat ze te heterogeen zijn en aan vele variaties onderhevig zijn. Meestal gaat het echter om ‘voor en na’-studies zoals die van het UZA, waaruit een gunstig effect blijkt door het gebruik van chloorhexidine-geïmpregneerde washandjes op het verminderen van bepaalde ziekenhuisinfecties (HA-BSI, CLABSI). Uit gerandomiseerde klinische studies daarentegen blijkt echter zelden een significant effect, wanneer ze apart worden beschouwd, omdat ze doorgaans niet groot genoeg zijn en het statistisch onderscheidingsvermogen onvoldoende is.
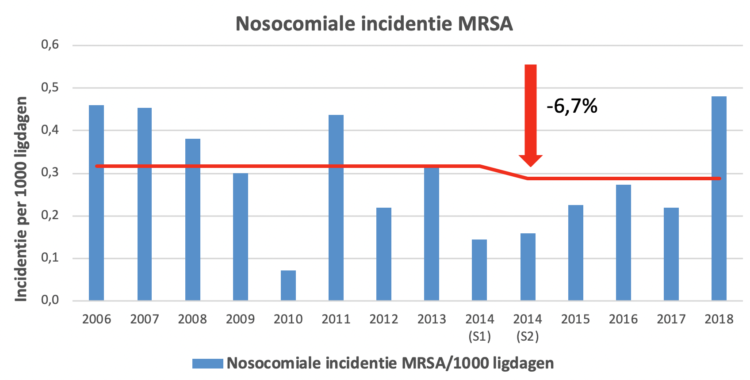
Voor multiresistente kiemen werden MRSA, VRE en ESBL-producerende enterobacteriën (soms Clostridium difficile) prioritair onderzocht. De studies richtten zich daarentegen amper op CPE (carbapenemaseproducerende enterobacteriën) en andere multiresistente Gram-negatieve bacteriën zoals Pseudomonas aeruginosa of Acinetobacter spp. Dit is nogal verrassend aangezien ze vaak een rol spelen bij het uitbreken van ziekenhuisinfecties op de intensieve zorgeenheden en gelet op de vele bronnen en reservoirs (vooral in het water) die ermee geassocieerd worden.
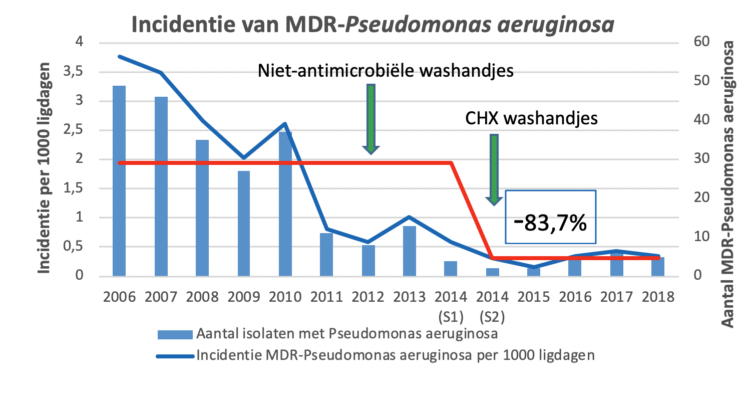
De significante daling van het aantal multiresistente P. aeruginosa die in de UZA-studie is vastgesteld, kan de hypothese ondersteunen dat het «wassen zonder water» met chloorhexidine-geïmpregneerde washandjes het risico op het verwerven van deze bacteriën beperkt, omdat de patiënt bij de dagelijkse wasbeurten minder contact met leidingwater zou hebben. Zeer waarschijnlijk is het ook zo dat er in de loop van de tijd ook andere variabelen (die niet in de studie zijn beoordeeld) zijn gewijzigd (zoals de systematische screening bij opname in de eenheid en de vroegtijdige isolatie van patiënten met multiresistente bacteriën, betere controle van microbiologische risico’s in het milieu, een beter voorschrijfgedrag voor antibiotica bij gehospitaliseerde patiënten na de oprichting van de antibioticatherapiebeleidsgroepen,…) en dat deze mogelijk ook de ecologie van multiresistente Pseudomonas aeruginosa op de intensieve zorgeenheden gunstig hebben beïnvloed.
Drie recente meta-analyses (Alonso et al., 2016; Frost et al. 2018; Lewis et al. 2019) hebben interessante informatie opgeleverd. De heterogeniteit (voor de geselecteerde studies) van Alonso’s onderzoek, dat vier gerandomiseerde cross-over studies omvatte (zo’n 23.000 patiënten in 25 intensieve zorgeenheden in verschillende Europese landen), was aanvaardbaar en uit dit onderzoek bleek een daling met 26% van de incidentie van nosocomiale septicemieën (HA-BSI). Een subanalyse wees uit dat vooral de incidentie van kathetergerelateerde septicemieën (CLABSI) was gedaald (-50%) maar deze daling werd enkel waargenomen bij Gram-positieve bacteriën (-55%) zonder wijziging in de incidentie van septicemieën veroorzaakt door Gram-negatieve bacteriën. Dit wijst op een gunstig effect van chloorhexidine op de preventie van HA-BSI en CLABSI door een reductie van Gram-positieve bacteriën in de commensale flora. Uit de resultaten bleken ook significante verschillen tussen de centra al naargelang de kwaliteit van de «basishygiëne», met beduidend minder verschil in impact op de intensieve zorgeenheden wanneer de baseline HA-BSI- en CLABSI, nog voor er chloorhexidine werd gebruikt bij de dagelijkse wasbeurt, al laag was.
De meta-analyse die Frost et al. rapporteerden omvatte vijf gerandomiseerde klinische studies (drie gecontroleerde gerandomiseerde studies en twee gerandomiseerde cross-over cluster studies). Deze analyse had betrekking op meer dan 17.000 patiënten op intensieve zorgeenheden (>50 eenheden, in een tiental landen) en sloot niet-volwassen populaties (pediatrische intensieve zorgeenheden) uit, waarbij overigens enkel rekening werd gehouden met het aantal dagen met een infectierisico. Ook werden alle studies uitgesloten waarin er behalve het gebruik van chloorhexidine, andere interventies aan te pas kwamen.
De belangrijkste geanalyseerde resultaten die van belang waren zijn de volgende:
1) septicemieën (HA en niet-HA BSI);
2) centrale kathetergerelateerde septicemieën (CLABSI);
3) MDRO kolonisatie/infectiecijfers (voornamelijk MRSA, VRE, +/-Clostridium difficile met weinig/geen informatie over gram-negatieve MDRO);
4) ventilatorgeassocieerde pneumonieën (VAP); en
5) kathetergeassocieerde urineweginfecties (CAUTI).
Voor BSI en CLABSI bedroeg de daling van de incidentie na de introductie van chloorhexidine respectievelijk 29% en 40%, met een baseline incidentie tijdens de controleperiode van 6 BSI/1000 dagen intensieve zorgen (IZ) en 3 CLABSI/1000 katheterdagen. Voor MDRO’s werd een algemene daling van de incidentie met 18% waargenomen in de chloorhexidineperiode (met een baseline incidentie van 6 MDRO/1000 dagen IZ). Voor VAP of CAUTI werd geen enkele daling vastgesteld. De auteurs kwamen tot het algemene besluit dat het voordeel van chloorhexidine ten opzichte van een standaard wasbeurt onzeker was en dat het op basis van bestaande gegevens onmogelijk was, de aanbevelingen voor het gebruik ervan te veralgemenen.
De nadruk lag vooral op de noodzaak om aanvullende studies uit te voeren die voldoende groot en krachtig zijn om type I-fouten te voorkomen (het niet detecteren van een echt verschil) en op de noodzaak om meer homogene groepen (chirurgische, medische Intensive Care (ICU) of trauma) op te nemen en individuele risicofactoren te bestuderen, om mogelijke groepen/typen patiënten te identificeren die in het bijzonder baat kunnen hebben bij een wasbeurt met chloorhexidine. Tot slot waren de mate van naleving, de frequentie van de wasbeurten (dagelijks vs. om de twee dagen), de mogelijke effecten van de gebruikte concentratie chloorhexidine (2% vs. 4%) en de formulering (in de handel verkrijgbare gebruiksklare chloorhexidine-geïmpregneerde washandjes vs. ex tempore bereiden van de verdunning van de oplossing door het verplegend personeel aan het bed van de patiënt) enkele van de vele factoren die in de studies in dit overzicht niet aan bod zijn gekomen.
De meest recente meta-analyse van de Cochrane systematische review (Lewis et al. 2019) omvatte acht studies (vier gecontroleerde gerandomiseerde studies met meer dan 1.500 patiënten en vier gerandomiseerde cross-over cluster studies met 23 intensieve zorgeenheden met een totaal van ruim 23.000 patiënten. Deze reeks vergeleek het gebruik van 2%-chloorhexidine-geïmpregneerde washandjes of 4% verdunde chloorhexidineoplossingen, met wasbeurten met zeepwater of wasbeurten met niet-antimicrobiële washandjes. Aan de hand van een ‘level of evidence’-benadering (GRADE) leverde de meta-analyse een lage of zeer lage mate van zekerheid van bewijs op, afhankelijk van de indicatoren. Op basis daarvan kon geen enkele conclusie worden getrokken over het effect van chloorhexidine op het verminderen van het aantal ziekenhuisinfecties, de duur van het verblijf en de mortaliteit van patiënten op intensieve zorgen. Hoewel in vijf van de acht studies huidreacties werden gemeld als mogelijke bijwerking, was de rapportage meestal onvoldoende specifiek en kon niet worden vastgesteld dat chloorhexidine daar de oorzaak van was.
Tot slot is het belangrijk verdere studies uit te voeren en te proberen deze resultaten in verschillende lokale omgevingen te reproduceren. De aanpak van het UZA-team zet de toon en moet andere zorgteams aanmoedigen om de klinische en economische voordelen van wasbeurten met chloorhexidine in Belgische ziekenhuizen te evalueren en te verduidelijken. Op termijn kan deze zorgpraktijk een belangrijke pijler worden bij het ontwikkelen van strategieën om zorggerelateerde infecties bij risicopatiënten op intensieve zorgafdelingen, of zelfs bij risicogroepen op andere zorgafdelingen, te voorkomen.
Referenties
– Alonso E, Blot K, Blot S. Prevention of hospital-acquired bloodstream infections through chlorhexidine gluconate-impregnated washcloth bathing in intensive care units: a systematic review and meta-analysis of randomised crossover trials. Eurosurveillance 2016 ; 21(46) : pii=30400. DOI: http://dx.doi.org/10.2807/1560-7917.
– Frost SA, Hou YC, Lombardo L, Metcalfe L, Lynch JM, Hunt L, Alexandrou E, Brennan K, Saxnchez D, Aneman A, Christensen M. Evidence for the effectiveness of chlorhexidine bathing and health care-associated infections among adult intensive care patients: a trial sequential meta-analysis.BMC Infectious Diseases, 2018, 18 : 679-89.
– Lewis SR, Schofield-Robinson OJ, Rhodes S, Smith AF. Chlorhexidine bathing of the critically ill for the prvention of hospital-acquired infection. Cochrane Systematic Review – Intervention Version published: 30 August 2019
– https://doi.org/10.1002/14651858.CD012248.pub2