Prévention des infections liées à l’utilisation du cathéter veineux central : vers une tolérance zéro ?
Introduction
Les septicémies sont une des premières causes de morbidité et de mortalité. Le diagnostic et l’enregistrement de cette infection sont établis par une hémoculture positive. En Belgique, nous ne disposons pas de taux d’incidence fiables pour toutes les septicémies, mais en 2013, l’incidence moyenne des septicémies survenues en milieu hospitalier était de 5,9 pour 1000 admissions [http://www.nsih.be/]. Les septicémies peuvent être subdivisées sur la base de l’environnement (de soins) dans lequel elles se manifestent. Plusieurs paramètres, dont le vieillissement progressif de la population, l’évolution des soins de santé et la globalisation de plus en plus poussée rendent la subdivision épidémiologique entre septicémie « community onset » et septicémie « hospital onset » de moins en moins pertinente. Dans la catégorie des infections « community onset », on retrouve en effet une importante partie de patients se trouvant dans des environnements de soins chroniques comme les soins à domicile, le séjour dans une maison de repos et de soins ou un centre de jour. Ces infections portent également le nom de « healthcare associated ».[1]
Les septicémies peuvent aussi être subdivisées sur la base du foyer infectieux où elles prennent naissance. Dans le cas des septicémies qui se sont déclarées à l’hôpital, après un précédent foyer infectieux, les infections pulmonaires et urinaires sont les plus fréquentes, suivies par les infections des plaies postopératoires. L’origine de certaines septicémies demeure inconnue. Une partie d’entre elles peut certainement être imputée à une transmission de bactéries dans le sang par le biais de muqueuses endommagées (MBI-LCBSI). Cette situation touche les patients dont l’immunité est compromise, comme les patients ayant subi une transplantation et les patients traités par chimiothérapie ou radiothérapie. [2] Les nouvelles définitions sont résumées dans le Tableau 1. Elles permettent de procéder à une classification plus précise des septicémies et d’ainsi plus facilement identifier la partie des infections qui pourrait être évitée.
Les septicémies se déclarant dans nos hôpitaux font partie des infections associées aux soins qui sont influençables par notre pratique des soins et notre attitude. La réduction de l’incidence des septicémies pouvant être réalisée par la prévention des infections est notable, d’autant plus que le risque de mortalité de ces infections est élevé. La prévention des septicémies provoquées par des cathéters veineux centraux incombe à cette entité et mérite dès lors toute l’attention de chaque établissement de soins et chaque professionnel de la santé.
Cet article relate notre expérience en tant que participant à une étude européenne ayant pour but d’éviter les septicémies provoquées par des cathéters veineux centraux en utilisant des « bundles ». Dans la description, nous mettons l’accent sur le changement de comportement nécessaire à la réussite de ce projet. Nous esquissons les obstacles et opportunités mis au jour lors de l’étude.
Matériel et méthode
L’étude PROHIBIT (PRevention Of Hospital Infections By Intervention and Training) a été mise en place au sein de l’Union européenne (UE). Le projet fait partie du Framework 7 Specific Targeted Research Projects (STReP) de l’UE. (http://ec.europa.eu/research/fp7). Les centres de coordination nationaux européens supervisant également le réseau EARS (en Belgique, il s’agit du WIV-ISP), ont porté ce projet européen à la connaissance de tous les hôpitaux aigus en 2010. Ceux qui étaient intéressés pouvaient introduire un dossier de candidature auprès du coordinateur européen national.
Lors du lancement de l’étude PROHIBIT, en 2010, le taux d’incidence moyen des septicémies déclarées en milieu hospitalier était de 7,5/10.000 jours patients en Belgique. Avec un taux d’incidence moyen de 3,5/10.000 jours patients, la proportion de septicémies secondaires dont le foyer se trouve dans un organe est la plus élevée. La proportion d’infections liées à un cathéter veineux central est moins élevée et présente de plus grandes disparités d’un hôpital à l’autre et s’élève en moyenne à 1,4/10.000 jours patients [http://www.nsih.be/]. L’AZ Sint-Lucas Gand est un hôpital secondaire de 805 lits et d’une durée d’admission moyenne de 6,1 jours. La durée d’admission moyenne en soins intensifs est de 4,1 jours. L’incidence des infections liées à un cathéter veineux central en hôpital était de 1,8/10.000 jours patients au début de l’étude.
PROHIBIT est une étude en six parties. Deux parties, l’étude d’intervention et le module « in depth », ont dû être menées au sein des départements soins intensifs de 15 hôpitaux répartis dans l’UE. Dans l’étude d’intervention, l’efficacité des stratégies reprises dans le bundle sur le taux d’incidence des infections liées à un cathéter veineux central a été mesurée. Cette partie prévoyait également des modules « train the trainer » consacrés à l’hygiène des mains et à la pose d’un cathéter veineux central. (www.carepractice.net). Dans le module « in depth », les facteurs de succès et obstacles à l’implémentation du bundle de pratiques pour la prévention des infections liées à un cathéter veineux central ont été mesurés auprès d’un échantillon représentatif de centres d’études.
La méthodologie « stepped wedge cluster randomisation » a été utilisée dans le cadre de l’étude. Cette dernière est une forme spéciale d’essais randomisés dans lesquels une intervention au niveau du groupe est introduite progressivement. Le concept peut s’utiliser lorsque la randomisation au niveau individuel n’est pas possible. Une période de contrôle est également intégrée dans ce concept : il s’agit du moment avant que l’intervention expérimentale soit introduite dans un cluster. Ce type d’essai est de meilleure qualité que les études avant/après ou des études de prévalence ponctuelles mais nécessite également de considérables investissements en termes de temps, d’argent et de personnel. L’étude PROHIBIT a comparé l’efficacité de 3 tactiques : hygiène des mains, bundle sur les cathéters ou les deux. L’étude a été déployée de manière séquentielle dans l’unité de soins intensifs de 14 hôpitaux aigus européens. Le coup d’envoi a été donné en janvier 2011 sous la forme d’une période de contrôle de 6 mois lors de laquelle, en marge de la mesure de l’observance de l’hygiène des mains au travers d’un système randomisé, intensif d’observations, les infections liées à un cathéter veineux central ont également été enregistrées. Ces observations et mesures se sont poursuivies tout au long du trajet. En juillet 2011, notre hôpital a été sélectionné au hasard pour appliquer le bundle lié à la pose de cathéters veineux jusqu’à la fin de l’étude, en juin 2013. Au rythme de 3 nouveaux participants par trimestre, une intervention avait été attribuée à tous les hôpitaux en juillet 2012. Nous n’avons pas participé au volet « in depth » mais avons tenu à jour un journal (implementation log) dans lequel nous avons documenté la mise en œuvre du bundle. Nous partagions régulièrement ce journal avec les coordinateurs de l’étude.
Résultats
L’étude a duré 36 mois. Au final, 14 hôpitaux provenant de 11 pays européens (Belgique, Grèce, Irlande, Italie, Hongrie, Lettonie, Autriche, Pologne, Roumanie, Slovénie et Espagne) ont pris part à l’étude. Au total, 25.377 patients ont été inclus, avec 35.894 cathéters, 263.093 jours cathéter et 384 infections liées à un cathéter veineux central. Un ratio d’infection moyen déjà faible avant l’étude, de 2,4 infections liées à un cathéter veineux central par 1000 jours cathéter, a encore reculé pour atteindre 0,9 infection par 1000 jours cathéter. [Figure 1] Les hôpitaux établis dans les pays aux dépenses en matière de soins de santé les moins élevées étaient également ceux affichant le taux d’infection de base le plus élevé. La compliance à l’hygiène des mains et la pratique d’insertion des cathéters se sont améliorées dans pratiquement chaque centre. La compliance à l’hygiène des mains moyenne était de 49 % au début de l’étude. L’amélioration de l’application de l’hygiène des mains la plus notable a été enregistrée dans les hôpitaux qui avaient été sélectionnés au hasard pour uniquement appliquer cette intervention. Dans plusieurs hôpitaux, dont celui à Gand, auxquels le bundle sur les cathéters a été attribué, on a également enregistré une amélioration notable de l’application de l’hygiène des mains. L’amélioration de l’application du bundle sur les cathéters la plus notable a été enregistrée dans les centres auxquels ce bundle a été attribué, éventuellement en combinaison avec l’hygiène des mains. Quelques centres devant uniquement faire la promotion de l’hygiène des mains ont également enregistré une légère hausse de l’application du bundle lié à la pose de cathéters. Les différents volets de l’étude PROHIBIT ont été présentés lors de congrès et dans des publications. [3] Un résumé des résultats complets de l’étude a été publié sur le site web CORDIS (Community Research and Development Information Service) de la Commission européenne. [ http://cordis.europa.eu/result/rcn/158223_en.html]
Discussion
Il avait auparavant déjà été démontré que les interventions multimodales lors de la pose de cathéters et de soins liés aux cathéters avaient une influence évidente sur le taux d’incidence des infections liées à un cathéter veineux central au sein du département soins intensifs [4]. Un bundle pour la prévention des infections liées à un cathéter veineux central contient tout au moins les paramètres suivants : barrière stérile maximale lors de la pose d’un cathéter, l’évitement de la pose de cathéters fémoraux, l’hygiène des mains lors des soins liés à la pose d’un cathéter et de la manipulation de cathéters et un questionnaire quotidien de l’indication pour le maintien du cathéter.
Un examen et une analyse méta systématiques récents de 2014 ont étudié les interventions les plus efficaces pour éviter les infections liées à un cathéter veineux central. Il en a été conclu que de telles interventions existaient et que les bundles de soins et les check-lists enregistraient les meilleurs scores.[5] Le principal objectif de l’étude PROHIBIT n’était pas de confirmer ces résultats, mais d’en évaluer l’efficacité dans la pratique.
Nous avons été confrontés à quelques obstacles avant même que l’étude ne débute. Le premier obstacle était la loi vie privée belge qui, dans le cadre d’une recherche interventionnelle, impose l’accord écrit de chaque patient intégré dans l’étude. [http://www.fagg-afmps.be/fr/]. Cette obligation est entièrement justifiée dans le cas de véritables recherches interventionnelles. L’étude PROHIBIT mène également des interventions, mais il s’agit d’actes qui devraient faire partie des GMP (Good Medical Practice) au sein de chaque établissement. Il s’agit ici de processus validés intégrés dans des directives (inter)nationales. Il s’agit également d’une exigence pour l’étude, attribuant la même qualité de soins/le même bundle de soins à autant de patients que possible au sein du département. L’obtention de ces autorisations écrites n’était une obligation légale qu’en Belgique et a induit une pression administrative importante sur l’étude et a parfois été source d’ambiguïtés auprès du patient. Nous préconisons donc que les comités d’éthique médicale examinent à l’avenir minutieusement les aspects éthiques des essais stepped-wedge, informant largement les patients et leur entourage, mais ne nécessitant plus d’accord écrit au niveau individuel. Chaque patient conserve bien évidemment le droit de choisir individuellement de ne pas participer à l’étude (opting out). Un deuxième obstacle de la méthodologie appliquée était que l’hôpital individuel pouvait tôt ou (très) tard être sélectionné au hasard de sorte que l’intervention ne pouvait être exécutée que pour une période limitée. En cas de randomisation tardive, vous disposez de nettement moins de temps pour mettre l’intervention en œuvre et, le cas échéant, l’ancrer au sein de l’établissement.
Il semble logique, dans le cadre de la prévention des infections liées aux cathéters veineux centraux, de se concentrer sur les départements où les cathéters veineux centraux sont présents en nombre comme les soins intensifs, l’hémato-oncologie, l’hémodialyse. Cependant, les départements au sein desquels le nombre de cathéters est nettement inférieur constituent également un risque réel vu que l’expertise des collaborateurs y est nettement moins élevée. Sur la base de l’enregistrement continu des septicémies nosocomiales dans le NSIH (national surveillance of healthcare associated infections and antimicrobial resistance in Belgian hospitals, WIV-ISP), nous avons obtenu un aperçu du taux d’incidence des infections liées à un cathéter veineux central dans notre établissement. Il en est ressorti que le taux d’incidence de base pour l’hôpital dans son ensemble était faible à moyen et qu’une importante partie des infections liées à un cathéter veineux central concernait le département des soins intensifs. A l’issue d’une concertation avec la direction (des soins) et l’équipe en charge de la prévention des infections, il a été décidé de directement mettre ce projet en œuvre au sein du service soins intensifs afin d’également permettre un meilleur enregistrement et une amélioration des soins liés aux cathéters au sein de tous les autres départements.[6] L’étude nous a permis de revoir en profondeur les procédures et d’élaborer des fiches d’instruction. Il s’agit d’une condition fondamentale pour l’amélioration de la qualité, mais il faut aller plus loin. La création d’une culture d’engagement et de responsabilité auprès de chaque collaborateur importe davantage. Chaque collaborateur doit être convaincu que les infections liées à un cathéter veineux central sont problématiques et qu’elles peuvent en partie être évitées. Il est possible de faire dans ce cadre appel à une communication directe et continue sur la prévalence et l’incidence des infections liées à un cathéter veineux central, en élaborant des procédures écrites et fiches d’instruction. Il est cependant également possible de faire mieux, de manière plus efficace et plus durable en impliquant dans ce processus chaque collaborateur sur son lieu de travail. [7] Cette approche permet de créer un réseau de pairs qui, en agissant correctement, exercent une pression normative sur ceux ne le faisant pas encore. L’amélioration de la qualité nécessite également un leadership, comme l’a illustrée la comparaison de la compliance au sein des deux départements utilisant des cathéters veineux centraux.
Le département soins intensifs s’est mué, avec le soutien de médecins intensivistes et infirmiers en chef, en une véritable équipe mettant expertise et habileté au service de la pose des cathéters et des soins liés à ces derniers. Le même résultat a été obtenu pendant une certaine période au sein du département en charge des opérations, sous l’impulsion de l’infirmier de l’étude, mais son impact s’est ensuite rapidement érodé.
Les interventions multimodales ne s’assortissent pas de points d’évaluation majeurs. Les résultats de l’étude ont démontré que les hôpitaux, en marge de l’intervention obligatoire, améliorent également la qualité des processus inhérents. Les coordinateurs de l’étude en avaient conscience et ont, également pour des raisons d’éthique, toujours ouvert la porte à des améliorations locales, parallèles. Le module « in depth » et les journaux ont permis de mieux comprendre la dynamique des stratégies multimodales et de confirmer que cette approche était réalisable en Europe.[8] Dans tous les hôpitaux, il est toujours apparu qu’une combinaison de facteurs conduisait à une amélioration de la qualité. Des personnes expérimentées, occupant une position respectée ou en mesure de créer des liens, restent indispensables à un processus d’amélioration. A côté de cela, un soutien financier semble indispensable à l’installation d’un coordinateur de projets. Le soutien par une équipe expérimentée en charge de la prévention des infections semble également jouer un rôle de facilitation majeur.
Il est possible d’extraire une vision et une mission pour les formateurs d’opinions et décideurs politiques. Nous avons, en notre qualité de participant à PROHIBIT, déjà commencé à le faire au sein de notre établissement.
Références
1. Laupland K, Church D. Population based epidemiology and microbiology of community onset bloodstream infections. Clin Microbiol Rev 2014; 27(4):647-664.
2. Steinberg J, Coffin S. Improving the Central Line–Associated Bloodstream Infection Surveillance Definition: A Work in Progress. Infection Control Hospital Epidemiol 2013; 34(8):769-776.
3. van der Kooi T, Wolkewitz M, van Benthem B et al. Prohibit (preventing hospital-acquired infections by intervention and training): preliminary results of a European multi-center study on the effectiveness of a hand hygiene campaign and a central venous catheter bundle. Antimicrob Resist Infect Control 2013; 2(Suppl 1):O83.
4. Pronovost P, Needham D, Berenholtz S et al. An Intervention to Decrease Catheter-Related Bloodstream Infections in the ICU. N Engl J Med 2006; 355:2725-2732.
5. Blot K, Bergs J, Vogelaers D et al. Prevention of central line-associated bloodstream infections through quality improvement interventions: a systematic review and meta-analysis. Clin Infect Dis 2014; 59(1):96-105.
6. Zingg W, Huttner B, Sax H. Assessing the Burden of Healthcare-Associated Infections through Prevalence Studies: What Is the Best Method? Infection Control Hospital Epidemiol 2014; 35 (6):674-684
7. Zingg W, Walder B, Pittet D. Prevention of catheter-related infection: toward zero risk? Curr Opin Infect Dis 2011; 24:377-384
8. Sax H, Clack L, Touveneau S et al. Implementation of infection control best practice in intensive care units throughout Europe: a mixed-method evaluation study. Implement Sci 2013; 8(24):8:24
Tableau 1 : Définitions utilisées dans l’étude européenne PROHIBIT sur l’efficacité d’une ‘bundle care’ pour la prévention des septicémie dans des hôpitaux aigus.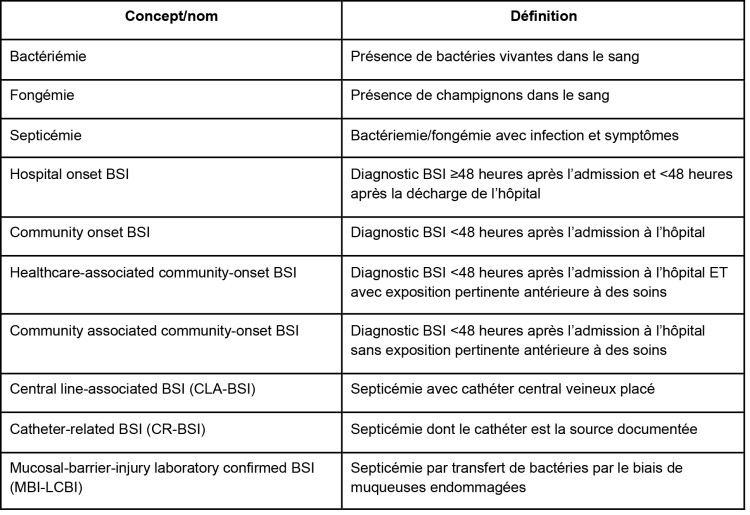
Figure 1 : Incidence des septicémies liées aux cathéters (CR-BSI) par 1000 journées cathéter avant et après une intervention ‘bundle care’, de l’étude PROHIBIT (14 hôpitaux dans 11 pays européens)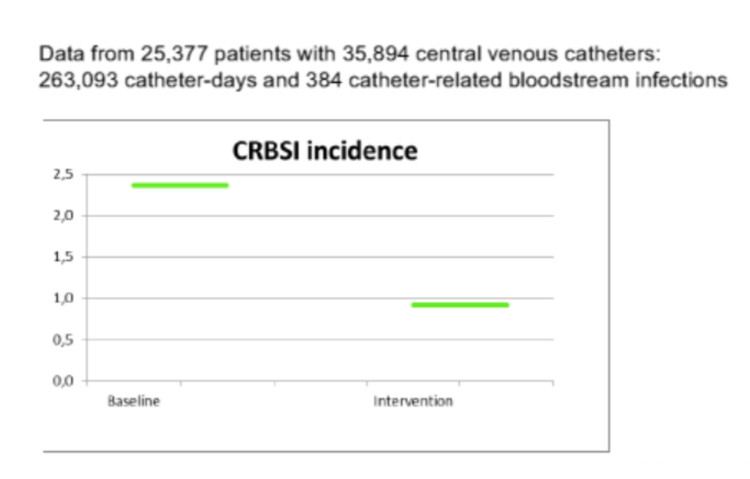
Nouveautés
Agenda scientifique
- avril 2025
-
du 11/04 au 15/04 || à Vienne
Congrès de l’ European Society of Clinical Microbiology and Infectious Diseases (ESCMID)
- juin 2025
-
du 4/06 au 6/06 || à Marseille
35ème Congrès National de la Société Française d’Hygiène Hospitalière (SF2H)
-
du 17/06 au 18/06 || à Londres
Congrès HIS (Healthcare Infection Society)
- septembre 2025
-
du 16/09 au 19/09 || à Genève
International Conference on Prevention and Infection control (ICPIC)
- octobre 2025
-
du 19/10 au 22/10 || à Atlanta
Society for Health Care Epidemiology of America (SHEA)


