A propos des masques: lesquels, quand et comment?

I. Masques chirurgicaux (« masques médicaux »)
1. Introduction
Les masques chirurgicaux (également appelés « masques médicaux » ou « masques de soins») sont des dispositifs médicaux qui couvrent la bouche et le nez et forment ainsi une barrière limitant le transfert d’agents infectieux entre les prestataires de soins de santé (PSS) et le patient. La réglementation européenne considère ces masques comme des dispositifs médicaux (« medical devices ») de classe I, et ils doivent se conformer au Règlement européen 93/42/CEE. Ce Règlement stipule que les dispositifs médicaux et accessoires ne peuvent être autorisés et mis sur le marché européen que s’ils portent le marquage CE. Le fabricant doit pour ce faire procéder à une évaluation de leur conformité. A partir du 26 mai 2020, la Directive 93/42/CEE sera abrogée et remplacée par le Règlement (UE) 2017/745.
Ces masques peuvent avoir différentes applications :
- Prévention de la contamination per-opératoire du patient vis-à-vis des micro-organismes provenant des PSS et émis lors de la toux, d’éternuements, de la parole (types II et IIR) ;
- Protection des PSS vis-à-vis des éclaboussures de sang et d’autres liquides biologiques (types IR et IIR) ;
- Limitation des risques de transmission de micro-organismes pathogènes (par ex. virus influenza) par des patients et/ou visiteurs (types I et II).
La norme européenne EN 14683:2014 précise les exigences auxquelles les masques chirurgicaux doivent répondre et facilite le choix par l’utilisateur d’un masque adapté à ses besoins. Conformément à cette norme, le fabriquant/fournisseur présente les caractéristiques de qualité de manière normalisée à l’utilisateur (1).
2. EN 14683:2014
Les exigences de performance minimale de la norme européenne EN 14683:2014 concernent :
- L’efficacité in vitro de filtration bactérienne (l’efficacité de filtration bactérienne exprimée en pourcentage (%) est mesurée sur le matériau du masque et elle ne prend pas en compte les fuites au visage): plus l’EFB est élevée, plus le degré de protection du patient contre les micro-organismes provenant de l’équipe chirurgicale est efficace. Les particules utilisées dans ce test ont une taille moyenne de 3 microns. Une efficacité filtrante ≥95% donne lieu à une classification de type I, une efficacité filtrante ≥98% à une classification de type II. Il est conseillé d’utiliser un masque à haute capacité filtrante pour les interventions chirurgicales de longue durée.
- La résistance respiratoire (Delta P): exprime la résistance du masque à la respiration. A niveau de fuite à la périphérie identique, un masque permettra un meilleur confort d’utilisation au porteur (respiration plus aisée, fraicheur accrue) lorsque la résistance respiratoire est basse. Une résistance plus faible entraîne une pression moindre sur le masque, qui conservera mieux sa forme. Par ailleurs, une moindre quantité d’air non filtré s’échappera des contours du masque. La résistance respiratoire s’exprime en mm H2O/cm2 ou en Pascal (Pa)/cm². Les masques non résistants aux éclaboussures (type I et II) présentent une résistance à la respiration < 3,0 mmH2O/cm2 (< 29,4 Pa/cm2) tandis que celle-ci doit être < 5,0 mmH2O/cm2 (< 49,0 Pa/cm2) pour les masques résistants aux éclaboussures (de type IR et IIR).
- La résistance aux éclaboussures : les masques doivent être conformes au test de résistance aux éclaboussures selon la norme EN ISO 22609 ; plus la résistance aux éclaboussures est élevée, plus l’utilisateur sera protégé des éclaboussures potentiellement contaminantes qui peuvent se produire lors d’interventions chirurgicales. La résistance s’exprime en mm Hg ou en kPa. La résistance doit être d’au moins 120 mm Hg (ou 16,0 kPa), ce qui correspond à la pression artérielle systolique moyenne. L’objectif est de protéger l’utilisateur de petites projections de sang qui se produisent lors de l’éclatement de petits vaisseaux.
- Pureté microbiologique : les masques doivent être testés conformément à la norme EN ISO 11737-1, pour confirmer que la présence de la charge microbienne (« bioburden ») composés de micro-organismes viables est ≤ à 30 cfu/g.
Confort cutané. Le test de résistance respiratoire reflète également un élément important de confort cutané. Cet aspect n’était pas repris dans la norme précédente de 2004. Compte tenu du contact direct du masque avec une zone sensible de la peau, il est important que celui-ci ne provoque pas d’irritation cutanée. La norme de 2004 stipule que le fabricant doit procéder à une évaluation des masques selon la norme EN ISO 10993-1 (évaluation biologique) Ce test apporte des élements d’information quant aux effets biologiques des masques sur la peau, tels que cytotoxicité, hypersensibilité et irritation cutanée. Les résultats de ce test doivent être documentés et disponibles sur demande des utilisateurs.
Synthèse des exigences de performance
Tableau 1 : exigences de performance selon la norme EN 14683:2014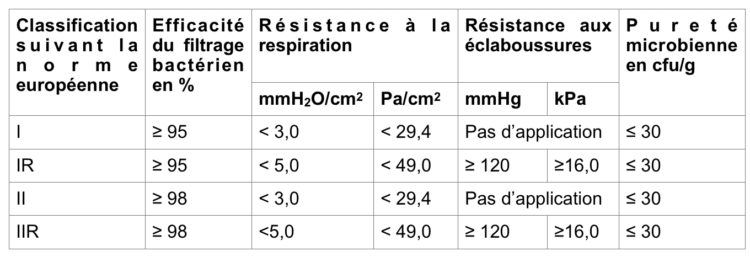
3. Tests non pris en compte dans la norme EN14683:2014 (1,2)
- Capacité de filtration de particules. Des particules de très petite taille (inférieure à 0,1 micron) peuvent être émises notamment lors d’interventions chirurgicales au laser (fumée due au laser/fumée diathermique). Des masques respiratoires de protection personnelle (EN 149:2001) adaptés peuvent constituer une barrière vis-à-vis des micro-organismes présents dans la fumée chirurgicale. Au Pays-Bas, le ‘Werkgroep Infectiepreventie’ (WIP) recommande le port d’un masque respiratoire de type FFP2 (voir plus loin) en l’absence d’aspiration à la source de la fumée de laser. Néanmoins, certains composés aromatiques volatils benzéniques, plusieurs particules d’ADN d’origine virale, telles celles des virus HPV (0,045 micron), HBV (0,042 micron) et VIH (0,10 micron) pénétreront facilement au travers de ces masques. Des particules intactes d’ADN et les virus correspondants ont en effet également été retrouvées dans la fumée chirurgicale. (3,4). En 1997, le WIP a émis la recommandation que les masques respiratoires à haute pression offraient la meilleure protection contre la fumée chirurgicale (5).
- Capacité de filtration en fonction du temps. Aucun élément ne semble actuellement indiquer une baisse de la capacité de filtration des masques lorsqu’ils sont portés pendant une longue période. Une étude (6) a cependant démontré que lors du port d’un masque (masque jetable double couche de 200 g/m2), le nombre de micro-organismes émis augmentait en fonction du temps; après le port du masque pendant environ 2,5 heures, la charge microbienne à l’extérieur du masque était aussi élevée que celle mesurée en l’absence du port de masque. Cette étude ne précisait cependant pas clairement les qualités techniques du masque testé, telles sa capacité de filtration, la présence de cordons ou d’élastiques d’oreille, etc.
Selon un fabricant (7) et des recommandations françaises (8), un masque chirurgical offre une protection pendant 3 heures maximum mais doit être remplacé plus tôt lorsqu’il est souillé ou humide. - Efficacité de la filtration bactérienne in vivo. Vu la très grande variabilité individuelle dans la façon de porter un masque, il faudrait idéalement évaluer un très large éventail de sujets, ce qui rend ce type de test très coûteux. A noter qu’un élément déterminant pour l’efficacité d’un masque est qu’il recouvre bien le nez et la bouche. Ainsi, un masque maintenu en place par des élastiques autour des oreilles sera moins efficace qu’un masque à cordons.
- Capacité d’absorption de l’humidité dans l’air expiré : pour des interventions de longue durée, il est particulièrement important de disposer de masques qui maintiennent leurs performances pendant une plus longue période.
4. Quel type de masque chirurgical utiliser dans quelles circonstances ?
a) Indications
Les indications suivantes ne sont pas limitatives et sont reprises uniquement à titre exemplatif. Pour garantir la standardisation, il peut être licite de décider de ne prévoir dans l’établissement qu’un seul type de masque pour l’ensemble des indications (par ex. le type IIR).
Tableau 2 : Exemples d’indication
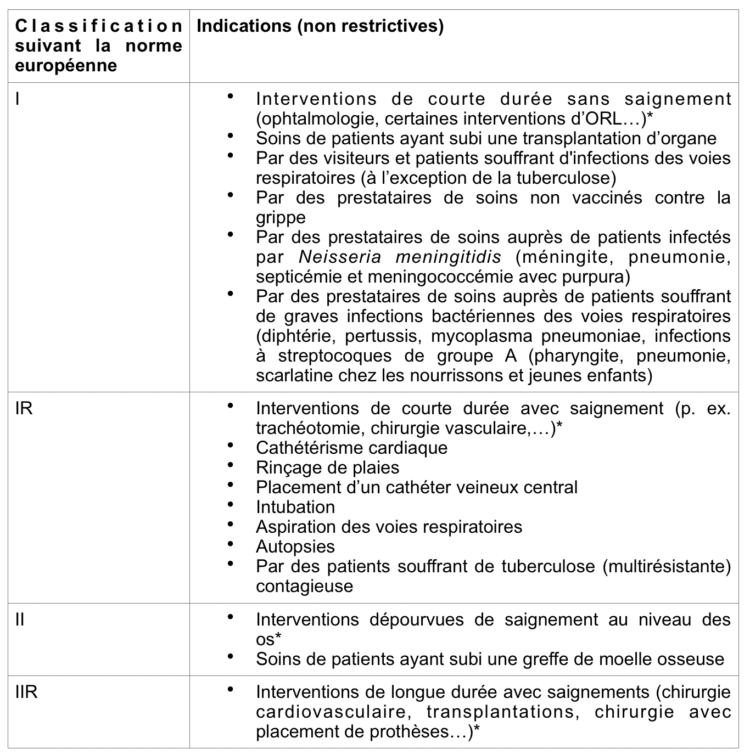
*Le port d’un masque chirurgical vise d’une part pendant l’intervention, à éviter l’émission de particules et l’introduction de la flore microbienne oro-pharyngée des opérateurs dans la plaie ouverte du patient et d’autre part de protéger l’équipe opératoire des éclaboussures de sang et de fluides corporels.
Bien que l’utilité du port du masque pour la prévention d’infections des plaies postopératoires (IPPO) reste controversée (9), le WIP estime que les données de la littérature ne permettent pas de conclure à contrario que le port du masque en prévention d’une infection des plaies constitue une pratique insensée 10).
Le Conseil Supérieur de la Santé (11) recommande également le port du masque chirurgical dans la zone d’activité critique du quartier opératoire, et ce, tant par l’équipe opératoire que par le personnel circulant. La zone critique en activité est décrite comme suit :
– les instruments sont préparés et disposés sur les tables ;
– un des opérateurs a terminé sa préparation de façon stérile ;
– le champ opératoire est préparé.
b) Visiteurs et patients
Il est recommandé que les visiteurs et patients souffrant de fortes quintes de toux portent un masque chirurgical. A cet égard, Il est important de mettre en place des affiches explicites aux différentes entrées de l’hôpital afin d’informer les patients que des masques peuvent être mis à disposition par le biais de « stations de toux », où des mouchoirs en papier et du gel hydroalcoolique sont également disponibles (Figure 1).
Lorsqu’il s’agit de maladies transmissibles par voie aérienne comme la tuberculose, le port d’un masque chirurgical peut suffire (voir plus loin, sous les masques respiratoires).
Figure 1: Exemple d’une « Station de toux » à l’UZA

c) Examen d’imagerie par résonance magnétique (IRM)
Les patients qui,en cas de maladie infectieuse potentiellement contagieuse, doivent porter un masque pendant un examen d’IRM, doivent s’en voir proposer un exempt de métal. Du métal est notamment présent au niveau de l’arceau nasal ou des cordons de fixation du masque.
5. Comment porter un masque chirurgical ?
Un masque chirurgical n’offre une protection optimale que lorsqu’il est correctement porté. Le masque doit dès lors bien épouser les contours de la peau et rester bien en place. Un masque qui bouge accroît l’exfoliation de la peau et la contamination bactérienne de surfaces directement sous le visage. McLure et al. (2000) (12) ont étudié l’effet des mouvements du masque auprès de 10 hommes barbus, 10 hommes rasés de près ainsi que chez 10 femmes. Le va-et-vient du masque a augmenté la charge bactérienne sur une gélose de culture posée 15 cm sous les lèvres tant chez les sujets barbus (p = 0,03) que chez les femmes (p = 0,03) mais pas chez les hommes rasés de près. Au repos, même avec masque bien fixé, les sujets barbus véhiculaient nettement plus de bactéries que les hommes rasés de près (p = 0,01) ou les femmes (p = 0,001). Globalement, ces données étayent bien l’importance de la bonne fixation du masque (sans va et vien) chez tout le monde pour réduire le risque de contamination du champ stérile. On peut utiliser l’ étude de McLure et al pour conseiller (et essayer de convaincre) que les chirurgiens barbus devraient raser leur barbe
Les masques à cordons sont dès lors à privilégier : les cordons supérieurs doivent être fixés à l’arrière de la tête et les cordons inférieurs à l’arrière, au niveau de la nuque. Le masque doit toujours être suffisamment déployé afin de réduire au minimum le nombre de couches à travers lesquelles la respiration doit se faire. Pour une occlusion optimale, l’arceau nasal doit être bien enfoncé (Figure 2).
Comme déjà signalé plus haut dans le texte, il est recommandé de porter un masque chirurgical au maximum pendant 3 heures, et, de le remplacer plus tôt lorsque celui-ci est souillé ou humide.
Figure 2 (13): masque chirurgical
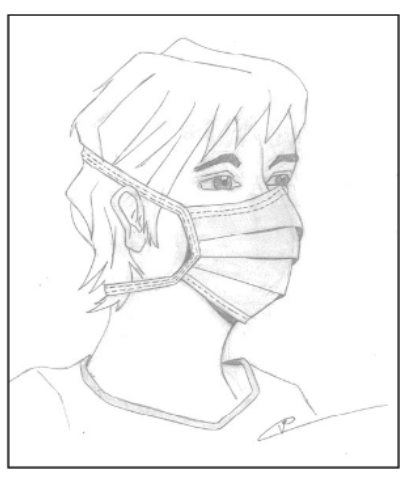
Pour éviter la contamination des mains, le masque ne peut être touché pendant qu’il est porté. Lors du retrait, le masque doit être éliminé avec les déchets médicaux sans risque. En aucun cas, le masque ne peut être conservé dans le sac des vêtements de travail en vue d’un usage ultérieur.
Une désinfection des mains doit être effectuée de manière systématique après le retrait du masque compte tenu de la contamination de celui-ci par la flore microbienne oro-pharyngée du porteur.
6. Les masques en tant que dispositifs médicaux et équipements de protection individuelle (EPI)
Dans certaines situations bien spécifiques, il peut s’avérer nécessaire de recommander le port d’un masque permettant d’assurer une protection adéquate des prestataires de soins vis-à-vis de maladies transmissibles par voie aérienne en plus de leur fonction habituelle de prévention de la contamination de la plaie opératoire à partir des particules respiratoires émises par les opérateurs pendant l’intervention (cf. supra). Pareille situation peut survenir par exemple lors d’interventions chirurgicales chez un patient avec tuberculose pulmonaire active ou laryngée (suspectée ou confirmée). Ces masques doivent se conformer aux exigences d’un masque chirurgical de type IIR (EN 14683) et aux exigences de la norme EN149 pour les masques respiratoires (masques FFP) (voir plus loin). Si l’on opte pour un masque avec valve respiratoire, il existe des masques dont les propriétés du revêtement apposé sur la valve répondent aux exigences d’un masque chirurgical de type IIR.
L’adaptation du Règlement européen concernant les dispositifs médicaux (« Medical Device Directive ») permet la mise en vente sur le marché européen des dispositifs médicaux qui protègent le porteur du masque mais aussi revendiquent des qualités en vertu du Règlement relatif aux équipements de protection individuelle, ce qui n’était pas possible auparavant.
7. Impact d’un masque chirurgical sur le patient
Une étude randomisée et contrôlée menée auprès de 1030 patients, a mis en évidence que le port d’un masque par les médecins pendant les consultations avait un impact négatif sur les patients ceux-ci percevant nettement moins l’empathie du médecin à leur égard. Un tel élément pourrait altérer la relation de confiance médecin-patient et entraîner des conséquences dommageables au niveau thérapeutique. Les auteurs concluaient que tant les avantages que les inconvénients du port d’un masque devraient être pris en considération dans le cadre de recommandations . Ka Man Wong et al. (14).
II. Masques respiratoires 1. Introduction
Les masques respiratoires sont considérés comme des EPI et devaient, conformément au Règlement européen 89/686/CEE, arborer une étiquette CE comportant un numéro d’enregistrement d’un « organisme notifié », un code à quatre chiffres de l’instance de contrôle. Le Règlement 89/686/CEE a été remplacé par le nouveau Règlement EPI 2016/425 qui est entré en vigueur le 21 avril 2018. Les normes européennes EN149:2001 et A1:2009 précisent les exigences auxquelles ces masques respiratoires doivent répondre.
Pour être conformes aux normes EN149:2001 et A1:2009, les masques doivent assurer une bonne protection vis-à-vis de la poussière, de la fumée ainsi que les aérosols « solides » (S) et « liquides » (L).
Sur la base des résultats de test de la norme européenne EN149, un masque respiratoire jetable (ne nécessitant pas d’entretien) est catégorisé dans l’une des trois classes : FFP1, FFP2 et FFP3. La classe « P» correspond au niveau de performance des filtres ; les lettres « FFP» font référence à la dénomination « filtering face piece ». Les classes les plus élevées correspondent aux meilleurs niveaux d’efficacité.
Le test européen utilise une solution de NaCl en phase aqueuse à un débit de 95 l/min (avec détermination d’un gradient de pression) et des particules d’un diamètre moyen de 0,6 micromètre. On effectue aussi un test pour les particules liquides au moyen d’un aérosol à base d’huile de paraffine. En outre, on effectue des tests in vivo (sur personnes réelles), qui déterminent le niveau total de fuite vers l’intérieur. Ce dernier élément permet d’évaluer la bonne occlusion au niveau du visage.
Tableau 3 : exigences de performance selon EN 149:2001+A1:2009
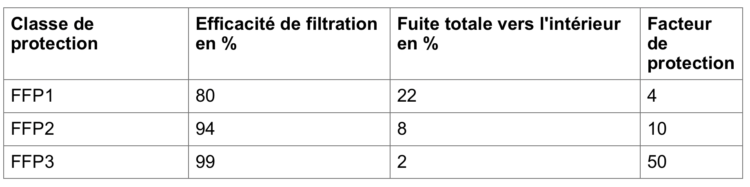
Les masques peuvent également être équipés ou non d’une valve respiratoire. Cette valve respiratoire augmente le confort du porteur, surtout en cas de port de longue durée (> 30 minutes). En effet, plus l’efficacité de filtration sera élevée, plus la résistance respiratoire le sera également. Cette valve évite en outre l’effet de surchauffe.
Les masques respiratoires jetables peuvent être portés pendant plusieurs heures (par ex. pendant un service complet).
Les masques à poussière portant le code D (exemple : FFP3D) peuvent être portés pour une durée supérieure à un service, pour autant que l’on suive les instructions d’emploi.
2. Types de masques respiratoires
Plusieurs types de masques respiratoires sont disponibles sur le marché. Dans le groupe des masques ajustés, on retrouve les masques jetables, les demi-masques et les masques complets réutilisables avec filtres. Citons également les systèmes respiratoires motorisés qui protègent l’ensemble du visage et dans lesquels l’air ambiant est injecté dans le masque ou dans la cagoule de protection (figure 4). Le facteur de protection de ces masques réutilisables, combiné aux filtres est très variable et d’autres normes européennes les régissent (comme les normes EN 143 et EN 12941). Conformément à la norme EN 143, les filtres sont répartis en trois classes de filtration, P1, P2 et P3 représentant une pénétration de filtration de respectivement 20 %, 6 % et 0,05 %.
Les masques non réutilisables arborent la mention « NR » (« non-reusable ») et peuvent être utilisés pendant maximum un service. Les masques réutilisables peuvent être portés pendant plusieurs services et doivent se soumettre à des tests supplémentaires pour pouvoir arborer la mention « R » (« reusable »).
Figure 3 : types de masques et systèmes respiratoires (13)
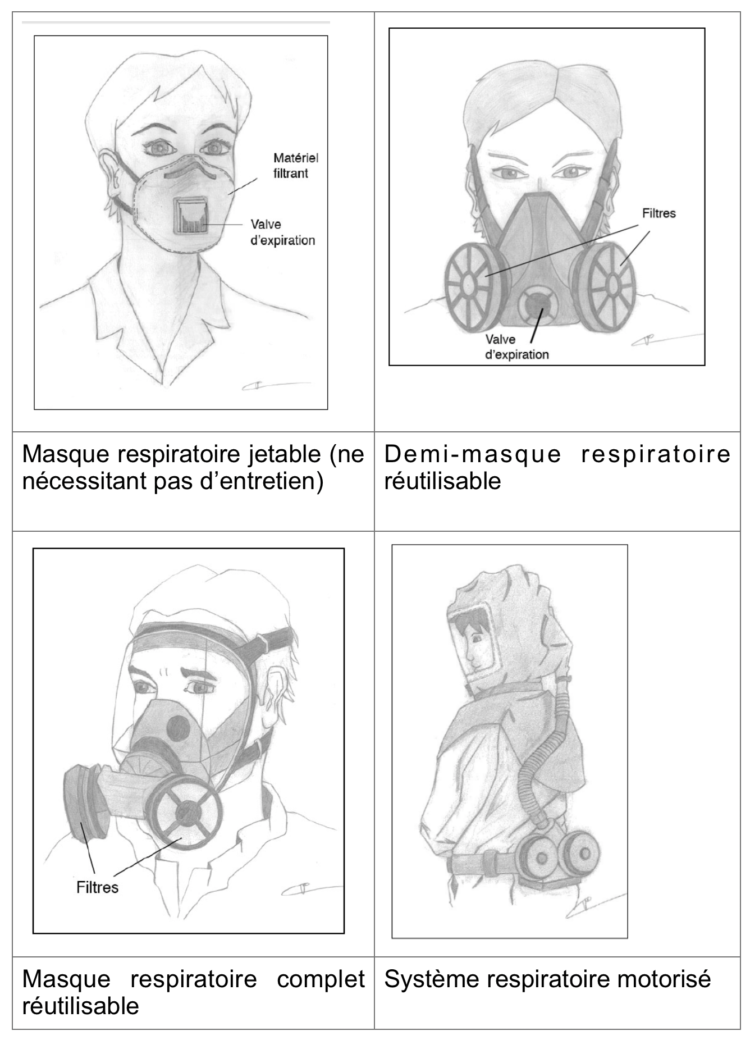
3. Indications des masques respiratoires
Outre l’application de ces masques lors de soins à des patients souffrant de maladies pouvant se propager par voie aérienne et/ou de maladies infectieuses hautement contagieuses, le port de masques respiratoires est également préconisé durant l’utilisation confinée en laboratoire d’organismes génétiquement modifiés et/ou hautement contagieux (13).
a) Masque respiratoire jetable
Dans le cadre des soins de santé, ce sont les masques de type jetable qui sont le plus souvent utilisés. Le port d’un masque respiratoire à haute efficacité filtrante est préconisé pour assurer la protection personnelle vis-à-vis de maladies infectieuses ayant une transmission par voie aérienne (« airborne ») comme la tuberculose, la rougeole, la varicelle. La propagation par voie aérienne se fait par des petites particules de poussière de moins de 5 micromètres (également appelées gouttelettes desséchées ou « droplet nuclei ») qui contiennent des micro-organismes et peuvent rester en suspension dans l’air pendant une période prolongée. Les micro-organismes peuvent dès lors se propager sur une grande distance et être inhalés par des personnes qui se trouvent dans un même espace (p.ex. la chambre du patient, l’unité/service). C’est la raison pour laquelle des conditions spéciales de traitement de l’air et de ventilation (chambres en dépression) sont nécessaires pour prévenir la transmission par voie aérienne. L’accès à une pièce affichant une concentration élevée de ces gouttelettes peut entraîner une contamination en l’absence du port de masque adapté. Les masques respiratoires doivent pouvoir filtrer ces gouttelettes.
Pratiquement, cela signifie que, dans le cas de chambres d’isolement hébergeant des patients atteints des affections précitées, le port du masque est indiqué avant d’entrer dans la pièce et il ne faut l’enlever qu’après avoir quitté la pièce. Cette mesure de précaution s’applique également lorsque le patient ne se trouve pas dans sa chambre.
Un masque de classe FFP2 minimum est recommandé pour les soins aux patients tuberculeux. Le masque FFP3 est à privilégier pour les patients qui souffrent de tuberculose à germes multirésistants (16).
b) Systèmes motorisés (« Powered Air Purifying Respirator » (PAPRs))
Ces dispositifs (avec casque ou cagoule) ne sont préconisés que pour les cas de maladies infectieuses hautement contagieuses tels le syndrome respiratoire du Moyen-Orient (MERS) à MERS-coronavirus et les fièvres hémorragiques (17). De tels systèmes sont utilisés notamment dans l’unité de haut isolement (High Level Isolation Unit, HILU) à l’UZA (figure 3). Dans ces systèmes, l’air est aspiré à travers les filtres à l’aide d’un ventilateur. Les unités motorisées éliminent ainsi la résistance respiratoire (il ne faut pas respirer par un filtre) et conviennent aux porteurs de lunettes et pour les personnes barbues.
Des systèmes motorisés similaires (« Orthopedic Surgical Space Suits » ou « Filtered-Exhaust Helmets ») sont parfois également utilisés notamment dans le cadre de la chirurgie orthopédique avec insertion de matériel prothétique. Les Centres pour le contrôle et la prévention des maladies (CDC) ne se prononcent cependant pas sur la question dans les recommandations de 2017, en raison du manque de preuves concernant le bénéfice de ces dispositifs très onéreux dans le cadre de la prévention d’ISO (18). S’Il est vrai que le porteur est protégé contre les éclaboussures de sang, il existe néanmoins d’autres type de protections (p.ex. « facial shields ») tout aussi efficaces et moins coûteuses. L’efficacité de ces systèmes motorisés n’est pas clairement établie pour la protection contre les infections transmises par voie aérienne ; ces dispositifs ne sont en outre pas vendus sur le marché en tant que masques respiratoires.
Les systèmes motorisés sont également subdivisés en trois classes de performance, à savoir TH1, TH2 et TH3, où l’abréviation TH signifie « Turbo Hood » (tableau 4). La norme européenne EN 12941 définit trois classes de performances. Les chiffres du tableau 4 renseignent l’exigence de performance (fuite totale vers l’intérieur en %) ainsi que la résistance à la traction des tuyaux et raccords pour chaque classification.
Tableau 4 : exigences de performance selon la norme EN 12941:1998/A2:2008
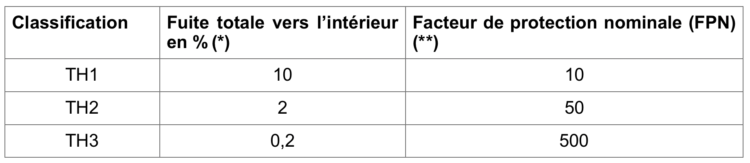
(*) Le niveau de fuite totale de vers l’intérieur réfère à la fois à l’efficacité de filtration inhérente au type de masque, à son degré de fuite (p.ex. au niveau des connexions avec le filtre) let également au degré de fuite vers l’intérieur entre la peau et le masque dans des conditions simulées de port chez des volontaires.
(**) Selon la norme européenne EN 12941: 1998/A2 :2008, le facteur de protection nominale (FPN) = 100 / fuite totale vers l’intérieur (%)..Au plus la valeur du FPN est élevée, au plus le masque est efficace et la fuite vers l’intérieur basse. Ce facteur de protection indique donc la relation entre le niveau de contamination de l’air à l’extérieur et celui de l’air inspiré (à l’intérieur).
C) Masques pour un patient souffrant d’une affection transmissible par voie aérienne
Les masques respiratoires avec valve respiratoire ne peuvent évidemment pas être portés par des patients souffrant d’une affection transmissible par voie aérienne lorsqu’ils quittent la chambre d’isolation pour se rendre à un examen. Ils portent donc un masque sans valve respiratoire ou un masque chirurgical.
Le port d’un masque sans valve respiratoire par le patient a pour but de réduire au maximum la contamination de l’air ambiant. Le masque forme une barrière vis-àvis des gouttelettes et empêche dès lors la formation d’aérosols. La recommandation du Conseil Supérieur de la Santé (CSS n°8579, Novembre 2013) stipule que tout patient atteint de tuberculose contagieuse (suspectée ou confirmée) doit porter un masque chirurgical (norme EN 14683 : 2006) lorsqu’il quitte la chambre d’isolement aérien. Les CDCs stipulent également que les patients souffrant de tuberculose doivent, outre le respect des mesures d’hygiène pendant la toux, porter un masque chirurgical et que le port d’un masque respiratoire par ces patients n’est pas nécessaire. En cas de tuberculose multirésistante, le port du masque est recommandé pendant les soins de longue durée effectués dans la chambre ainsi que lors des visites de la famille. L’utilisation appropriée du masque (pourquoi et comment il faut le porter) doit être bien expliquée au patient. Ce dernier doit recouvrir à la fois le nez et la bouche, et être suffisamment solide que pour résister à des sécrétions générées par la toux ou par des éternuements. Un masque résistant aux éclaboussures, conçu avec une couche plus résistante aux liquides, est préférable (type IR ou IIR selon la norme européenne). Il doit être changé lorsqu’il devient humide ou lorsqu’il se déchire (16,19).
D) Résumé des indications
Le tableau 5 reprend quelques exemples d’indications non limitatives pour un masque respiratoire dans le secteur des soins de santé.
Tableau 5 : Indications masque respiratoire
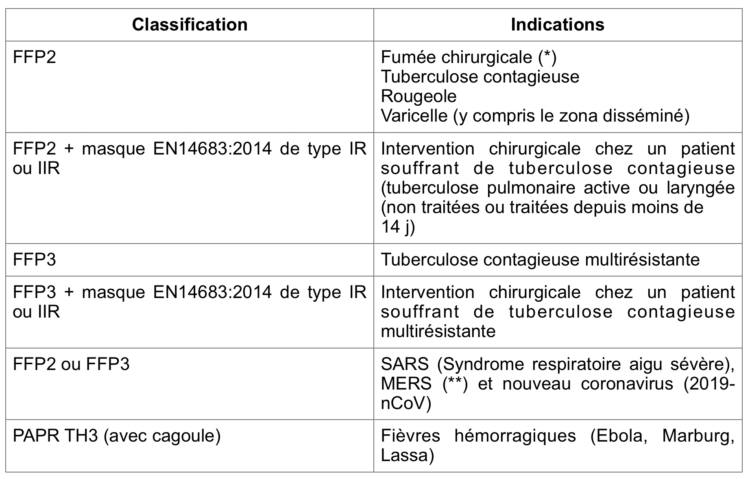
(*) Le “National Institute for Occupational Safety and Health” (NIOHS) recommande le port d’un masque respiratoire plutôt qu’un masque chirurgical spécifiquement en cas d’absence de systèmes d’aspiration de fumée ou en cas de fonctionnement suboptimal. Par ailleurs, le NIOHS recommande le port de masque respiratoire dans le cadre d’interventions reconnues associées à un risque de pathologies infectieuses transmissibles telles l’infection à HPV (19).
(**) L’Organisation Mondiale de la Santé (OMS) mentionne dans sa recommandation de 2014 le port d’un masque respiratoire de classe FFP2 ou FFP3 (20), tandis que dans une recommandation de protocole de prise en charge du MERS datant d’août 2019, Sciensano renseigne également le port d’un système motorisé (PAPR) mais sans donner plus de détails sur cette indication (21).
4. Comment porter un masque respiratoire ?
Compte tenu de la diversité des modèles et marques sur le marché, il est important d’utiliser le masque conformément aux directives du fabricant. En présence d’un arceau nasal, comme dans le type jetable, il doit d’abord être mis en forme en étant plié légèrement au milieu. Le masque doit recouvrir entièrement la bouche et le nez. Il est important de n’avoir aucune fuite. Il est possible de le vérifier facilement en inspirant profondément et expirant vigoureusement en cas de masque avec valve respiratoire. Si de l’air s’échappe au niveau de l’arceau nasal, il doit être remodelé. Les fuites latérales peuvent éventuellement être résolues par le repositionnement des lanières ou la remise en place du masque.
La morphologie du visage peut cependant être très différente d’une personne à l’autre. Il est dès lors peu probable qu’un modèle spécifique convienne à tous. D’autres facteurs peuvent avoir une influence sur l’étanchéité d’un masque respiratoire, tels :
- La pilosité faciale. Les personnes qui portent un masque respiratoire ajusté doivent être rasées de près au niveau des bords du masque ;
- Les lunettes. Des lunettes, qu’elles soient sur ordonnance ou de sécurité, ont également une influence sur l’étanchéité du masque et la personne qui porte des lunettes doit également les porter lors du fit testing ;
Fit testing
Outre l’efficacité de filtration et le confort, la forme (fit) du masque est également essentielle à une bonne protection. Pour déterminer si le masque a la forme adéquate, on réalise un test d’étanchéité (fit test). Ce type de test permet de détecter la présence éventuelle de fuites latérales et peut contribuer à une bonne étanchéité faciale. Il existe des méthodes qualitatives et quantitatives pour la réalisation du fit test. Le fit test qualitatif évalue la simplement la capacité de détection (qualitative) d’un goût, d’une odeur ou d’une fumée irritante par le porteur du masque. Ce test s’utilise aussi bien pour les masques jetables (uniquement test de goût) que pour les demi-masques filtrants. Le fit test quantitatif évalue la fuite en créant une dépression et mesure le nombre de particules présentes dans le masque et en dehors de celui-ci. Cette méthode convient pour les masques jetables, les demi-masques filtrants réutilisables ainsi que pour les masques complets réutilisables (22,23).
III. Références
- British Standards Institution. Medical face masks – Requirements and test methods. 30/04/2014.
- Van Laer F. Masques chirurgicaux. Noso-info, 2005; Vol. IX (2):15-17.
- Werkgroep Infectiepreventie (WIP). Infectiepreventie bij gebruik van laserapparatuur. Juin 2013.
- Vroegop JEM. Chirurgische rook maakt meer kapot dan je lief is. Een literatuurstudie naar de schadelijke effecten. Tijdschrift voor Hygiëne en Infectiepreventie, 2002;1:7-9.
- Werkgroep Infectiepreventie (WIP). Infectiepreventie bij het gebruik van laserinstrumentarium. Juin 1997.
- Uday Kelkar, Bageshri Gogate, Satish Kurpad et al. How effective are face masks in operation theatre? A time frame analysis and recommendations. Int J Infect Control 2013, v9:i1 doi: 10.3396/ijic.v9i1.003.13.
- Campagne gesteund door Mölnlycke Health Care. Aanstekelijk.be. Het gebruik van chirurgische maskers: OK in uw OK? Janvier 2010.
- CCLIN Sud-Ouest – Groupe Hospitalier Pellegrin. Recommandations pour l’utilisation des masques médicaux et des appareils de protection respiratoire dans les établissements de santé, 2006.
- Woodhead K, Taylor EW, Bannister G et al. Behaviours and rituals in the operating theatre. Journal of Hospital Infection, 2002;51: 241-255.
- WIP. Preventie van postoperatieve wondinfecties. Révision : mai 2011.
- Conseil Supérieur de la Santé Recommandations pour la prévention des infections post-opératoires au sein du quartier opératoire. Mai 2013. CSS n° 8573.
- McLure HA, Mannam M, Talboys CA et al. The effect of facial hair and sex on the dispersal of bacteria below a masked subject. Anesthesia, 2000 Feb;55(2):173-176.
- Institut scientifique de santé publique Emploi d’appareils de protection respiratoire durant l’utilisation confinée d’organismes génétiquement modifiés et/ou pathogènes (Gebruik van ademhalingsbeschermingsmiddelen bij het ingeperkt gebruik van genetisch gemodificeerde organismen en/of pathogenen),2007.
- Ka Man Wong C, Hon Kei Yip B, Mercer S et al. Effect of Facemasks on Empathy and Relational Continuity. BMC Fam Pract. 2013;14(200).
- Forgie SE, Reitsma J, Spady D, et al. The “fear factor” for surgical masksand face shields, as perceived by children and their parents. Pediatrics 2009;124:e777-e781.
- Conseil Supérieur de la Santé Avis n° 8579. Recommandations relatives à la prévention de la tuberculose dans les institutions de soins Novembre 2013
- Conseil Supérieur de la Santé Avis n° 9188. Recommandations pratiques concernant l’identification et la prise en charge de patients suspectés ou avérés être porteurs de virus hautement contagieux (de type Ebola ou Marburg) dans le cadre d’une bouffée épidémique en Afrique de l’Ouest, à l’attention des professionnels de la santé et des autorités sanitaires 4 juillet 2014.
- Berríos-Torres SI, Umscheid CA, Bratzler DW et al. Centers for Disease Control and Prevention Guideline for the Prevention of Surgical Site Infection, 2017. JAMA Surg., 2017;152(8):784-791. doi:10.1001/jamasurg.2017.0904.
- MMWR. Guidelines for Preventing the Transmission of Mycobacterium tuberculosis in Health-Care Settings, 2005;54;No. RR-17.
- World Health Organisation. Infection prevention and control of epidemic-and pandemic-prone acute respiratory infections in health care, 2014. WHO guidelines, april 2014.
- Sciensano. Procedure for case management for a suspicion of a middle east respiratory syndrome (MERS) coronavirus infection. Update August 2019.
- 3M. Zit uw masker goed? Fittest technische fiche. BSG 2015/13.072.
- Health and Safety Executive. Review of fit test pass criteria for Filtering Facepieces Class 3 (FFP3) Respirators. RR 1029, 2015.
Nouveautés
Agenda scientifique
- janvier 2026
-
27/01
Symposium georganiseerd door de BICS, ABIHH en WIN Opleiding van zorgprofessionals in infectie-preventie en controle (IPC)
- mars 2026
-
5/03
Kennis delen samen sterker – intercollegiale uitwisseling infectiepreventie (CONTRAIN)
-
21/03
Symposium Séminaire de diagnostic des maladies infectieuses.(SSID)
-
26/03
WZC symposium – zorginfecties en antimicrobiële resistentie (SCIENSANO)
- juin 2026
-
du 3/06 au 5/06 || à Lille
36ème Congrès de la Société Française en Hygiène Hospitalière (SF2H)


