UVC-robot: een noodzaak ? Stand van zaken in 2022.
Achtergrond
Sinds de SARS-CoV2 pandemie worden vanuit de industrie systemen voor “no touch automated room desinfection” (NTD) sterk gepromoot. Binnen ons ziekenhuis toont zowel de schoonmaakdienst als het bureau innovatie interesse voor het inzetten van een UVC looprobot (UVC-desinfectie met een autonoom gestuurde robot). Als onderdeel van het EU-programma om EU lidstaten te ondersteunen in de strijd tegen het coronavirus schonk de Europese commissie in 2021 maar liefst 200 UVC-looprobots (UVD robots – Blue Ocean Robotics) aan ziekenhuizen binnen de EU-lidstaten, 10 daarvan gingen naar ziekenhuizen binnen de Benelux 1. Dit gegeven versterkt de interne perceptie dat een robot met UV technologie in een innoverend ziekenhuis geïntroduceerd moet worden.
Fig. 1 Schoonmaakrobot inzetbaar voor vloeronderhoud
Robotisering binnen de schoonmaak is in opmars. Schoonmaakrobots worden voorgesteld om autonoom op basis van mapping navigatie vloeren te reinigen (Figuur 1). Nieuwe (semi-)automatische technologie kan zeker de zorgsector helpen om het schoonmaakgebeuren doeltreffender en doelmatiger te maken. Gezien een gecontamineerde ziekenhuisomgeving kruisbesmettingen in de hand werkt, kan dit alleen maar toegejuicht worden. Manuele reiniging/desinfectie is arbeidsintensief en handmatig terminaal onderhoud verloopt vaak suboptimaal 2,3. Een geautomatiseerde no touch terminale desinfectiemethode elimineert onnauwkeurigheden en variatie inherent aan menselijke arbeid, verzekert een constante (hoge) kwaliteit met mogelijkheden tot monitoring.
Op dit ogenblik zijn er op de markt 3 NTD systemen: waterstofperoxideverneveling (natte nevel), waterstofperoxide aërolisatie (droge mist) en inzetten van UVC-lichtbron. Al deze NTD systemen veronderstellen wel dat voorafgaandelijk een degelijke manuele reiniging van de te behandelen lokalen/ruimtes gebeurde 4-6. De onderlinge keuze gebeurt door rekening te houden met de bewezen antimicrobiële werkzaamheid, procesdoorlooptijd, kostprijs van toestel/desinfectiecyclus/onderhoud, evt. beperkingen door volume of design kamer, logistieke vereisten, mogelijkheden tot procesvalidatie (via traceersystemen en/of specifieke teststrips), veiligheid voor personeel en patiënten. Bij alle NTD systemen geldt dat blootstelling van mensen tijdens een lopend desinfectieproces moet vermeden worden.
In AZ Groeninge werd in het verleden, naar aanleiding van een uitbraak met een OXA-24 carbapenemase-producerende multidrug resistente Acinetobacter baumannii, de keuze gemaakt voor waterstofperoxideverneveling met Aerosept compact 250. Dit toestel vernevelt Aseptanios AD (een oplossing van waterstofperoxide en perazijnzuur). De keuze destijds was o.a. gebaseerd op bewezen antimicrobiële activiteit conform NF T 72-281, louter bio-afbreekbare ingrediënten in de verneveloplossing met afwezigheid van zilvermoleculen, mogelijkheid tot uitlezing van het desinfectieproces, kostprijs en beschikbaarheid van 1 prospectieve cohort gerandomiseerde controlestudie7. Waterstofperoxideverneveling wordt nog steeds actueel ingezet in de terminale kamerdesinfectie bij carbapenemase-producerende Enterobacteriaceae, carbapenemase-producerende multidrug resistente Acinetobacter baumannii, VRE en Norovirus aanvullend op een handmatige kamerreiniging-en desinfectie. Bij deze pathogenen is een NTD aangewezen gezien de literatuur duidelijk beschrijft dat opname in een kamer waar de vorige patiënt gekoloniseerd of geïnfecteerd was met een van deze pathogenen een duidelijk verhoogd risico inhoudt voor een nieuwe patiënt om deze kiem ook te verwerven daar het pathogenen betreft die dagen tot maanden op gecontamineerde oppervlakken in de kamer weten te overleven 3,8 .
Hoewel het gebruik van NTD systemen steeds meer ingeburgerd raakt binnen Belgische ziekenhuizen wordt de vraag naar overtuigend wetenschappelijk bewijsvoering die aantoont dat de toepassing van NTD voor desinfectie van patiëntenkamers in ziekenhuizen leidt tot verminderd aantal zorginfecties te weinig gesteld. Een systematische review van Dancer & King biedt hierin een verhelderend antwoord 9.
Terwijl in vitro studies duidelijk een reductie van de bioburden aantonen 9 vormt het bewijzen van het klinisch impact van deze NTD systemen een veel grotere uitdaging 10,11. Bij het volgen van de indeling van evidentie niveau’s voorgesteld door McDonald kan men 4 niveau’s onderscheiden (zie figuur 2)12.
Fig. 2 Evidentiehiërarchie van “no touch” technologie studies (McDonald model aangepast door De Bel 2017) 11 (niveaus 3 en 4 vertegenwoordigen de klinische impact in termen van reductie in het verwerven van infecties en in het aantal overdrachten)
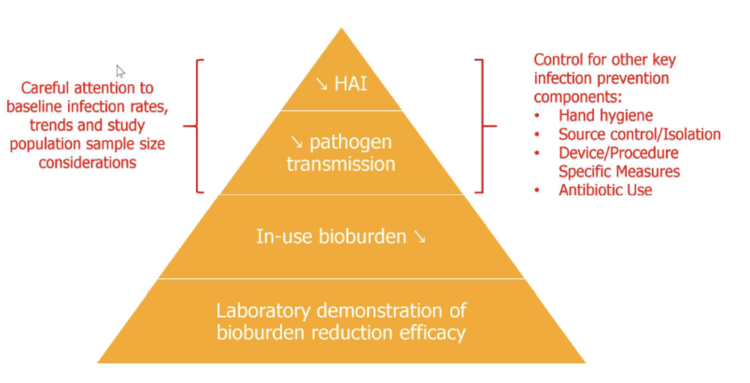
Niveau 1 (basis van de evidentiepiramide) bestaat uit laboratoriumstudies waarbij de werkzaamheid van de techniek onderzocht wordt in intentioneel gecontamineerde kamers. Het inoculum gebruikt in deze studies is vaak zeer hoog en is eerder bedoeld om de maximale reductiecapaciteit van de techniek te testen, eerder dan een realistische besmettingsgraad van kamers te simuleren. De resultaten van dit type studies worden dan ook vaak uitgedrukt in log10 reductiecapaciteit. Studies van niveau 2 evalueren de reductie van de besmettingsgraad van de high touch oppervlakken in reële contactisolatiekamers na versus vóór behandeling. Daar de bioburden in deze kamers veel lager is dan bij studies van niveau 1, is het weinig zinvol deze resultaten uit te drukken in log10 reductiecapaciteit maar wordt hier meestal gewerkt met percentage positieve plaatsen na versus vóór behandeling. Studies van niveau 3 en 4 leveren de meest waardevolle klinische informatie, maar zijn moeilijk uit te voeren daar veel “confounding factors” op de loer liggen. Deze studies gaan respectievelijk de verticale transmissie en het aantal infecties met nosocomiale pathogenen na 11.
In de systematische review van Dancer en King werden 43 studies gepubliceerd in de periode 2005-2020 weerhouden 9.
Vierentachtig procent van deze niveau 3 en niveau 4 studies hadden een before-and-after design waardoor het aantonen van een positief effect van NTD gebruik op patient outcomes wordt bemoeilijkt. In pre-poststudies worden vaak mogelijke verstorende variabelen zoals patiëntenkenmerken, infectiepreventiepraktijken en zorgaspecten vóór en na onvoldoende geïdentificeerd en gecontroleerd 13. Dit onderzoeksdesign levert daardoor onvoldoende betrouwbare robuuste evidentie aan.
Ultraviolet (UV) licht is onzichtbaar voor het menselijk oog en wordt onderverdeeld in UV-A, UV-B en UV-C. UV-C is aanwezig in het golflengtebereik van 100-280 nm. Professionele geïoniseerde kwiklampen produceren vooral UVC-licht met een golflengte van 254 nm,d.i. de golflengte met de krachtigste desinfecterende werking (zie figuur 3).
Figuur 3. Celdeactivering van micro-organismen door UV-C licht
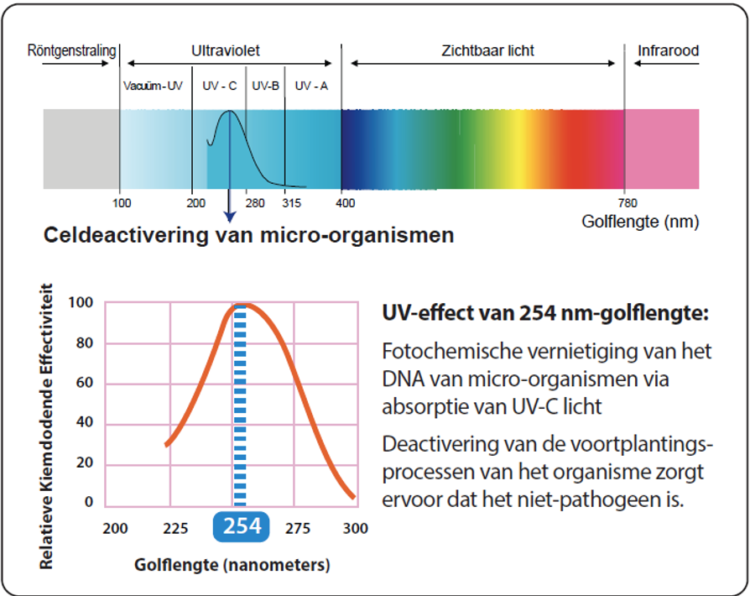
UVC licht verstoort het DNA/RNA van pathogenen en voorkomt dat ze zich verder kunnen vermenigvuldigen. De effectieve weerstand van micro-organismen tegen UV-C-straling verschilt aanzienlijk, het aantal mJ/cm2 om een voldoende log reductie te bekomen varieert naargelang het af te doden micro-organisme. UVC desinfectie is een line of sight technologie d.w.z. directe blootstelling van oppervlakken aan UVC licht is noodzakelijk om een kiemdodend effect te bekomen, schaduwplaatsen worden niet bereikt en niet ontsmet. Om die reden kunnen UVC-robots nooit volledig autonoom instaan voor een kamerdesinfectie. Ook de afstand tot de UVD lichtbron is belangrijk. De intensiteit van de UV-straling is omgekeerd evenredig met het kwadraat van de afstand tussen de UV-lamp en het blootgestelde oppervlak. Het ontwerp van de mobiele UVC lichtbron kan verschillen naargelang de fabrikant met impact op de performantie. In tegenstelling tot NTD op basis van waterstofperoxide waarbij de antimicrobiële doeltreffendheid van de aërogene desinfectie kan afgetoetst worden volgens de EN 17272 bestaat er voor het aantonen van de antimicrobiële doeltreffendheid van UVC geen internationaal uniforme teststandaard. Dit bemoeilijkt het onderling vergelijken van diverse UVC systemen op de markt.
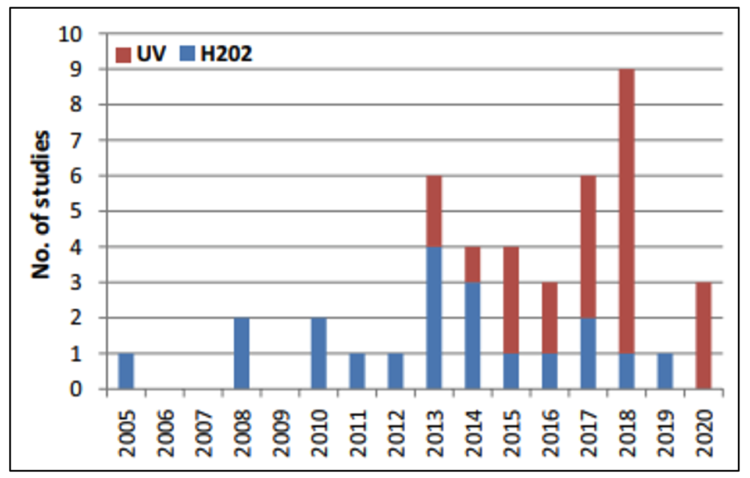
Figuur 4 geeft een duidelijke opmars aan van publicaties over UVC, opvallend geen enkele studie is van Europese bodem.
Fig. 4 Overzicht aantal jaarlijkse publicaties per NTD type (UVC vs H2O2) in periode 2005-2020 9. Geen Europese, wel hoofdzakelijk Noord-Amerikaanse UVC studies.
Aanhangers van mobiele UVC-desinfectiesystemen verwijzen graag naar 2 publicaties die onderdeel uitmaken van de BETR studie (Benefits of Enhanced Terminal Room Disinfection Study). In 2017 publiceerden Anderson et al. de resultaten van een pragmatische cluster-gerandomiseerde cross-over studie waarbij het effect van 4 verschillende regimes voor terminale kamerdesinfectie werd bestudeerd op het in het ziekenhuis verwerven van resp. Clostridiodes difficile, MRSA, VRE en multidrug resistente Acinetobacter baumannii 14. De vergeleken werkwijzen voor terminale kamerdesinfectie waren: desinfectie met een quaternaire ammoniumderivaat en enkel in geval van Clostridiodes difficile gebruik van bleekwater (“referentie” genoemd), referentie met aanvullend UVC, desinfectie met bleekwater, desinfectie met bleekwater met aanvullend UVC. Tijdens de 2 jaar durende studieperiode werden 31 226 patiëntenkamers (21 395 patiënten goed voor 97 833 blootstellingsdagen) opgenomen voor de intention-to-treat analyse. Alle patiënten waren min. 24 uur gehospitaliseerd en community-acquired dragerschap/infectie voor de bestudeerde pathogenen werd uitgesloten. Het relatief risico voor het verwerven van Clostridiodes difficile, MRSA, VRE of multidrug resistant acinetobacter baumannii vergeleken met de “referentie” bedroeg 0.70 (95% B.I. 0.5-0.98) in de UVC-groep, 0.85 (95% B.I. 0.69-1.04) in de bleekwatergroep en 0.91 (95% B.I. 0.76-1.09) in de bleekwater met aanvullend UVC. De pathogeen specifieke resultaten zijn veel minder overtuigend en tonen voor Clostridiodes difficile, MRSA en VRE geen significante reductie t.g.v. UVC. Over multidrug resistant acinetobacter baumannii kon men geen uitspraak doen gezien er zich slechts 1 casus voordeed in de gehele studieperiode.
In 2018 publiceerden Anderson at al. de resultaten van een secundaire analyse op data verzameld tijdens de BETR studie15. Dit maal werden alle patiënten min. 48u gehospitaliseerd opgenomen in de studie met exclusie van deze met community-acquired dragerschap/infectie voor Clostridiodes difficile MRSA, VRE of multidrug resistant acinetobacter baumannii. Er werden 31 4637 opnames, goed voor 1 169 416 patiëntdagen, bestudeerd. Enkel voor Clostridiodes difficile en VRE kon een significante risicoreductie bij gebruik van UVC aangetoond worden. Het relatief risico voor het verwerven van Clostridiodes difficile vergeleken met de “referentie” bedroeg 0.89 (95% B.I. 0.80-0.99), het relatief risico voor VRE vergeleken met de “referentie” bedroeg 0.56 (95% B.I. 0.31-0.99) in de UVC-groep. De bekomen resultaten liggen volledig in lijn met deze van de systematische review en meta-analyse van Marra, Schweizer en Edmond 16.
Hoewel NTD een toegevoegde waarde kan bieden, is tot op heden de evidentie m.b.t. de reductie van zorginfecties beperkt.
Waterstofperoxide NTD’s zijn tijdrovend, relatief omslachtig en vaak is er een probleem van gebrekkige procescontrole en/of duidelijke criteria zoals noodzakelijk te bereiken ppm waterstofperoxide om een cyclus als eindgebruiker te valideren, hetgeen geen overbodigheid is gezien elke ruimte verschillend is 11.
UVC decontaminatie biedt een aantal voordelen t.o.v. waterstofperoxide. Geen specifieke voorbereiding of nazorg vereist van de te desinfecteren ruimte, geen gebruik van chemicaliën, afwezigheid van evt. toxische residuen (zilverpartikels), een procesdoorlooptijd van minuten i.p.v. uren, na desinfectie is de behandelde ruimte onmiddellijk opnieuw toegankelijk en gebruiksklaar. Echter, net zoals bij NTD op basis van waterstofperoxide, is er ook in UVC-oplossingen behoorlijk wat variatie op de markt. In tegenstelling tot waterstofperoxide decontaminatie – die een volledige kamerdesinfectie kan claimen – zal UVC decontaminatie zich enkel beperken tot die plaatsen die door de eindgebruiker als risicovol in de overdracht van zorginfecties zijn bepaald en effectief voldoende lang en op de juiste afstand werden blootgesteld aan UVC licht.
Conclusie
Gepubliceerde NTD studies hebben vaak een gebrekkig studiedesign en zijn overwegend door de industrie gesponsord. Een zorgvuldige kosten-baten analyse moet gebeuren, tot op heden zijn er geen studies die een kostenbesparing kunnen aantonen9. Implementatie van een goed professioneel schoonmaakprogramma is een noodzaak alvorens te investeren in nieuwe NTD technologie. “One wipe, one site and one direction with detergent and water is easy, cheap and effective and will not upset the surface ecology or create a futuristic superbug” 9. NTD kunnen een toegevoegde waarde bieden maar wie denkt hiermee schoonmaakpersoneel te kunnen uitsparen heeft het mis.
Bibliografie
1. -, Coronavirus: 200th EU disinfection robot delivered to European hospital, a further 100 confirmed, European Commission, press corner, daily news 21/09/2021.
2. Carling P.C. et al., Improving cleaning of the environment surrounding patients in 36 acute care hospitals, Infect Control Hosp Epidemiol, 2008 nov, 29(11):1035-41.
3. Otter J.A., Evidence that contaminated surfaces contribute to the transmission of hospital pathogens and an overview of strategies to adressed contaminated surfaces in hospital settings, Am J Infect Control, 2013, may, 41(5 suppl):S6-11.
4. Boyce J.M., Modern technologies for improving cleaning and disinfection of environmental surfaces in hospitals, Antimicrob Resist Infect Control, 2016:5:10.
5. Carling P.C., The need for clinical relevant studies of no-touch disinfecting systems, J Hosp Infect, 2013:84:33940.
6. Dancer S.J., Floor wars: the battle for clean surfaces, J Hosp Infect, 2013:84:339-340.
7. Passaretti C.L. et al., An evaluation of environmental decontamination with hydrogen peroxide vapor for reducing the risk of patient acquisition of multidrug-resistant organisms, Clin Infect Dis, 2013:56 (1 january), 27-35.
8. Mitchell B.G. et al., Risk of organism acquisition from prior room occupants: a systematic review and meta-analysis, J Hosp Infect, 2015, 91:211-17.
9. Dancer S.J., KingM., Systematic review on use, cost and clinical efficacy of automated decontaminatjon devices, Antimicrob Resist Infect Control, 2021, 10:34.
10. Weber D.J. et al., Effectiveness of ultraviolet devices and hydrogen peroxide systems for terminal room decontamination: focus on clinical trials, Am J Infect Control, 2016, 44:e77-84.
11. De Bel A., Kamerdecontaminatie met “no touch” technologie: vergelijkende studie tussen waterstofperoxide en quaternaire ammoniumderivaten, ManaMa ziekenhuishygiëne, Universiteit Gent, 2017, 49pp.
12. McDonald L.C., Arduino M., Climbing the evidentiary hierachy for environmental infection control, Clin Infect Dis, 2013 january, 56(1):36-39.
13. Caluwaerts A. Is UV-straling het nieuwe wondermiddel om patiëntenkamers te desinfecteren?, examenopdracht Evidence Based Heathcare Critically Appraised Topic, KU Leuven, 2020.
14. Anderson D.J. et al., Enhanced terminal room disinfection and acquisition and infection caused by multidrug-resistant organisms and Clostridium difficile (the Benefits of Enhanced Terminal Room Disinfection study): a cluster-randomised, multicentre crossover study, The Lancet, 2017, jan 16.
15. Anderson D.J. et al., Effectiveness of targeted enhanced terminal room disinfection on hospital-wide acquisition and infection caused by multidrug-resistant organisms and Clostridium difficile: a secondary analysis of a multicentre cluster randomised controlled trail with crossover design (BETR Disinfection), Lancet infect Dis, 2018, june 4.
16. Marra A.R., (M.L.), (M.L.) Schweizer, (M.B.) Edmond, No touch disinfection methods to decrease multidrugresistant organism infections: a systematic review and meta-analysis, Infect Control Hosp Epidemiol, 2017, 1-12.
17. Reiser GR, Moskal JT. Cost Efficacy of Methicillin-Resistant Staphylococcus aureus Decolonization With Intranasal Povidone-Iodine. The Journal of Arthroplasty. Elsevier, 2018, Vol. 33, 1652-1655.
18. 3M Infection Prevention Division. Safety & Efficacy Information 3M Skin and Nasal Antiseptic. USA : s.n., 2016.
19. Ghaddara HA, Kumar JA, Cadnum JL, Ng-Wong YK, Donskey CJ. Efficacy of a povidone iodine preparation in reducing nasal methicillin-resistant Staphylococcus aureus in colonized patients. American Journal of Infection Control. Elsevier, 2020, Vol. 48, 456-459.
20. Hill RLR, Casewell MW. The in-vitro activity of povidone–iodinecream against Staphylococcus aureus and its bioavailability in nasal secretions. Journal of Hospital Infection. Elsevier, 2000, Vol. 45 (3).
21. Simor EA, Stuart TL, Louie L, Watt C, Ofner-Agostini M, Gravel D, Mulvey M, Loeb M, McGeer A, Bryce E, Matlow A, and the Canadian Nosocomial Infection Surveillance Program. Mupirocin-Resistant, Methicillin-Resistant Staphylococcus aureus strains in canadian hospital. Antimicrobial Agents and Chemotherapy. American Society of Microbiology, 2007, Vol. 51(11), 3880-3886.
22. Rezapoor M, Nicholson T, Mostafavi Tabatabaee R, Chen AF, Maltenfort MG, Parvizi J. Povidone-iodine-Based Solutions for Decolonization of Nasal Staphylococcus aureus : A Randomized, Prospective, Placebo-controlled Study. The Journal of Arthroplasty. Elsevier, 2017, Vol. 32, 2815-2819.
Nieuwigheden
Wetenschappelijke agenda
- oktober 2024
-
van 16/10 tot 20/10 || in Los Angeles
SHEA ID week. A joint meeting of IDSA, SHEA, HIVMA, PIDS and SIDP
- november 2024
-
van 20/11 tot 22/11 || in Liverpool
Healthcare infection society
- april 2025
-
van 11/04 tot 15/04 || in Wenen
Congrès de l’ European Society of Clinical Microbiology and Infectious Diseases (ESCMID)
- juni 2025
-
van 4/06 tot 6/06 || in Marseille
35ème Congrès National de la Société Française d’Hygiène Hospitalière (SF2H)
-
van 17/06 tot 18/06 || in Londen
HIS congres (Healthcare Infection Society)



