Kenmerken en klinische evolutie van 29 OXA-48-achtige infecties door carbapenemaseproducerende enterobacteriën in een Belgisch perifeer ziekenhuis.
Inleiding
Sinds verschillende jaren neemt het aantal infecties door carbapenemaseproducerende enterobacteriën (CPE) overal ter wereld toe (1). Uit de eerste in 2013-2014 uitgevoerde Europese surveillancestudie (EuSCAPE studie) voor klinische ziekenhuisstammen van Klebsiella pneumoniae en Escherichia coli CPE bleek een incidentie van 1.3 patiënten/10 000 opnames, zijnde 2.5 patiënten/100 000 hospitalisatiedagen (1). De maximale incidentie deed zich voor in de landen rond de Middellandse Zee en in de Balkanregio.
In deze studie waren de predominante carbapenemasen voor de Klebsiella pneumoniae-stammen van het type KPC (45%), gevolgd door die van het OXA-48-achtige type (37%). Voor E. coli was OXA-48-achtig predominant (56%), gevolgd door NDM (26%).
De in België aangetroffen incidentie in EuSCAPE voor Klebsiella pneumoniae en E. coli CPE bedroeg 0 .124/10 000 opnames in 2013 en 0.223 /10 000 opnames in 2014 (2).
Voor Klebsiella pneumoniae was OXA-48-achtig goed voor 37% van de carbapnenemasen tegenover 31% voor E. Coli (1).
Tussen 2012 en 2015 is de CPE-incidentie in de klinische stalen van Belgische ziekenhuizen gestegen van 0.25% naar 0.55% (3). Deze verhoogde incidentie van CPE is zorgwekkend omdat die infecties met een verhoogd sterftecijfer worden geassocieerd. Een beperkt aantal antibiotica is op deze bacteriën actief (4-10). Gelet op het geringe aantal gerandomiseerde studies dat kon worden uitgevoerd (7-10), is de optimale behandeling van die infecties nog altijd voer voor discussie. In ons ziekenhuis werden in de periode januari 2016 tot oktober 2017, 29 gevallen van CPE-infecties geregistreerd. Alle waren van het OXA-48-achtige type. De patiëntendossiers werden opnieuw doorgenomen om deze infecties nauwkeuriger te kenmerken en ze op die manier beter te kunnen aanpakken.
Methodologie
1. Inzamelen van de klinische gegevens:
De patiëntendossiers waarin sprake was van een CPE-infectie in het CHU Tivoli in de periode januari 2016 tot oktober 2017 werden opnieuw bekeken. Het CHU Tivoli is een perifeer ziekenhuis met 518 bedden, met een jaarlijks aantal opnames van 20 984 patiënten in 2016 en 17 745 (januari tot oktober 2017) voor 138 550 hospitalisatiedagen in 2016 en 115 131 (januari-oktober 2017). Het type infectie werd geclassificeerd op basis van de diagnose van de clinicus op het ogenblik dat de patiënt werd behandeld en van de beschikbare microbiologische resultaten. Een ernstscore voor deze infecties kon achteraf niet worden uitgevoerd. De klinische kenmerken van de patiënten werden verzameld (demografische gegevens, hospitalisatie-eenheid op het ogenblik van de infectie en co-morbiditeitfactoren). Het met deze infecties geassocieerde sterftecijfer werd op de veertiende dag geregistreerd. Patiënten werden onderverdeeld in «overlevenden» en «niet-overlevenden» om een potentieel profiel te identificeren, dat geassocieerd werd met een klinisch falen om deze CPE OXA-48-achtige infecties te behandelen.
2. Microbiologische bepaling van de carbapenem-resistentie
De carbapenemaseproductie werd vermoed via de schijfjesdiffusiemethode volgens de EUCAST 2016-criteria (11). Voor het bepalen van de productie van het enzym OXA-48-achtig werd gebruik gemaakt van de immunochromatografische methode (OXA-48 K-Set, Coris BioConcept®, Belgium). Voor het bepalen van de minimale inhibitorische concentraties (MIC) voor meropenem werd gebruik gemaakt van de E-test-methode (Biomérieux®). De MIC voor colistine werd bepaald via de E-test-methode (Liofilchem®) voor 24 van de infecties en via de microverdunningsmethode voor de 5 andere (Liofilchem® SensiTest Colistin). De stammen werden niet systematisch naar het referentielaboratorium van de gram-negatieve bacillen (GNB) gestuurd. De waarden van de MIC voor meropenem werden onderverdeeld in 7 categorieën, verdeeld over de waarden < 1 µg/ml tot ≥ 32 µg/ml.
3. Verzamelen van gegevens over de antibioticabehandeling:
De behandelingen die werden toegediend werden onderverdeeld als monotherapie, bitherapie, tritherapie en geen therapie. Volgende antibiotica werden gebruikt: meropenem, colistimethaatnatrium (colistine), tigecycline, trimethoprim/sulfamethoxazol, amikacine en nitrofurantoine. De oplaad- en onderhoudsdoseringen, en ook de wijze van toediening van de moleculen werden verzameld. Voor colistimethaat werd een oplaaddosering van 9 miljoen eenheden toegediend, ongeacht de nierfunctie. De eenheidsdosering meropenem bedroeg 1g voor de MIC < 2 μg/ml en 2g voor de MIC ≥ 2 <16 μg/ml. Meropenem werd in 3 uur geperfuseerd.
Resultaten
Bij de 29 CPE-infecties werden 34 enterobacteriën geïsoleerd en verschillende infecties waren polymicrobieel. Het geïdentificeerde type carbapenemase voor die 34 stammen was van het OXA-48-achtige type.
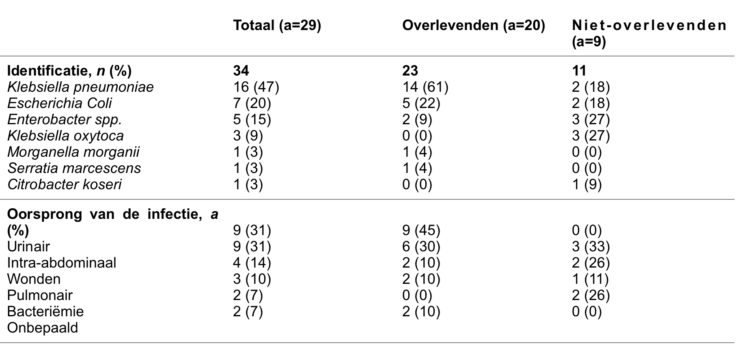
Twintig patiënten (69%) leefden nog op de veertiende dag van de infectie («overlevenden»), negen (31%) andere waren overleden («niet-overlevenden») (tabel 1). Van de 29 infecties was Klebsiella pneumoniae goed voor 47% van de stammen, gevolgd door E. Coli (20%). Klebsiella oxytoca en de Enterobacters spp overheersten voor 27% in de groep «niet-overlevenden». De oorsprong van de infectie was urinair in 31% van de gevallen, intra-abdominaal in 31%, het gevolg van een wonde in 14%, respiratoir in 10% en in 7% ging het om een bacteriëmie. In 7% van de gevallen kon de oorsprong van de infectie niet worden bepaald. Deze verdeling was verschillend voor de groepen «overlevenden» en «niet-overlevenden». In de eerste groep waren de meeste infecties urinair (45%), in vergelijking met de groep van de «niet-overlevenden», waarin de intra-abdominale infecties overheersten (33%), gevolgd door de bacteriëmieën (26%) en de wonden (26%).
Tabel 1: Identificatie en oorsprong van de 29 CPE OXA-48-achtige infecties (a=29):
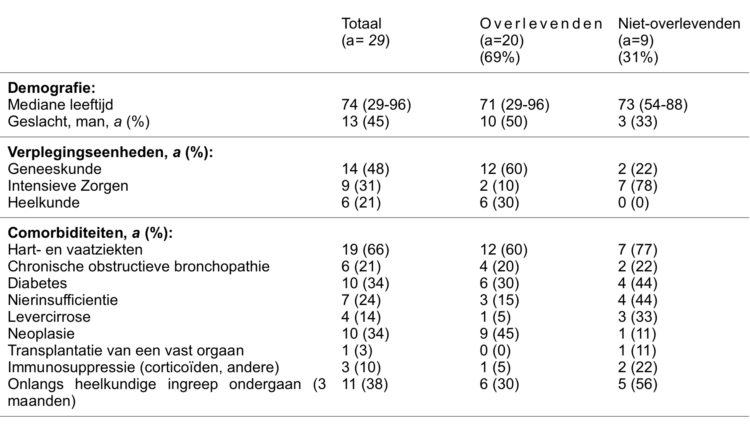
De mediane leeftijd van de patiënten was 74 jaar, met een meerderheid aan vrouwen (55%) (tabel 2). De meeste patiënten werden gehospitaliseerd in de geneeskundige eenheden (48%), vervolgens op Intensieve Zorgen (31%). In de groep «niet overlevenden» verbleef 78% van de patiënten op Intensieve Zorgen. Het aantal comorbiditeiten, zoals de aanwezigheid van een patiënt met diabetes (44%), met een nierinsufficientie (44%), een levercirrose (33%), die een immunosuppressieve therapie en onlangs een heelkundige ingreep heeft ondergaan (in de 3 voorafgaande maanden) waren talrijker in de groepen «niet-overlevenden».
Tabel 2: Kenmerken van de patiënten (a=29):
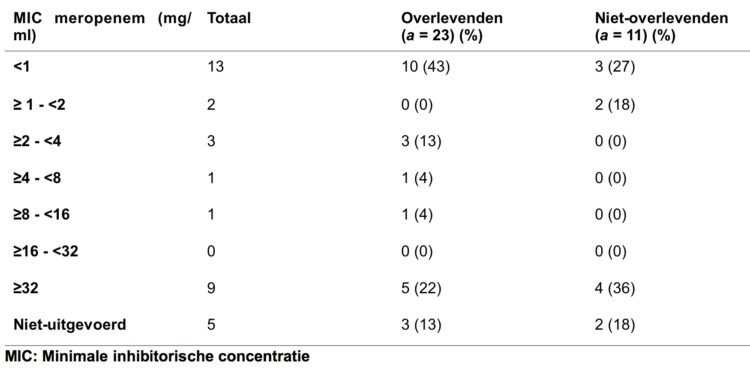
De MIC voor meropenem werd bepaald op 29 van de 34 klinische stammen (tabel 3). Voor de 5 andere werd de MIC bepaald op voordien uitgevoerde uitstrijkjes. De MIC voor de meeste stammen (13/29) was < 1 g/ml. Voor 9 stammen was de MIC zeer hoog (≥32 μg/ml), zonder bevestiging van die waarden door het referentielaboratorium. De hoge MIC waren dominant in de groep «niet-overlevende» patiënten (36%).
Tabel 3: Verdeling van de MIC voor meropenem voor de CPE
OXA-48-achtige stammen
De toegediende antibiotica werd bepaald door de infectioloog, in samenwerking met de clinicus, en was afhankelijk van de klinische toestand van de patiënt. Negenenvijftig procent van de patiënten kreeg een monotherapie, 31% een bitherapie (doorgaans in combinatie met meropenem of colistine) en 7% een tritherapie. Een patiënt op Palliatieve Zorgen werd niet behandeld. De keuze voor monotherapie, bitherapie of tritherapie werd bepaald door de ernst van de infectie en het CPE-antibiogram. Gelet op de ernstigere klinische toestand van die patiënten, waren de bi-therapieën in de groep «niet-overlevenden» (56%) dominant. De tritherapieën werden niet vaak voorgeschreven en waren niet altijd mogelijk, gelet op de resistentie van CPE tegen de verschillende in België in 2016-2017 uitgeteste en beschikbare antibiotica (tabel 4).
Tabel 4: Toegediende antibiotica 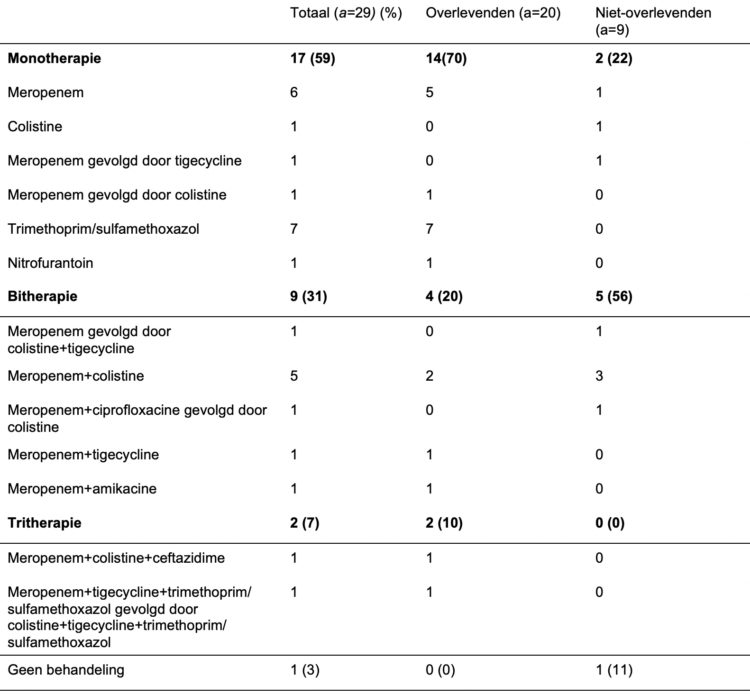
Discussie
De behandeling van CPE-infecties is voor elke clinicus een uitdaging. Weinig antibiotica helpen tegen CPE. Een hoge mortaliteit (tussen 39 et 71%) wordt geassocieerd met ernstige infecties, en met name voor de bacteriëmieën (4-10). In laatste instantie worden meestal colistine, tigecycline, fosfomycine (niet beschikbaar in België) en aminoglycosiden gebruikt.
De beschikbare gegevens voor de behandeling van die infecties waren, vóór de publicatie van de multicentrische studie AIDA (9), afkomstig van retrospectieve studies (4-7). Daarin werd gesuggereerd dat combinatietherapieën superieur waren aan monotherapieën. De meeste van die studies werden uitgevoerd voor de carbapenemaseproducerende Klebsiella pneumoniae KPC (5, 6).
Bitherapieën kunnen ook leiden tot de ontwikkeling van carbapenemresistente bacteriën en Clostridium difficile infecties (9).
In dit verband heeft het gerandomiseerd, gecontroleerd onderzoek AIDA de behandeling met «enkel colistine» vergeleken met de behandeling «colistine plus carbapenem» voor ernstige infecties met carbapenemresistente gram-negatieve bacillen. Uit de resultaten van deze studie is gebleken dat de bitherapie niet beter was dan de monotherapie «enkel colistine» in de groep Acinetobacter baumannii. Door de geringe significantie van de studie voor deze groep konden geen conclusies over Enterobacteriën worden getrokken. Opvallend is dat de meeste MIC voor meropenem in deze studie hoger waren dan 8 mg/l.
De door Vardakas et al (10) uitgevoerde meta-analyse waarbij de «combinatiebehandelingen colistine» werden vergeleken met de «enkel colistine behandeling» is tot het besluit gekomen dat de combinatiebehandeling de mortaliteit van ernstige carbapenemresistente GNB-infecties niet vermindert. Mogelijk is er een voordeel wanneer een hoge dosis colistine (>6 miljoen eenheden/dag) wordt toegediend bij patiënten met een bacteriëmie in Azië of een Acinetobacter baumannii infectie.
Op basis van deze studies kan dus niet worden vastgesteld wat de beste behandeling is voor ernstige CPE-infecties.
In ons overzicht van 29 gevallen van CPE OXA-48-achtige infecties, met een verschillende ernstgraad, werden voor de ernstige gevallen, bitherapieën voorgeschreven. Gelet op de MIC voor meropen <16 mg/ml, kon in de meeste gevallen meropenem worden voorgeschreven. Colistine werd gebruikt met een oplaaddosering van 9 miljoen eenheden ongeacht de nierfunctie, gevolgd door een onderhoudsdosering aangepast aan de creatinineklaring. Een Therapeutic Drug Monitoring (TDM) is niet uitgevoerd.
Infecties van de urinewegen zonder verwikkelingen konden worden behandeld met trimethoprim/sulfamethoxazole of nitrofurantoin, met een goed klinisch verloop.
De tritherapieën konden enkel in zeer ernstige gevallen worden voorgeschreven, wanneer het antibiogram de combinatie van 3 moleculen mogelijk maakte.
De met deze 29 OXA-48-achtige infecties geassocieerde mortaliteit is hoog, aangezien 31% patiënten is overleden. De meeste van die patiënten vertoonden verschillende comorbiditeitsfactoren.
Conclusie
Tot op vandaag zijn er geen duidelijke aanbevelingen voor de behandeling van ernstige CPE-infecties. De gerandomiseerde studies hebben nog niet formeel kunnen vaststellen dat de combinatietherapieën beter waren dan de monotherapieën.
Andere studies zijn nodig om deze behandeling te verduidelijken en idealiter in functie van het type carbapenemase.
Binnenkort worden nieuwe moleculen op de markt verwacht (ceftazidime+avibactam,meropenem-vaborbactam), waardoor er een ruimere keuze zal zijn uit het aantal bruikbare moleculen voor de behandeling van deze infecties, ook hier in functie van het type carbapenemase. Hopelijk leidt dit ook tot betere prognoses.
Referenties
1. Grundmann H, Glasner C, Albiger B, et al. Occurrence of carbapenemase-producing Klebsiella pneumoniae and Escherichia coli in the European survey of carbapenemase-producing Enterobacteriaceae (EuSCAPE): a prospective, multinational study. Lancet Infect Dis. 2017 Feb;17(2):153-163.
2. De Laveleye M, Huang TD, Bogaerts P, et al. Increasing incidence of carbapenemase-producing Escherichia coli and Klebsiella pneumoniae in Belgian hospitals. Eur J Clin Microbiol Infect Dis. 2017 Jan;36(1):139-146.
3. Huang TD, Bogaerts P, Berhin C, Hoebeke M, Bauraing C, Glupczynski Y; a multicentre study group. Increasing proportion of carbapenemase-producing Enterobacteriaceae and emergence of a MCR-1 producer through a multicentric study among hospital-based and private laboratories in Belgium from September to November 2015. Euro Surveill. 2017 May 11;22(19).
4. Balkan II, Aygün G, Aydın S, Mutcalı SI, et al. Blood stream infections due to OXA-48-like carbapenemase-producing Enterobacteriaceae: treatment and survival. Int J Infect Dis. 2014 Sep;26:51-6.
5. Daikos GL, Tsaousi S, Tzouvelekis LS, et al. Carbapenemase-producing Klebsiella pneumoniae bloodstream infections: lowering mortality by antibiotic combination schemes and the role of carbapenems. Antimicrob Agents Chemother. 2014;58(4):2322-8.
6. Tumbarello M, Viale P, Viscoli C, et al.Predictors of mortality in bloodstream infections caused by Klebsiella pneumoniaecarbapenemase-producing K. pneumoniae: importance of combination therapy. Clin
Infect Dis. 2012 Oct;55(7):943-50.
7. Gutiérrez-Gutiérrez B, Salamanca E, de Cueto M, Hsueh PR, et al. Effect of appropriate combination therapy on mortality of patients with bloodstream infections due to carbapenemase-producing Enterobacteriaceae (INCREMENT): a retrospective cohort study. Lancet Infect Dis. 2017 Jul;17(7):726-734.
8. Pletz MW, Hagel S, Forstner C. Who benefits from antimicrobial combination therapy? Lancet Infect Dis. 2017 Jul;17(7):677-678.
9. Paul M, Daikos GL, Durante-Mangoni E, Yahav D, Carmeli Y, et al. Colistin alone versus colistin plus meropenem for treatment of severe infections caused by carbapenem-resistant Gram-negative bacteria: an open-label, randomised controlled trial. Lancet Infect Dis. 2018 Apr;18(4):391-400.
10. Vardakas KZ, Mavroudis AD, Georgiou M, Falagas ME. Intravenous colistin combination antimicrobial treatment vs. monotherapy: a systematic review and meta-analysis. Int J Antimicrob Agents. 2018 Apr;51(4):535-547
11. EUCAST. Breakpoints table for interpretation of MICs and zone diameter 2016. www/eucast.org
Nieuwigheden
Wetenschappelijke agenda
- oktober 2024
-
van 16/10 tot 20/10 || in Los Angeles
SHEA ID week. A joint meeting of IDSA, SHEA, HIVMA, PIDS and SIDP
- november 2024
-
van 20/11 tot 22/11 || in Liverpool
Healthcare infection society
- april 2025
-
van 11/04 tot 15/04 || in Wenen
Congrès de l’ European Society of Clinical Microbiology and Infectious Diseases (ESCMID)
- juni 2025
-
van 4/06 tot 6/06 || in Marseille
35ème Congrès National de la Société Française d’Hygiène Hospitalière (SF2H)
-
van 17/06 tot 18/06 || in Londen
HIS congres (Healthcare Infection Society)