De lavabo als een potentiële bron voor de overdracht van carbapenemase producerende Enterobacteriaceae op de intensieve zorgenafdeling van het UZ Brussel.
Inleiding
Carbapenemase-producerende Enterobacteriaceae (CPE) vormen de dag van vandaag een grote bedreiging voor de volksgezondheid, zowel in de acute als de chronische gezondheidszorg, maar ook in de gemeenschap. Behandeling van patiënten geïnfecteerd met CPE is een uitdaging, aangezien maar een selectief aantal antibiotica in aanmerking komen. (Doi et al. (2015)).
Tussen 2010 en 2014 werd onze gezondheidsinstelling geconfronteerd met een stijgend aantal CPE positieve patiënten, met 26 geconfirmeerde gevallen tegen het einde van deze periode. Patiënten opgenomen op de intensieve zorgeneenheid (IZE) vormden het merendeel van alle gekoloniseerde en geïnfecteerde patiënten. Ondanks screening en grondige reiniging en desinfectie van de patiëntenomgeving steeg de incidentie verder in de eerste helft van 2015, wat gelinkt kon worden aan gecontamineerde lavabo’s.
Er wordt beschreven dat de afvoer van een ziekenhuislavabo 106-1010 kolonievormende eenheden (KVE)/ml bevat, waarvan bij benadering 103-105 KVE/ml Gram-negatieve bacillen. Deze bacteriën kunnen de patiënt koloniseren/infecteren via verschillende transmissieroutes. Ten eerste kan er aerosolvorming optreden wanneer er water uit de kraan stroomt. Deze aerosolen bevatten bacteriën afkomstig uit de afvoer, waardoor deze de omgeving van de patiënt kunnen contamineren. Ten tweede kunnen handen van gezondheidswerkers of medisch materiaal gebruikt bij de patiënt eveneens gecontamineerd raken en wanneer correcte handhygiëne of desinfectie van materiaal niet wordt toegepast, kunnen de bacteriën worden overgebracht naar de patiënt tijdens het patiëntencontact (Döring et al. (1991)). In de literatuur zijn reeds verschillende artikels verschenen waarbij de lavabo betrokken is bij uitbraken met (resistente) Gramnegatieve bacillen (Kramer et al. (2005); Lowe C et al. (2012)); Roux et al. (2013); Starlanger G et al. (2012); Wolf I et al. (2014)).
Het doel van deze studie was om een uitbraak van CPE te beschrijven in de IZE van het UZ Brussel (UZB) en om na te gaan of de lavabo hierin een rol gespeeld had. Bovendien werd ook onderzocht of dergelijke transmissies in de toekomst vermeden zouden kunnen worden door het verbeteren van infectiepreventie maatregelen en door het vervangen van de lavabo’s.
Onderzoeksmethoden
Setting
Het UZB heeft meer dan 700 bedden. Er zijn vier IZE voor volwassenen met elk zes bedden waarvan er twee in een isolatiekamer gelegen zijn (bed 1 (met sas) en bed 6). Elke IZE heeft acht lavabo’s ter beschikking, 1 bij elk bed en 2 centrale ter hoogte van de medicatietoog en in de spoelruimte.
CPE surveillance en isolatiepolitiek
Patiënten op de IZE worden rectaal gescreend bij opname, ontslag en wekelijks tijdens een langdurige opname. Wanneer een screening positief is, wordt de patiënt in contactisolatie geplaatst in een afzonderlijke kamer. De gezondheidsmedewerkers moeten handschoenen en een wegwerp beschermschort dragen.
Omgevingsreiniging
De kamer moet dagelijks gereinigd en gedesinfecteerd worden met Incidin® Plus (0.5% glucoprotamine). Bij ontslag wordt de kamer intensief gereinigd en gedesinfecteerd en wordt materiaal op de kamer, zoals handschoenen en handalcohol, weggegooid. Periodiek gebeuren er controles van de eindschoonmaak met de Glowcheck® (Hartmann, Heidenheim, Germany).
Microbiologische methoden
Swabs (eSwab, Copan, Brescia, Italië) van de afvoer (sifon) van de lavabo (10-15 cm diepte), de omgeving van de lavabo, en de kamer (high-touch oppervlakken zoals het bed, deurklink, velcro sluiting van de bloeddrukmetermanchet, matras en gordijn) werden op verschillende tijdstippen afgenomen en verwerkt volgens de standaard microbiologische methoden in het laboratorium na aanrijking. Voor de kweek werden selectieve chromogene platen gebruikt (chromID® CARBA en OXA-48 (bioMérieux, Marcy l’Etoile, Frankrijk)). Gevoeligheidsbepalingen werden geïnterpreteerd in functie van de EUCAST richtlijnen (The European Committee on Antimicrobial Susceptibility Testing).
Er werden eveneens stalen van de lucht afgenomen met de MAS-100® Airsampler (MerckMillipore, Darmstadt, Germany). De bacteriële aerosol werd gemeten 10 cm boven de lavabo wanneer er water uit de kraan stroomde en vergeleken met de resultaten in de setting waarbij de kraan dicht was. Er werd specifiek gezocht naar Gram-negatieve bacillen.
Resultaten
Epidemiologisch onderzoek
Tussen 2010 en 2015 steeg het aantal nieuwe patiënten per jaar met een CPE van 1 naar 21 met als predominant type het Klebsiella pneumoniae carbapenemase. In 2015 verbleef 67% van alle patiënten met een CPE op de IZE. Tussen januari en augustus 2015 ontwikkelden vijf patiënten, van wie de initiële screenings negatief waren, dragerschap/infectie met CPE tijdens hun verblijf op dezelfde IZE (verder IZE A genoemd), bed 6. De isolaten behoorden tot verschillende species met een verschillend antibiogram. De tijdspanne tussen de detectie van deze CPE positieve patiënten was relatief klein, en aangezien carbapenemase resistentiedeterminanten gelokaliseerd zijn op genetische mobiele elementen, werd de omgeving beschouwd als mogelijke bron van transmissie.
Omgevingsonderzoek
Swabs van zowel droge oppervlakken als uit de sifon van de lavabo werden op de IZE A, bed 6 afgenomen. Twee monsters werden positief voor CPE: de sifon van de lavabo en de de velcro sluiting van de bloeddrukmetermanchet van de bloeddrukmeter, desondanks de gebruikte reinigings- en desinfectieprocedure met Incidin®foam voor deze laatste. De monsters van de droge oppervlakken waren allen negatief voor CPE, wat aangeeft dat de reiniging afdoende was. Om na te gaan of de andere isolatiekamers ook CPE in hun afvoer droegen, werden deze eveneens bemonsterd. Behoudens 1 kamer, waren al de andere monsters positief voor CPE. Verschillende species en types van CPE werden geïsoleerd: Klebsiella pneumoniae NDM, Klebsiella pneumoniae KPC, Klebsiella pneumoniae OXA-48, Enterobacter cloacae complex OXA-48, Citrobacter freundii OXA-48, Citrobacter freundii OXA-48 + NDM, Klebsiella oxytoca/Raoultella species OXA-48 en Escherichia coli OXA-48, wat suggereerde dat resistentiegenen inderdaad accumuleerden in de afvoer. De resultaten toonden ook aan dat in sommige van de kamers, de bacteriële microbiota in de afvoer vermoedelijk dezelfde was als deze gekweekt uit de patiëntenstalen. Tussen eind juli en augustus 2015, waren vijf patiënten positief met CPE die vermoedelijk dezelfde waren als deze geïsoleerd uit de gootstenen. Drie van deze patiënten waren niet gekend met een CPE bij opname en in deze gevallen kan dus de hypothese gesteld worden dat de lavabo de transmissiebron was. Twee van deze patiënten hadden een respiratoire infectie met CPE.
In 2015 was Citrobacter freundii type OXA-48 de meest geïsoleerde kiem uit de gootstenen en patiënten. Om genetische verwantschap tussen de verschillende isolaten na te gaan, werd er pulsed field gel elektroforese (PFGE) uitgevoerd. Citrobacter freundii CPE positieve stammen van patiënten die verbleven op de IZE, geïsoleerd in 2013 en 2014, werden ook geïncludeerd. De resultaten zijn terug te vinden in Figuur 1 en tonen aan dat de stammen van de patiënten en verschillende monsters van de lavabo uit kamer 6 sterk verwant zijn.
Figuur 1: Fylogenetische verwantschap tussen Citrobacter freundii CPE (Carbapenemase producerende enterobacteriaceae) stammen.
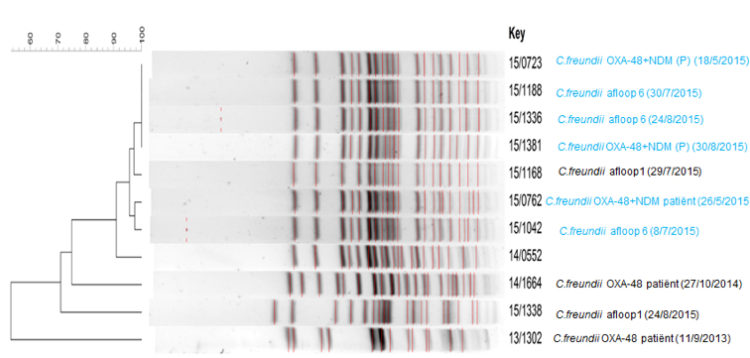
Op de linkerzijde van de figuur wordt er een dendogram weergegeven dat de genetische verwantschap uitdrukt in %. Aan de rechterzijde, worden in het blauw de culturen van Intensieve zorgen eenheid (IZE) A, bed 6 voorgesteld en in het zwart die van IZE A, bed 1, samen met de datum van isolatie. De stammen geïsoleerd uit de patiënten en lavabo van kamer zes zijn sterk verwant.
Infectiepreventie maatregelen
In de weken en maanden volgend op de voorgaande resultaten, probeerde het infectiepreventie team de uitbraak onder controle te krijgen door het implementeren van nieuwe maatregelen bovenop de reeds bestaande. Medische stafleden en verpleegkundigen werden geïnformeerd over de uitbraak, educatieve presentaties werden gegeven, het extreem belang van correcte handhygiëne werd nog eens extra in de verf gezet, en er gebeurde een controle op de eindschoonmaak na het ontslag van een besmette patiënt. Aangezien de velcro sluiting van de bloeddrukmetermanchet positief was met een CPE, werd beslist om te werken met wegwerp materiaal. Bovendien werd een overeenkomst gesloten met de technische dienst om alle sifons te vervangen in de isolatiekamers, en om deze van de andere kamers in cultuur te zetten. Een dagelijkse desinfectie van de lavabo’s met Incidin® Plus (bevat glucoprotamine, Microtek, Zutphen, Nederland) werd ingevoerd. Vóór deze uitbraak werden de lavabo’s in de IZE gebruikt voor het wassen van handen en medisch materiaal alvorens desinfectie, maar eveneens voor het doorspoelen van lichaamsvochten van patiënten zoals dialysevloeistoffen die antibiotica en micro-organismen bevatten. Deze acties kunnen biofilmvorming promoten en resistente bacteriën selecteren. Daarom werd beslist om de lavabo’s alleen te gebruiken voor “proper” werk. De dialysevloeistoffen vb. worden naar een centrale utility gebracht en daar in een slokop leeggemaakt, met aandacht voor het vermijden van spatten. .
Bij patiënten op IZE wordt door de kinesitherapeuten intermittente percussieventilatie toegepast met behulp van een ( Percussionaire® toestel van (Percussionaire Corp, Idaho, USA). De onderdelen van dit toestel die in rechtstreeks contact komen met de patiënt (Phasitron®), zijn herbruikbaar.. In het verleden werd dit na gebruik in de lavabo op de kamer gedemonteerd en gereinigd met kraantjeswater en zeep, gevolgd door een desinfectie met alcohol 70%. Bij ontslag van de patiënt gaan de hulpstukken naar de centrale sterilisatieafdeling voor desinfectie. Aangezien de geïnfecteerde site met CPE meestal de longen betrof bij de patiënten, werd er beslist om de procedure na elke behandeling aan te passen de hulpstukken worden nu gedroogd met een wegwerp doekje en vervolgens behandeld met alcohol 70%.
Opvolging
Tussen september en eind december 2015, werden swabs uit de afvoer van de sifon genomen op regelmatige basis in elke kamer van elke IZE. Desondanks bovenstaande maatregelen, waren nog steeds 9 van de 32 sifons (28%) positief met CPE eind september 2015. Tijdens deze periode vertoonden drie patiënten een positief monster met CPE. Twee van hen waren reeds positief bij opname. Een derde patiënt had een respiratoire infectie met CPE, maar in zijn geval was het onmogelijk te beoordelen of hij dit nosocomiaal verworven had aangezien hij niet gescreend werd bij opname. Omwille van het hoog aantal sifons dat een CPE bevatte, zelfs na vervanging, werd er beslist om de complete lavabo’s te vervangen door nieuwe die een andere design hadden (open inlet zonder rooster, gladde wand zonder openingen) (Figuur 2). Dit ontwerp zorgt ervoor dat de schoonmaak gemakkelijker is en bovendien wordt de vorming van biofilm verhinderd.
Figuur 2: Nieuw design van lavabo’s in de intensieve zorgeneenheid (IZE).

Deel 1 past in deel 2 en samen passen ze in deel 3. De binnenzijde van deel 1 is glad zonder gaten, wat in contrast staat met het vorig ontwerp van de lavabo’s. De vorige lavabo’s waren voorzien van een rooster (foto 4), terwijl de nieuwe een open afvoer hebben. Dit alles maakt reiniging gemakkelijker en voorkomt extra biofilmvorming. Foto 5 toont de hele lavabo.
In het algemeen waren er tussen 1 januari en 31 december 2015, 21 patiënten die gekoloniseerd/geïnfecteerd geraakten toen ze gehospitaliseerd waren op de IZE, waarvan 8 vermoedelijk door een gecontamineerde lavabo. Sinds de vervanging van de complete lavabo’s op het einde van 2015, werd slechts 1 patiënt positief met CPE (maart 2016), nadat hij verbleven had op de IZE. Op dat ogenblik was hij reeds vier weken gehospitaliseerd. De afvoer van de lavabo in de kamer waar deze patiënt verbleven had, was positief met een CPE, maar dit ging over een ander species en stam. In dit geval was het moeilijk te zeggen of de transmissie van CPE gebeurde van de patiënt naar de lavabo of vice versa aangezien de patiënt niet gescreend werd bij opname. De andere lavabo’s bleven negatief tot op de laatste dag van de staalname en andere mogelijke transmissies werden niet vastgesteld.
Airsampling experimenten met twee lavabo’s toonden aan dat het mogelijk was dat bacteriën in de biofilm van de sifon los kunnen geraken en verstrooid worden in de lucht erboven wanneer er water stroomt, aangezien we in staat waren om Gram-negatieve bacteriën op te pikken in de lucht boven de afvoer en de omgeving van de lavabo wanneer de kraan open stond. In de lucht werden Stenotrophomonas maltophilia, Serratia marcescens, Pseudomonas oleovorans groep en Pseudomonas putida geïsoleerd. Op de kranen werden Serratia marcescens en Pseudomonas fluorescens groep teruggevonden en op de lavabo zelf een multiresistente Serratia marcesens en Stenotrophomonas maltophila.
Discussie
De prevalentie van infecties met multiresistente Gram-negatieve bacteriën zoals CPE stijgt wereldwijd (Hoxha et al. (2016)) en vermoedelijk bestaat er een grotere waaier aan omgevingsreservoirs voor dergelijke bacteriën in vergelijking met Gram-positieve multiresistente kiemen (Wilson et al. (2016)). Zowel de resultaten in deze studie als in de literatuur tonen aan dat de lavabo een ideaal vochtig reservoir is voor de overleving van Gram-negatieve bacillen. Het feit dat antibioticabevattende vloeistoffen vaak werden doorgespoeld via de lavabo, zorgt ervoor dat de selectie van resistente bacteriële stammen gestimuleerd wordt. Desondanks de inspanningen die geleverd werden en het stoppen van de uitbraak met CPE op kamer 6 van de IZE A, werden er nog multiresistente Pseudomonas species en Stenotrophomonas maltophilia gekweekt uit de afvoer. Deze bacteriën kunnen eveneens patiënten gaan koloniseren/infecteren en we stelden dan ook effectief vast dat sommige patiënten positieve respiratoire stalen vertoonden met deze species na enkele dagen hospitalisatie op de IZE (data niet weergegeven). Er werd echter geen moleculaire analyse uitgevoerd om deze hypothese te bevestigen. Staalname van de lucht boven en de omgeving rondom de lavabo leerde ons dat het mogelijk is dat bacteriën uit de sifon losgeraken wanneer de kraan opengedraaid wordt. Handen van gezondheidswerkers kunnen op die manier gecontamineerd geraken. Dit gegeven onderlijnt nog eens het extreem belang van handhygiëne.
De komende jaren zal er een nieuwe IZE gebouwd worden in het UZ Brussel. Enkele voorstellen met betrekking tot de architectuur van de kamer en de lavabo kunnen gemaakt worden. In de eerste plaats moet er overwogen worden om kamers te bouwen zonder lavabo. Deze werden tot voor kort gebruikt om herbruikbaar materiaal af te spoelen alvorens desinfectie, als “afvalvaten” en als watervoorziening bij het scheren. Er werd afgesproken dat herbruikbaar materiaal naar de centrale centralisatie-eenheid gebracht moet worden, scheren kan gebeuren door een aparte waskom te gebruiken en lichaamsvochten/dialysevloeistoffen van de patiënt moeten verwijderd worden via speciale afvalcontainers die gemakkelijk te transporteren zijn. Een tweede mogelijkheid is om een kamer te construeren met twee aparte lavabo’s. Eén daarvan zou strikt gelimiteerd moeten worden tot handen wassen. De andere lavabo, gebruikt voor het verwijderen van lichaamsvloeistoffen, moet systematisch beschouwd worden als potentieel gecontamineerd.
In onze IZE is de afstand tussen het bed en de lavabo minder dan 1 m. Er bestaan geen richtlijnen over deze minimaal vereiste afstand, en dit hangt ook af van de constructie van de lavabo, maar zoals beschreven wordt in de literatuur, kunnen aerosolen en spatten komende van de afvoer van de lavabo tot wel 1 m ver reiken wanneer de kraan opengedraaid wordt (Hota S. et al. (2009)). Wij zouden daarom aanraden om als minimale afstand tussen bed en lavabo 2 m meter te hanteren.
In onze IZE bestaan er twee types van kranen. De kranen in de isolatiekamers zijn correct opgebouwd met een afstand tussen de kraan en de ingang van de lavabovan 40 cm (Figuur 3A). Bij de kranen in de standaardkamers daarentegen is er slechts een afstand van 20 cm tussen de kraan en de ingang van de afvoer van de lavabo (Figuur 3B). Op die manier kan de kraan gecontamineerd geraken door spatten wanneer het water stroomt. Bovendien stroomt het water in de standaardkamers loodrecht in de afvoer, wat terugspatten in de hand werkt (Ambrogi et al. (2016)). In de toekomst zullen deze types van kranen vervangen worden.
Figuur 3: Kranen in de isolatiekamers (A) en in de standaardkamers (B).

Glucoprotamine is een breedspectrum desinfectans en kan de bacteriële load in de afvoer verminderen. Het heeft echter geen effect op de vorming van biofilm en het zou beter zijn moest er geopteerd worden om een andere chemische stof te kiezen die hier wel werkzaam op is. Een mogelijkheid beschreven in de literatuur is azijnzuur (Aspelund et al. (2016)).
Een Duitse firma bracht een zelf-desinfecterende sifon op de markt (MoveoSiphon ST24, MoveoMed, Dresden, Duitsland) (Figuur 4). Dit toestel voorkomt de vorming van een biofilm door permanente fysische desinfectie, elektromagnetische reiniging en antibacteriële coating (Sissoko et al. (2004)). Deze sifon werd getest op de aanwezigheid van Gram-negatieve bacillen gedurende vijf maanden (juli- november 2016) in de IZE A, kamer 1. Tijdens deze hele periode werd er geen enkele Gram-negatieve bacil opgepikt. Desondanks deze veelbelovende resultaten, moet er nog onderzocht worden of deze sifon werkelijk zorginfecties kan voorkomen in onze IZE en of deze interventie kosten-effectief is.
Figuur 4: Plaatsing van de MoveoSiphon ST24
Conclusie
Er kan besloten worden dat de omgeving een belangrijk reservoir vormt voor multiresistente Gram-negatieve bacillen zoals aangetoond in deze CPE uitbraak, gelinkt aan gecontamineerde gootstenen. De nodige inspanningen leidden tot het stoppen van de uitbraak met CPE, maar tot op heden worden nog steeds multiresistente Pseudomonas species in de afvoer gevonden. Daarom is het nodig dat mensen uit de verschillende disciplines (medisch personeel, technische dienst, ziekenhuishygiëne etc…) samenzitten en nadenken over hoe een “ideale” patiëntenkamer er uit kan zien, uiteraard ook rekening houdend met het economisch aspect.
Referenties
1. Ambrogi V, Cavalié L, Mantion B, Ghiglia MJ, Cointault O, Dubois D, Prère MF, Levitzki N, Kamar N, Malavaud S. Transmission of metallo-β-lactamase-producing Pseudomonas aeruginosa in a nephrology-transplant intensive care unit with potential link to the environment. J Hosp Infect. 2016 Jan; 92(1):27-9.
2. Stjärne Aspelund A, Sjöström K, Olsson Liljequist B , Mörgelin M , Melander E , Pahlmzn LI. Acetic acid as a decontamination method for sink drains in a nosocomial outbreak of metallo-β-lactamase-producing Pseudomonas aeruginosa. J Hosp Infect. 2016 Sep; 94(1):13-20
3. Doi Y, Paterson DL. Carbapenemase-producing Enterobacteriaceae. Semin Respir Crit Care Med. 2015; 36(1):74–84.
4. Döring G, Ulrich M, Müller W, Bitzer J, Schmidt-Koenig L, Münst L, Grupp H, Wolz C, Stern M, Botzenhart K. Generation of Pseudomonas aeruginosa aerosols during handwashing from contaminated sink drains, transmission to hands of hospital personnel, and its prevention by use of a new heating device. Zentralbl Hyg Umweltmed. 1991; 191(5–6):494–505.
5. Hota S, Hirji Z, Stockton K, Lemieux C, Dedier H, Wolfaardt G, Gardam MA. Outbreak of multidrug-resistant Pseudomonas aeruginosa colonization and infection secondary to imperfect intensive care unit room design. Infect Control Hosp Epidemiol. 2009 Jan; 30(1):25-33.
6. Kramer A, Daeschlein G, Niesytto C, Sissoko B, Sütterlin R, Blaschke M, Fusch C. Contamination of sinks and emission of nosocomial gramnegative pathogens in a NICU – outing of a reservoir as risk factor for nosocomial colonization and infection. Umweltmed. Forsch. Prax. 2005; 10(5):327.
7. Leitner E, Zarfel G, Luxner J, Herzog K, Pekard-Amenitsch S, Hoenigl M, Valentin T, Feierl G, Grisold A, Högenauer C, Sill H, Krause R, Zollner-Schwetzd I. Contaminated Handwashing Sinks as the Source of a Clonal Outbreak of KPC-2-Producing Klebsiella oxytoca on a Hematology Ward. AAC. 2015; 59(1):714–6.
8. Lowe C, Willey B, O’Shaughnessy A, Lee W, Lum M, Pike K, Larocque C, Dedier H, Dales L, Moore C. Outbreak of extended-spectrum β-lactamase-producing Klebsiella oxytoca infections associated with contaminated handwashing sinks. Emerg Infect Dis. 2012; 18(8):1242–7.
9. Roux D, Aubier B, Cochard H, Quentin R, van der Mee-Marquet N. Contaminated sinks in intensive care units: an underestimated source of extended-spectrum beta-lactamase-producing Enterobacteriaceae in the patient environment. J Hosp Infect. 2013; 85(2):106–11.
10. Starlander G, Melhus Å. Minor outbreak of extended-spectrum β-lactamase-producing Klebsiella pneumoniae in an intensive care unit due to a contaminated sink. J Hosp Infect. 2012; 82(2):122–4.
11. Wolf I, Bergervoet P, Sebens F, van den Oever H, Savelkoul P, van der Zwet W. The sink as a correctable source of extended-spectrum β-lactamase contamination for patients in the intensive care unit. J Hosp Infect
Afkortingenlijst
CPE: Carbapenemase-producerende Enterobacteriaceae
EUCAST: The European Committee on Antimicrobial Susceptibility Testing
IZE: intensieve zorgeneenheid
KVE: kolonievormende eenheden
UZB: Universitair Ziekenhuis Brussel
Nieuwigheden
Wetenschappelijke agenda
- oktober 2024
-
van 16/10 tot 20/10 || in Los Angeles
SHEA ID week. A joint meeting of IDSA, SHEA, HIVMA, PIDS and SIDP
- november 2024
-
van 20/11 tot 22/11 || in Liverpool
Healthcare infection society
- april 2025
-
van 11/04 tot 15/04 || in Wenen
Congrès de l’ European Society of Clinical Microbiology and Infectious Diseases (ESCMID)
- juni 2025
-
van 4/06 tot 6/06 || in Marseille
35ème Congrès National de la Société Française d’Hygiène Hospitalière (SF2H)
-
van 17/06 tot 18/06 || in Londen
HIS congres (Healthcare Infection Society)




